锂空气电池放电时的工作原理如图所示。下列叙述正确的是


| A.放电时Li+由B极向A极移动 |
| B.电池放电时总反应方程式为4Li+O2 +2H2O===4LiOH |
| C.电解液a、b之间可采用阴离子交换膜 |
| D.电解液a可能为LiCl水溶液 |
更新时间:2018/03/15 15:53:00
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+ AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液.下列叙述中正确的是
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液.下列叙述中正确的是
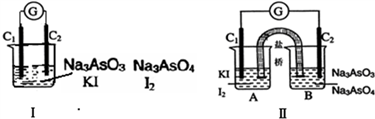
 AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液.下列叙述中正确的是
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液.下列叙述中正确的是
| A.乙组操作时,C2做正极 |
| B.乙组操作时,C1上发生的电极反应为I2+2e-═2I- |
| C.甲组操作时,电流表(G)指针发生偏转 |
| D.甲组操作时,溶液颜色变深 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
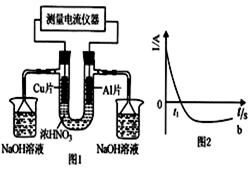
【推荐2】SO2通过下列工艺流程可以制取化工原料H2SO4和清洁能源H2。下列说法正确的是
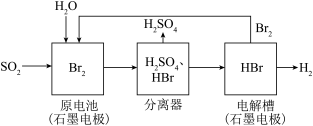

| A.电解槽中也可以用铁电极代替石墨作为阳极 |
B.原电池中负极的电极反应为:SO2+2H2O-4e-=SO +4H+ +4H+ |
| C.该工艺流程用总反应的化学方程式表示为:SO2+Br2+2H2O=2HBr+H2SO4 |
| D.该生产工艺的优点是Br2被循环利用,原电池产生的电能可以充分利用,还能获得清洁能源 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】钠离子电池具有充电速度快和低温环境性能优越的特点,其电极材料的导电聚合物中掺杂磺酸基可增强其电化学活性,其工作原理如图所示。下列说法正确的是
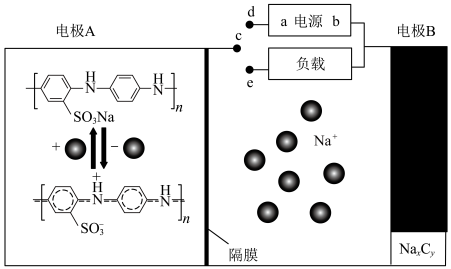
A. 连接 连接 时, 时, 透过隔膜进入电极 透过隔膜进入电极 室 室 |
B. 连接 连接 时,电源 时,电源 极的电势比 极的电势比 极低 极低 |
C. 连接 连接 时,每转移 时,每转移 ,两电极质量变化相差 ,两电极质量变化相差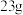 |
D. 连接 连接 时, 时, 的电极反应为: 的电极反应为: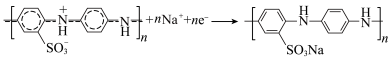 |
您最近一年使用:0次
单选题-单题
|
较难
(0.4)
解题方法
【推荐2】科学家用氮化镓材料与铜组装成如图所示的人工光合系统,实现 的再利用。电池的总反应为:
的再利用。电池的总反应为: (已知:质子交换膜仅允许
(已知:质子交换膜仅允许 通过),下列说法正确的是
通过),下列说法正确的是
 的再利用。电池的总反应为:
的再利用。电池的总反应为: (已知:质子交换膜仅允许
(已知:质子交换膜仅允许 通过),下列说法正确的是
通过),下列说法正确的是 
A.该装置的电解质溶液可能为 |
| B.电子从GaN电极流出经过电解质溶液到Cu电极 |
C.理论上生成11.2L 质子交换膜通过 质子交换膜通过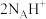 |
D.Cu电极上发生的电极反应是: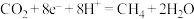 |
您最近一年使用:0次

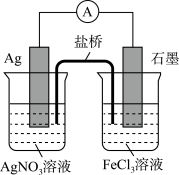
 Ag++Fe2+设计成如图所示的原电池装置(已知电流表指针偏向与电子的流向相同)。下列有关判断不正确的是
Ag++Fe2+设计成如图所示的原电池装置(已知电流表指针偏向与电子的流向相同)。下列有关判断不正确的是