化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素。少量A与水反应完全水解但不发生氧化或还原反应,所有反应产物均可溶于水。将A配成水溶液稀释后分成几份,分别加入一系列0.1mol/L的试剂,现象如下:
①加入硝酸酸化的硝酸银,产生白色沉淀;
②加入氯化钡溶液,无沉淀产生;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀。
(1)由①判断组成该化合物的元素中,肯定存在的卤素有_____ ,由②判断A与水反应后生成的溶液中肯定不存在的离子有________ 。由③判断A与水反应后生成的溶液中肯定存在的离子有___________ ;
(2)要确定该化合物的分子式,称取11.90gA溶于水稀释至250.00mL,取25.00mL溶液加入足量的高锰酸钾和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重为2.33g。试确定A的化学式_______ ,写出计算推理过程。
①加入硝酸酸化的硝酸银,产生白色沉淀;
②加入氯化钡溶液,无沉淀产生;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀。
(1)由①判断组成该化合物的元素中,肯定存在的卤素有
(2)要确定该化合物的分子式,称取11.90gA溶于水稀释至250.00mL,取25.00mL溶液加入足量的高锰酸钾和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重为2.33g。试确定A的化学式
10-11高二·全国·阶段练习 查看更多[1]
(已下线)2010—2011学年高二年级高考复习方案配套课标版(二)月考化学试卷
更新时间:2016-12-09 01:37:32
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有一瓶澄清的溶液,其中可能含有NH 、K+、Ba2+、Al3+、Fe3+、I-、
、K+、Ba2+、Al3+、Fe3+、I-、 、
、 、SO
、SO 、
、 。取该溶液进行以下实验:
。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液:a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除_______ 的存在。
(2)由②可以证明_______ 的存在,同时排除_______ 的存在。
(3)由③可以证明_______ 的存在;写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:c._______ ;d._______ 。
(4)由④可以证明_______ 的存在。
 、K+、Ba2+、Al3+、Fe3+、I-、
、K+、Ba2+、Al3+、Fe3+、I-、 、
、 、SO
、SO 、
、 。取该溶液进行以下实验:
。取该溶液进行以下实验:①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液:a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
(4)由④可以证明
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某溶液中只含有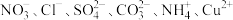 和
和 中的某几种离子,且离子数目均相等。某实验兴趣小组同学取
中的某几种离子,且离子数目均相等。某实验兴趣小组同学取 该溶液,平均分成2份,进行以下操作:
该溶液,平均分成2份,进行以下操作:
Ⅰ.①第一份溶液中加入过量 溶液,加热,产生
溶液,加热,产生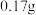 氨气,同时产生蓝色沉淀
氨气,同时产生蓝色沉淀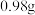 ,过滤、洗涤、干燥、灼烧,得到一定量黑色固体。
,过滤、洗涤、干燥、灼烧,得到一定量黑色固体。
②向上述滤液中加入足量 溶液,过滤,洗涤、干燥,得到
溶液,过滤,洗涤、干燥,得到 沉淀,加入足量的盐酸沉淀质量不变。
沉淀,加入足量的盐酸沉淀质量不变。
Ⅱ.第二份溶液中加入过量的 溶液,取上层清液加入足量
溶液,取上层清液加入足量 溶液,得到白色沉淀,经过滤、洗涤、干燥后加入稀硝酸沉淀不溶解且沉淀质量没有变化。
溶液,得到白色沉淀,经过滤、洗涤、干燥后加入稀硝酸沉淀不溶解且沉淀质量没有变化。
已知: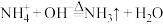
由上述分析可知:
(1)该溶液一定不存在的离子为___________ (填离子符号)。
(2)操作Ⅰ中②“不溶于盐酸的沉淀”为___________ (填化学式)。
(3)溶液中可能存在的离子为___________ (填离子符号),检验阳离子存在的实验方法称为___________ ;可能存在阴离子是否需要检验,请说明理由___________ 。
(4)常用氨气检验液氯管道是否发生泄漏,反应原理: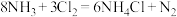 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为___________ 。
(5)在操作Ⅱ中,加入过量的 溶液的目的是
溶液的目的是___________ 。
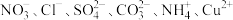 和
和 中的某几种离子,且离子数目均相等。某实验兴趣小组同学取
中的某几种离子,且离子数目均相等。某实验兴趣小组同学取 该溶液,平均分成2份,进行以下操作:
该溶液,平均分成2份,进行以下操作:Ⅰ.①第一份溶液中加入过量
 溶液,加热,产生
溶液,加热,产生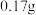 氨气,同时产生蓝色沉淀
氨气,同时产生蓝色沉淀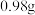 ,过滤、洗涤、干燥、灼烧,得到一定量黑色固体。
,过滤、洗涤、干燥、灼烧,得到一定量黑色固体。②向上述滤液中加入足量
 溶液,过滤,洗涤、干燥,得到
溶液,过滤,洗涤、干燥,得到 沉淀,加入足量的盐酸沉淀质量不变。
沉淀,加入足量的盐酸沉淀质量不变。Ⅱ.第二份溶液中加入过量的
 溶液,取上层清液加入足量
溶液,取上层清液加入足量 溶液,得到白色沉淀,经过滤、洗涤、干燥后加入稀硝酸沉淀不溶解且沉淀质量没有变化。
溶液,得到白色沉淀,经过滤、洗涤、干燥后加入稀硝酸沉淀不溶解且沉淀质量没有变化。已知:
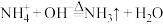
由上述分析可知:
(1)该溶液一定不存在的离子为
(2)操作Ⅰ中②“不溶于盐酸的沉淀”为
(3)溶液中可能存在的离子为
(4)常用氨气检验液氯管道是否发生泄漏,反应原理:
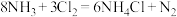 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为(5)在操作Ⅱ中,加入过量的
 溶液的目的是
溶液的目的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某溶液甲中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 八种离子中的若干种。为确定甲溶液的组成,取100mL的甲溶液,进行如下实验:
八种离子中的若干种。为确定甲溶液的组成,取100mL的甲溶液,进行如下实验:
①向甲溶液中滴加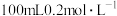 的
的 溶液过滤,得到不溶于酸的白色沉淀2.33g和蓝色滤液乙
溶液过滤,得到不溶于酸的白色沉淀2.33g和蓝色滤液乙
②取滤液乙,先用硝酸酸化,再加足量的硝酸银溶液,过滤得2.87g沉淀及滤液丙
据此,请回答下列问题(用相应的离子符号表示):
(1)上述实验①中生成沉淀的离子方程式为___________ 。
(2)甲溶液中一定不存在的离子是___________ (填离子符号,下同);可能存在的离子是___________ 。
(3)甲溶液里一定存在的离子中,物质的量浓度能确定的离子是___________ 。物质的量浓度不能确定的离子是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 八种离子中的若干种。为确定甲溶液的组成,取100mL的甲溶液,进行如下实验:
八种离子中的若干种。为确定甲溶液的组成,取100mL的甲溶液,进行如下实验:①向甲溶液中滴加
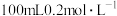 的
的 溶液过滤,得到不溶于酸的白色沉淀2.33g和蓝色滤液乙
溶液过滤,得到不溶于酸的白色沉淀2.33g和蓝色滤液乙②取滤液乙,先用硝酸酸化,再加足量的硝酸银溶液,过滤得2.87g沉淀及滤液丙
据此,请回答下列问题(用相应的离子符号表示):
(1)上述实验①中生成沉淀的离子方程式为
(2)甲溶液中一定不存在的离子是
(3)甲溶液里一定存在的离子中,物质的量浓度能确定的离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】从海水或盐湖水中直接制得的粗盐中含有不溶性的泥沙和CaCl2、MgCl2、Na2SO4等杂质,某实验小组用这种粗盐样品来提取纯净的NaCl固体,实验步骤如下:
(1)取适量该样品加水溶解后过滤,目的是:_________________________________________________
(2)检验滤液中仍然还含有SO42—的方法是:_____________________________________________________
(3)为了除去NaCl溶液中的可溶性杂质,还需要向溶液中依次加入下列化学试剂:①BaCl2溶液; ②NaOH溶液; ③Na2CO3溶液。其中加入试剂③反应时的化学方程式为:___________________________________________________________
(4)反应结束后,过滤,向滤液中加入适量盐酸,就得到不含杂质的NaCl溶液。加入盐酸的作用是________________________
(5)最后蒸发NaCl溶液中得到不含杂质的NaCl固体。该实验要用到的玻璃仪器有:_____________ (填仪器名称)
(1)取适量该样品加水溶解后过滤,目的是:
(2)检验滤液中仍然还含有SO42—的方法是:
(3)为了除去NaCl溶液中的可溶性杂质,还需要向溶液中依次加入下列化学试剂:①BaCl2溶液; ②NaOH溶液; ③Na2CO3溶液。其中加入试剂③反应时的化学方程式为:
(4)反应结束后,过滤,向滤液中加入适量盐酸,就得到不含杂质的NaCl溶液。加入盐酸的作用是
(5)最后蒸发NaCl溶液中得到不含杂质的NaCl固体。该实验要用到的玻璃仪器有:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某盐的无色溶液中同时有Cl-、SO42-,检验时,应先检验________ 离子,首先取少量待测液于试管中,向其中加入试剂__________ 且至________ 时,经过________ 操作后,再用试剂___________ 检验另一种离子。
您最近一年使用:0次
【推荐3】某课题组同学查阅文献知:3(NH4)2SO4(s)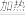 4NH3↑+3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):
4NH3↑+3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):
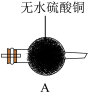
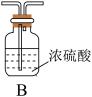
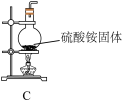
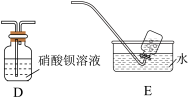
回答下列问题:
(1)仪器A的名称是___________ 。
(2)甲组同学选择上图装置来证明该气体中有H2O、NH3、SO2的存在。
①装置的链接顺序为:C→_____ →_____ →______ →E;
②能证明有水生成的实验现象是_____________________________________________ ;
③B瓶的作用是_________________________ ,实验一段时间后,若要检验新生成的阳离子,具体操作是______________________________________________________ 。
(3)实验中,观察到D装置产生白色沉淀。该白色沉淀的化学式:____________ ;
(4)D装置中发生的反应与硝酸钡的量有关,若硝酸钡足量,则D中反应的离子方程式为__________________________________________________________ 。
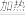 4NH3↑+3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):
4NH3↑+3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):



回答下列问题:
(1)仪器A的名称是
(2)甲组同学选择上图装置来证明该气体中有H2O、NH3、SO2的存在。
①装置的链接顺序为:C→
②能证明有水生成的实验现象是
③B瓶的作用是
(3)实验中,观察到D装置产生白色沉淀。该白色沉淀的化学式:
(4)D装置中发生的反应与硝酸钡的量有关,若硝酸钡足量,则D中反应的离子方程式为
您最近一年使用:0次
【推荐1】纯碱(Na2CO3)在生产生活中具有广泛的用途.如图1是实验室模拟制碱原理制取Na2CO3的流程图.
完成下列填空:
已知:粗盐中含有Ca2+、Mg2+、SO42﹣等杂质离子.
(1)精制除杂的步骤顺序是____ →___ →____ →____ →____ (填字母编号).
a 粗盐溶解 b 加入盐酸调pH c 加入Ba(OH)2溶液 d 加入Na2CO3溶液 e 过滤
(2)向饱和食盐水中先通入NH3,后通入CO2,理由是______ .在滤液a中通入NH3和加入精盐的目的是______ .
(3)请在图1流程图中添加两条物料循环的路线.____
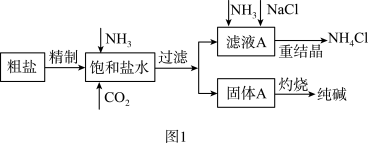
(4)图2装置中常用于实验室制备CO2的是__ (填字母编号);用c装置制备NH3,烧瓶内可加入的试剂是___ (填试剂名称).
(5)一种天然碱晶体成分是aNa2CO3•bNa2SO4•cH2O,利用下列提供的试剂,设计测定Na2CO3质量分数的实验方案.请把实验方案补充完整:
供选择的试剂:稀H2SO4、BaCl2溶液、稀氨水、碱石灰、Ba(OH)2溶液
①______ .
②______ .
③______ .
④计算天然碱晶体中含Na2CO3的质量分数.
完成下列填空:
已知:粗盐中含有Ca2+、Mg2+、SO42﹣等杂质离子.
(1)精制除杂的步骤顺序是
a 粗盐溶解 b 加入盐酸调pH c 加入Ba(OH)2溶液 d 加入Na2CO3溶液 e 过滤
(2)向饱和食盐水中先通入NH3,后通入CO2,理由是
(3)请在图1流程图中添加两条物料循环的路线.

(4)图2装置中常用于实验室制备CO2的是

(5)一种天然碱晶体成分是aNa2CO3•bNa2SO4•cH2O,利用下列提供的试剂,设计测定Na2CO3质量分数的实验方案.请把实验方案补充完整:
供选择的试剂:稀H2SO4、BaCl2溶液、稀氨水、碱石灰、Ba(OH)2溶液
①
②
③
④计算天然碱晶体中含Na2CO3的质量分数.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为测定某工业碱(组成为xNa2CO3·yNaHCO3)中Na2CO3的质量分数,甲、乙、丙三名同学分别设计并完成了如下实验:
甲同学:准备称取11.40 g样品利用图中装置进行实验,反应后测定装置C中碱石灰增重5.06g。
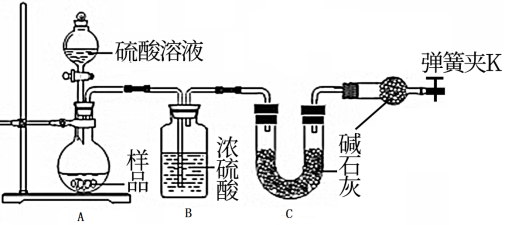
乙同学:准确称取11.40 g研细的样品,加热样品至固体完全分解,剩余固体质量为9.54 g.
丙同学:准确称取11. 40 g样品,配成1000 mL溶液,量取25. 00 mL溶液于锥形瓶中,加入指示剂,用0.1500 mol/L标准盐酸溶液滴定至终点。完成三次平行实验后,消耗盐酸的体积平均为30.00 mL。
(1)如何检查甲同学实验装置的气密性?_______________ 。
(2)①乙同学需要在______ (填仪器名称,下同)将样品研细,在______ 中加热样品;
②乙同学在实验时需要将固体加热一段时间然后冷却,称量,再加热、冷却、称量,直至最后两次称量的质量差不超过0.10 g,其目的是___________ 。
(3)丙同学在实验之前为了确定晶体中是否含有NaHCO3,设计了以下实验方案进行检验。
实验步骤:取少量样品于锥形瓶中加入适量蒸馏水使之溶解,加入几滴酚酞,用0.100mol/L盐酸滴定至溶液由浅红色变无色,记录消耗盐酸的体积为V1;______ (填实验操作),记录消耗盐酸的体积为V2,若V2_____ V1(填“<、>或=”),说明晶体中含有NaHCO3.
(4)请分析、计算后回答。
①_____ 同学实验结果错误,其实验失败的原因是___________ 。
②晶体中Na2CO3的质量分数为____________ 。(计算结果保留4位有效数字)
甲同学:准备称取11.40 g样品利用图中装置进行实验,反应后测定装置C中碱石灰增重5.06g。

乙同学:准确称取11.40 g研细的样品,加热样品至固体完全分解,剩余固体质量为9.54 g.
丙同学:准确称取11. 40 g样品,配成1000 mL溶液,量取25. 00 mL溶液于锥形瓶中,加入指示剂,用0.1500 mol/L标准盐酸溶液滴定至终点。完成三次平行实验后,消耗盐酸的体积平均为30.00 mL。
(1)如何检查甲同学实验装置的气密性?
(2)①乙同学需要在
②乙同学在实验时需要将固体加热一段时间然后冷却,称量,再加热、冷却、称量,直至最后两次称量的质量差不超过0.10 g,其目的是
(3)丙同学在实验之前为了确定晶体中是否含有NaHCO3,设计了以下实验方案进行检验。
实验步骤:取少量样品于锥形瓶中加入适量蒸馏水使之溶解,加入几滴酚酞,用0.100mol/L盐酸滴定至溶液由浅红色变无色,记录消耗盐酸的体积为V1;
(4)请分析、计算后回答。
①
②晶体中Na2CO3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为研究生命起源,科研人员发现了120多种含铁硫簇(如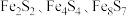 等)的酶和蛋白质,它们是存在于生物体的最古老的生命物质之一、为研究某铁硫簇结构
等)的酶和蛋白质,它们是存在于生物体的最古老的生命物质之一、为研究某铁硫簇结构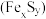 的组成,某化学兴趣小组设计了下列实验:
的组成,某化学兴趣小组设计了下列实验:
实验Ⅰ:测定硫的质量
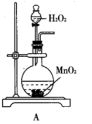
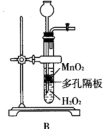
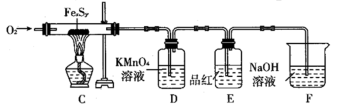
(1)实验过程中使用装置A制备氧气,___________ (填“能”或“不能”)使用装置B代替装置A。
(2)检查装置的气密性后,在C中放入ag铁硫簇的样品(含有不溶于水和盐酸的杂质),在E中加入品红溶液,在D中加入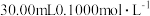 的酸性
的酸性 溶液。写出实验过程中仪器D中发生的离子反应方程式:
溶液。写出实验过程中仪器D中发生的离子反应方程式:___________ 。
(3)通入氧气并加热,发现C中固体逐渐转变为红棕色。待固体完全转化后,取D中的 溶液15.00mL,用0.1000mol/L碘化钾溶液进行滴定。记录数据如下:
溶液15.00mL,用0.1000mol/L碘化钾溶液进行滴定。记录数据如下:
①滴定终点的颜色变化为___________ 。
②滴定过程中发生的离子反应为___________ 。
③计算ag铁硫簇的样品中含有S的物质的量为___________ 。
实验Ⅱ:测定铁的质量
(4)取实验Ⅰ硬质玻璃管C中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经灼烧得0.32g固体。通过计算,可以得出该铁硫簇的化学式为___________ 。
实验Ⅲ:问题研讨
(5)①有同学提出,撤去E装置,对实验没有影响,你的看法是___________ (填“合理”或“不合理”),理由是___________ 。
②下列操作,可能引起x∶y偏大的是___________ 。
a.滴定剩余 溶液时,KI溶液滴到锥形瓶外边一滴
溶液时,KI溶液滴到锥形瓶外边一滴
b.配制标准KI溶液时,定容时俯视刻度线
c.用碘化钾溶液滴定剩余 溶液时,滴定前有气泡,滴定后无气泡
溶液时,滴定前有气泡,滴定后无气泡
d.实验Ⅱ中,对滤渣灼烧不充分
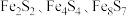 等)的酶和蛋白质,它们是存在于生物体的最古老的生命物质之一、为研究某铁硫簇结构
等)的酶和蛋白质,它们是存在于生物体的最古老的生命物质之一、为研究某铁硫簇结构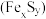 的组成,某化学兴趣小组设计了下列实验:
的组成,某化学兴趣小组设计了下列实验:实验Ⅰ:测定硫的质量



(1)实验过程中使用装置A制备氧气,
(2)检查装置的气密性后,在C中放入ag铁硫簇的样品(含有不溶于水和盐酸的杂质),在E中加入品红溶液,在D中加入
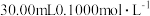 的酸性
的酸性 溶液。写出实验过程中仪器D中发生的离子反应方程式:
溶液。写出实验过程中仪器D中发生的离子反应方程式:(3)通入氧气并加热,发现C中固体逐渐转变为红棕色。待固体完全转化后,取D中的
 溶液15.00mL,用0.1000mol/L碘化钾溶液进行滴定。记录数据如下:
溶液15.00mL,用0.1000mol/L碘化钾溶液进行滴定。记录数据如下:| 滴定次数 | 待测溶液体积/mL | 消耗KI溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第1次 | 3.00 | 1.00 | 7.50 |
| 第2次 | 3.00 | 1.02 | 6.03 |
| 第3次 | 3.00 | 1.00 | 5.99 |
②滴定过程中发生的离子反应为
③计算ag铁硫簇的样品中含有S的物质的量为
实验Ⅱ:测定铁的质量
(4)取实验Ⅰ硬质玻璃管C中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经灼烧得0.32g固体。通过计算,可以得出该铁硫簇的化学式为
实验Ⅲ:问题研讨
(5)①有同学提出,撤去E装置,对实验没有影响,你的看法是
②下列操作,可能引起x∶y偏大的是
a.滴定剩余
 溶液时,KI溶液滴到锥形瓶外边一滴
溶液时,KI溶液滴到锥形瓶外边一滴b.配制标准KI溶液时,定容时俯视刻度线
c.用碘化钾溶液滴定剩余
 溶液时,滴定前有气泡,滴定后无气泡
溶液时,滴定前有气泡,滴定后无气泡d.实验Ⅱ中,对滤渣灼烧不充分
您最近一年使用:0次



