以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法正确的是
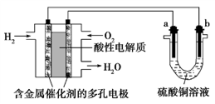
| A.燃料电池工作时,正极反应为O2+2H2O+4e-===4OH- |
| B.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| C.电解过程中SO42— 移向b极 |
| D.a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
更新时间:2018-05-04 15:27:14
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将镁片和铁片用导线连接置于同一稀盐酸溶液中,经过一段时间后,下列叙述正确的是
| A.正极附近Cl-的浓度逐渐增大 |
| B.溶液中Cl-的浓度总体上基本不变 |
| C.负极上有Cl2逸出,正极上有H2逸出 |
| D.溶液的pH在电池工作过程中基本不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用生物燃料电池原理研究室温下氨的合成,电池工作时 在电极与酶之间传递电子,示意图如下所示。下列说法
在电极与酶之间传递电子,示意图如下所示。下列说法不正确 的是

 在电极与酶之间传递电子,示意图如下所示。下列说法
在电极与酶之间传递电子,示意图如下所示。下列说法
A.正极电极反应式为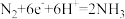 |
B.负极区,在氢化酶作用下发生反应 |
| C.电池工作时质子通过交换膜由负极区向正极区移动 |
| D.相比现有工业合成氨,该方法条件温和,同时还可提供电能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】为防止因天然气泄漏,居家安装天然气报警器很重要。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警,图1是成品装置,其工作原理如图2所示,其中 可以在固体电解质
可以在固体电解质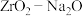 中移动。当报警器触发工作时,下列说法正确的是
中移动。当报警器触发工作时,下列说法正确的是

 可以在固体电解质
可以在固体电解质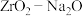 中移动。当报警器触发工作时,下列说法正确的是
中移动。当报警器触发工作时,下列说法正确的是
| A.图2中的多孔电极b上发生氧化反应 |
B. 在电解质中向a电极移动,电流方向由a电极经导线向b电极 在电解质中向a电极移动,电流方向由a电极经导线向b电极 |
| C.当电路中有0.008mol电子转移时,则电极a有22.4mL甲烷参与反应 |
D.多孔电极a极上发生的反应的电极反应式为: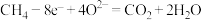 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下图装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池。装置(Ⅰ)的离子交换膜只允许Na+通过,已知电池充、放电的化学方程式为2Na2S2+NaBr3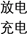 Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
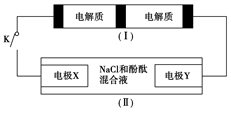
 Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
| A.闭合开关K时,Na+从右到左通过离子交换膜 |
| B.闭合开关K时,负极反应式为3NaBr-2e-===NaBr3+2Na+ |
| C.闭合开关K时,当有0.1 mol Na+通过离子交换膜时,X电极上放出标准状况下气体1.12 L |
| D.闭合开关K时,X电极反应式为2Cl--2e-===Cl2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】电浮选凝聚法是工业上采用的一种污水处理方法,某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法正确的是
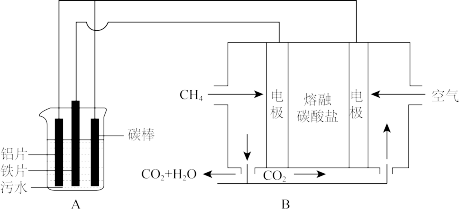

| A.装置A中碳棒为阴极 |
| B.装置B中通入空气的电极反应是O2+2H2O+4e-═4OH- |
| C.污水中加入适量的硫酸钠,既可增强溶液的导电性,又可增强凝聚净化的效果 |
| D.标准状况下,若A装置中产生44.8L气体,则理论上B装置中要消耗CH4 11.2L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】LiOH和钴氧化物可用于制备锂离子电池正极材料。利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。下列说法不正确的是()


| A.B极区电解液为LiOH溶液 |
| B.电解过程中Li+向B电极迁移 |
| C.每产生标准状况下2.24L氢气,就有0.1mol阳离子通过交换膜进入阴极区 |
| D.阳极电极反应式为2Cl-- 2e-=Cl2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】该科研小组探究用磷酸铁锂电池处理含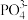 的酸性废水,以得到有用的FePO4,其装置如图所示,下列说法正确的是
的酸性废水,以得到有用的FePO4,其装置如图所示,下列说法正确的是
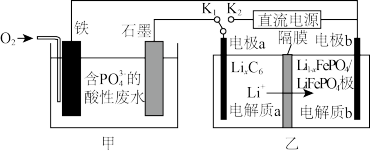
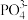 的酸性废水,以得到有用的FePO4,其装置如图所示,下列说法正确的是
的酸性废水,以得到有用的FePO4,其装置如图所示,下列说法正确的是
A.连接K1甲池中铁电极附近总反应为4Fe2++O2+4H++4PO =4FePO4↓+2H2O =4FePO4↓+2H2O |
| B.乙池中电解质a可以用Li2SO4水溶液 |
| C.连接K1,甲池中石墨为阳极,发生氧化反应 |
| D.连接K2给乙池充电,电极b的电极反应式为LiFePO4+xe-=Li1-xFePO4+xLi+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】世界某著名学术刊物介绍了一种新型中温全瓷铁-空气电池,其结构如图所示。下列有关该电池放电时的说法正确的是
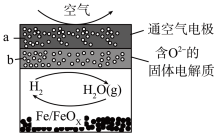

| A.a极为原电池的负极 |
| B.正极的电极反应为O2+4e-+2H2O=4OH- |
| C.铁表面发生的反应为xH2O(g)+Fe=FeOx+xH2 |
| D.若有22.4L(标准状况)空气参与反应,则电路中有4mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是
 3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是A.放电时负极反应为:Zn−2e−+2OH﹣ Zn(OH)2 Zn(OH)2 |
B.充电时阳极反应:F e(OH)3-3e−+5OH−   +4H2O +4H2O |
| C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D.该电池放电后,溶液的碱性增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】高效能电池的研发制约着电动汽车的推广。有一种新型燃料电池,它以多孔镍板为电极并将其插入KOH溶液中然后分别向两极通入乙烷(C2H6)和氧气,其总反应为2C2H6+7O2+8KOH=4K2CO3+10H2O,下列有关此电池的推断不正确的是
| A.正极的电极反应式为2H2O+O2+4e-=4OH- |
| B.放电过程中KOH的物质的量浓度减小 |
| C.每消耗1 mol C2H6,则外电路上转移的电子为14 mol |
| D.放电一段时间后,负极周围的pH升高 |
您最近一年使用:0次

 的废水。如下图所示;电解过程中溶液发生反应:
的废水。如下图所示;电解过程中溶液发生反应:
 的数目不变
的数目不变
 +4H2O
+4H2O

