已知两个羟基同时连在同一碳原子上的结构是不稳定的,它要发生脱水反应:
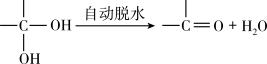
现有分子式为C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生上述一系列反应
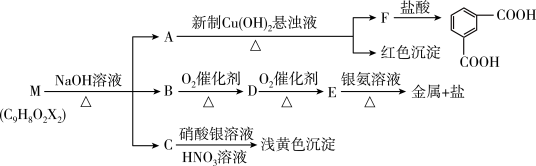
试回答下列问题:
(1)X为____________________ (填元素符号);
(2)上述转化中其中属于氧化反应的共有_______ 步(填数字);M与NaOH溶液共热反应的所属类型是_______________ 反应。
(3)M的结构简式为________________________________
(4)写出下列反应的化学方程:
E和银氨溶液反应的化学方程式:_______________________________________________

现有分子式为C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生上述一系列反应

试回答下列问题:
(1)X为
(2)上述转化中其中属于氧化反应的共有
(3)M的结构简式为
(4)写出下列反应的化学方程:
E和银氨溶液反应的化学方程式:
更新时间:2018-05-21 17:29:16
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】已知(X代表卤素原子,R代表烃基)

利用上述信息,按以下步骤从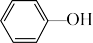 合成
合成 。 (部分试剂和反应条件已略去)
。 (部分试剂和反应条件已略去)
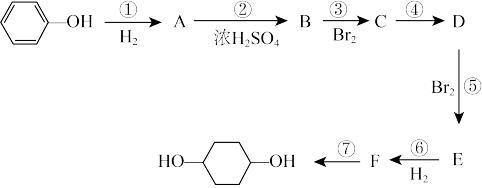
请回答下列问题:
(1)分别写出下列物质的结构简式:B______ ,D_______ ,E______ ;
(2)反应①~⑦中,属于消去反应的是____ (填反应数字代号,下同),属于加成反应的是____ ,属于取代反应的是____ ;
(3)反应④的条件为_____ ,反应⑦的条件为_____ ;
(4)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为_____ 。

利用上述信息,按以下步骤从
 合成
合成 。 (部分试剂和反应条件已略去)
。 (部分试剂和反应条件已略去)
请回答下列问题:
(1)分别写出下列物质的结构简式:B
(2)反应①~⑦中,属于消去反应的是
(3)反应④的条件为
(4)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】图中A~J均为有机化合物,根据图中的信息,回答下列问题。
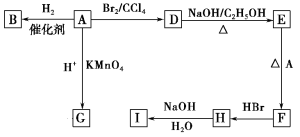
已知:分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生反应: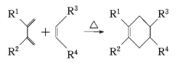
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.2%。B的一氯代物仅有一种,B的结构简式为_______________________ 。
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则M的结构简式为__________________________________ 。
(3)由E和A反应生成F的化学方程式为___________________________________ 。
(4)D中含有的官能团是________ ,由H生成I的反应类型是______________
(5)已知:R-COOH+NaOH→R-COONa+H2O,G的分子式为C6H10O4,0.146gG需用20mL0.100mol·L-1 NaOH溶液完全中和,G的结构简式为______________________ ;
(6)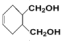 为重要的化工原料,根据题中信息,设计以1,3-丁二烯为原料合成
为重要的化工原料,根据题中信息,设计以1,3-丁二烯为原料合成 的合成路线
的合成路线_____________________________ (以流程图形式表示,无机试剂任选)。

已知:分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生反应:

(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.2%。B的一氯代物仅有一种,B的结构简式为
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则M的结构简式为
(3)由E和A反应生成F的化学方程式为
(4)D中含有的官能团是
(5)已知:R-COOH+NaOH→R-COONa+H2O,G的分子式为C6H10O4,0.146gG需用20mL0.100mol·L-1 NaOH溶液完全中和,G的结构简式为
(6)
 为重要的化工原料,根据题中信息,设计以1,3-丁二烯为原料合成
为重要的化工原料,根据题中信息,设计以1,3-丁二烯为原料合成 的合成路线
的合成路线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
名校
【推荐1】某兴趣小组设计实验探究 ,催化空气氧化
,催化空气氧化 的效率。回答下列问题:
的效率。回答下列问题:
步骤Ⅰ 制备
在通风橱中用下图装置制备 (加热及夹持装置省略),反应方程式:
(加热及夹持装置省略),反应方程式: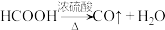

(1)装置A中盛放甲酸的仪器的名称是_______ 。
(2)从B、C、D中选择合适的装置收集 ,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。
,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。______
步骤Ⅱ 检验
将 通入新制银氨溶液中,有黑色沉淀生成。
通入新制银氨溶液中,有黑色沉淀生成。
(3)该反应的化学方程式为_______ 。
步骤Ⅲ 探究 催化空气氧化
催化空气氧化 的效率
的效率
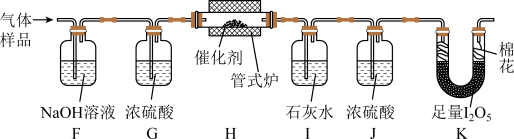
将一定量 与空气混合,得到
与空气混合,得到 体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至
体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至 ,按一定流速通入气体样品。(已知:
,按一定流速通入气体样品。(已知: 是白色固体,易吸水潮解:
是白色固体,易吸水潮解: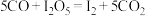 )
)
(4)通入 (已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了
(已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了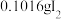 。
。
①能证明 被空气氧化的现象是
被空气氧化的现象是_______ ;
② 被催化氧化的百分率为
被催化氧化的百分率为_______ ;
③若未通入氮气,②的结果将_______ (填“偏大”“偏小”或“无影响”)。
(5)探究气体与催化剂接触时长对催化氧化效率的影响时,采用_______ 方法可以缩短接触时长。
(6)步骤Ⅲ装置存在的不足之处是_______ 。
 ,催化空气氧化
,催化空气氧化 的效率。回答下列问题:
的效率。回答下列问题:步骤Ⅰ 制备

在通风橱中用下图装置制备
 (加热及夹持装置省略),反应方程式:
(加热及夹持装置省略),反应方程式: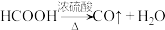

(1)装置A中盛放甲酸的仪器的名称是
(2)从B、C、D中选择合适的装置收集
 ,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。
,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。步骤Ⅱ 检验

将
 通入新制银氨溶液中,有黑色沉淀生成。
通入新制银氨溶液中,有黑色沉淀生成。(3)该反应的化学方程式为
步骤Ⅲ 探究
 催化空气氧化
催化空气氧化 的效率
的效率将一定量
 与空气混合,得到
与空气混合,得到 体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至
体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至 ,按一定流速通入气体样品。(已知:
,按一定流速通入气体样品。(已知: 是白色固体,易吸水潮解:
是白色固体,易吸水潮解: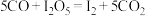 )
)
(4)通入
 (已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了
(已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了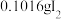 。
。①能证明
 被空气氧化的现象是
被空气氧化的现象是②
 被催化氧化的百分率为
被催化氧化的百分率为③若未通入氮气,②的结果将
(5)探究气体与催化剂接触时长对催化氧化效率的影响时,采用
(6)步骤Ⅲ装置存在的不足之处是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】连二亚硫酸钠( )也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
)也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
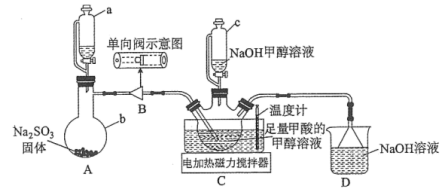
回答下列问题:
(1)仪器a的名称是___________ ,用装置A制备 时所选用的酸,你认为下列最适宜选用的是
时所选用的酸,你认为下列最适宜选用的是___________ (填字母)。
A.浓盐酸 B.质量分数为70%的
C.稀硝酸 D.质量分数为10%的稀硫酸
(2)单向阀的作用是___________ ,制备保险粉前先打开仪器a的活塞的目的是___________ 。
(3)已知三颈烧瓶中的甲酸转化为 ,写出生成
,写出生成 的化学方程式:
的化学方程式:___________ 。
(4) 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:___________ 。
(5) 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:___________ (写出实验操作、现象及结论)。
(6)称取粗产品 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应(
溶液恰好完全反应( ),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到
),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为___________ (含 、
、 的表达式)。
的表达式)。
 )也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
)也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
回答下列问题:
(1)仪器a的名称是
 时所选用的酸,你认为下列最适宜选用的是
时所选用的酸,你认为下列最适宜选用的是A.浓盐酸 B.质量分数为70%的

C.稀硝酸 D.质量分数为10%的稀硫酸
(2)单向阀的作用是
(3)已知三颈烧瓶中的甲酸转化为
 ,写出生成
,写出生成 的化学方程式:
的化学方程式:(4)
 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:(5)
 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:(6)称取粗产品
 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应(
溶液恰好完全反应( ),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到
),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为 、
、 的表达式)。
的表达式)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】物质M可用作调味剂、乳化剂、抗氧化增效剂、吸湿剂、pH调节剂、增香剂、缓冲剂。其结构式如图所示,其组成元素X、Y、Z、Q为原子序数依次增大的短周期主族元素,且Y的一种核素常用于检测文物的年代。
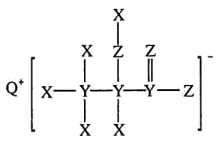
请回答下列问题:
(1)元素Q在周期表中的位置为_______ ,工业上采用_______ 法冶炼Q的单质。
(2)物质M中所含化学键的类型为_______ ,物质M与稀硫酸反应生成有机物N,N中所含官能团的名称为_______ 。
(3)相同条件下,等质量的Y的两种单质 、
、 分别在足量
分别在足量 中燃烧,放出热量前者大于后者。则两种单质中,
中燃烧,放出热量前者大于后者。则两种单质中,_______ (填“ ”或“
”或“ ”)更稳定。Y与Z分别形成的简单氢化物的沸点由高到低的顺序为
”)更稳定。Y与Z分别形成的简单氢化物的沸点由高到低的顺序为_______ (填化学式)。
(4)QX的电子式为_______ ,与水反应的化学方程式为_______ 。

请回答下列问题:
(1)元素Q在周期表中的位置为
(2)物质M中所含化学键的类型为
(3)相同条件下,等质量的Y的两种单质
 、
、 分别在足量
分别在足量 中燃烧,放出热量前者大于后者。则两种单质中,
中燃烧,放出热量前者大于后者。则两种单质中, ”或“
”或“ ”)更稳定。Y与Z分别形成的简单氢化物的沸点由高到低的顺序为
”)更稳定。Y与Z分别形成的简单氢化物的沸点由高到低的顺序为(4)QX的电子式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】乳酸亚铁晶体[CH3CH(OH)COO]2Fe·3H2O是一种很好的食品铁强化剂,吸收效果比无机铁好,可由乳酸与FeCO3反应制得,而乳酸可由聚乳酸(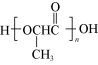 )得到。某化学兴趣小组利用化学解聚方法,先由废旧聚乳酸餐盒制得乳酸,再与碳酸亚铁反应可得乳酸亚铁晶体。已知:
)得到。某化学兴趣小组利用化学解聚方法,先由废旧聚乳酸餐盒制得乳酸,再与碳酸亚铁反应可得乳酸亚铁晶体。已知:
①乳酸亚铁晶体易溶于水,难溶于乙醇
②乳酸是淡黄色粘性液体,与乙醇、水混溶
I.废旧聚乳酸材料的解聚(装置如图1)
①分别取一定量的NaOH、无水乙醇和白色聚乳酸餐盒碎片,装入锥形瓶,加热解聚;
②待反应完毕,向锥形瓶中加入少量浓盐酸,然后加热浓缩,得到淡黄色粘稠状液体和少量白色不溶物;
③往②中所得混合物加入20mL无水乙醇并搅拌均匀,静置、过滤,弃去白色不溶物。
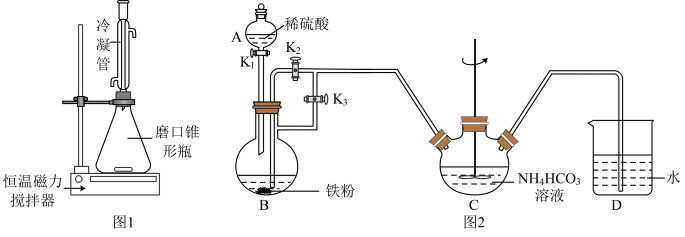
(1)步骤②中,加入浓盐酸的目的是_______ 。
(2)步骤③加入20mL无水乙醇的作用是_______ 。
II.碳酸亚铁的制备(装置如图2)实验步骤如下:
①检查气密性,按图示添加药品;
②在装置B中制取硫酸亚铁,并将整个装置内的空气排净;
③将B中溶液导入C中产生FeCO3沉淀;
④将C中混合物分离提纯,获得纯净的碳酸亚铁产品。
(1)装置D的作用是_______ 。
(2)装置C中生成FeCO3的离子方程式是_______  。
。
(3)步骤②中应打开的开关是_______ 。(选填“K2”或“K3”)
II.制备乳酸亚铁晶体
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。经系列操作后得到产品。
(1)欲获得尽可能多的产品,上述系列操作指的是:冷却,_______ ,过滤,再洗涤和干燥。
(2)乳酸亚铁晶体中铁元素含量
称取mg样品,灼烧完全灰化,加足量盐酸溶解,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用cmol·L-1硫代硫酸钠溶液滴定(已知:I2+2 =2I-+
=2I-+ ),滴定终点时,测得消耗标准溶液VmL。样品中铁元素的质量分数为
),滴定终点时,测得消耗标准溶液VmL。样品中铁元素的质量分数为_______ 。(用含有相关字母的代数式表示)。
 )得到。某化学兴趣小组利用化学解聚方法,先由废旧聚乳酸餐盒制得乳酸,再与碳酸亚铁反应可得乳酸亚铁晶体。已知:
)得到。某化学兴趣小组利用化学解聚方法,先由废旧聚乳酸餐盒制得乳酸,再与碳酸亚铁反应可得乳酸亚铁晶体。已知:①乳酸亚铁晶体易溶于水,难溶于乙醇
②乳酸是淡黄色粘性液体,与乙醇、水混溶
I.废旧聚乳酸材料的解聚(装置如图1)
①分别取一定量的NaOH、无水乙醇和白色聚乳酸餐盒碎片,装入锥形瓶,加热解聚;
②待反应完毕,向锥形瓶中加入少量浓盐酸,然后加热浓缩,得到淡黄色粘稠状液体和少量白色不溶物;
③往②中所得混合物加入20mL无水乙醇并搅拌均匀,静置、过滤,弃去白色不溶物。

(1)步骤②中,加入浓盐酸的目的是
(2)步骤③加入20mL无水乙醇的作用是
II.碳酸亚铁的制备(装置如图2)实验步骤如下:
①检查气密性,按图示添加药品;
②在装置B中制取硫酸亚铁,并将整个装置内的空气排净;
③将B中溶液导入C中产生FeCO3沉淀;
④将C中混合物分离提纯,获得纯净的碳酸亚铁产品。
(1)装置D的作用是
(2)装置C中生成FeCO3的离子方程式是
 。
。(3)步骤②中应打开的开关是
II.制备乳酸亚铁晶体
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。经系列操作后得到产品。
(1)欲获得尽可能多的产品,上述系列操作指的是:冷却,
(2)乳酸亚铁晶体中铁元素含量
称取mg样品,灼烧完全灰化,加足量盐酸溶解,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用cmol·L-1硫代硫酸钠溶液滴定(已知:I2+2
 =2I-+
=2I-+ ),滴定终点时,测得消耗标准溶液VmL。样品中铁元素的质量分数为
),滴定终点时,测得消耗标准溶液VmL。样品中铁元素的质量分数为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】有机物J是合成抗炎药洛索洛芬钠的关键中间体,它的一种合成路线如图:
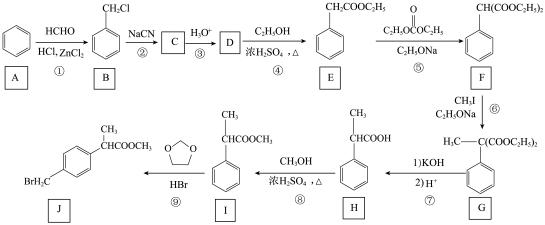
回答下列问题:
(1)反应④的反应类型是______ ;J中官能团名称是______ 。
(2)不用甲苯与氯气在光照条件下反应得到B物质的原因是______ 。
(3)根据流程中的信息,在反应⑥的条件下,CH2(COOC2H5)2与足量CH3CH2CH2I充分反应生成的有机产物结构简式为______ 。
(4)反应⑨的化学方程式为:
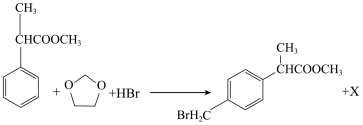
其中产物X的结构简式是______ 。
(5)写出符合下列条件的I的同分异构体______ 。
①能发生银镜反应,但不能发生水解反应;②苯环上一氯取代物只有一种;③核磁共振氢谱有4组峰。
(6)根据流程中的信息,写出以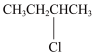 、CH3OH为有机原料合成
、CH3OH为有机原料合成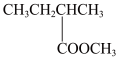 的合成路线。
的合成路线。_______

回答下列问题:
(1)反应④的反应类型是
(2)不用甲苯与氯气在光照条件下反应得到B物质的原因是
(3)根据流程中的信息,在反应⑥的条件下,CH2(COOC2H5)2与足量CH3CH2CH2I充分反应生成的有机产物结构简式为
(4)反应⑨的化学方程式为:

其中产物X的结构简式是
(5)写出符合下列条件的I的同分异构体
①能发生银镜反应,但不能发生水解反应;②苯环上一氯取代物只有一种;③核磁共振氢谱有4组峰。
(6)根据流程中的信息,写出以
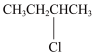 、CH3OH为有机原料合成
、CH3OH为有机原料合成 的合成路线。
的合成路线。
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】早在2000多年前,人们发现柳树皮中含有一种具有解热镇痛功效的物质—水杨酸,此后科学家对水杨酸的结构进行一系列改造,合成出疗效更佳的长效缓释阿司匹林,其开发过程蕴含着重要的思想方法,请回答下列问题:
 (柳树皮) →
(柳树皮) →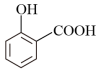 (水杨酸) →
(水杨酸) →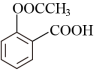 (阿司匹林) →
(阿司匹林) →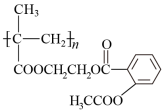 (长效缓释阿司匹林)
(长效缓释阿司匹林)
(1)水杨酸的结构与性质
①水杨酸中含氧官能团的名称是____________ 、______________ 。
②下列关于水杨酸的说法正确的是__________ 。
A.分子式为C7H7O3
B.1 mol水杨酸能与2 molNaOH反应
C.可发生加成、取代、消去反应
(2)水杨酸的合成
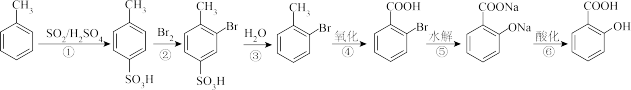
①由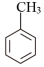 制
制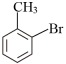 ,不采取甲苯直接与Br2直接反应,而是经过步骤①~③,目的是
,不采取甲苯直接与Br2直接反应,而是经过步骤①~③,目的是_______________
②步骤④~⑥的顺序能够改为水解、酸化、氧化?____________ (填“能”或“不能”),理由是__________________________________
(3)水杨酸具有解热镇痛的功效,但是其酸性很强,对人的肠胃有刺激性,容易引发胃溃疡,1897年德国化学家菲利克斯·霍夫曼对水杨酸的结构进行改造合成出阿司匹林。
①水杨酸的酸性主要来源于-COOH,将-OH转化为-OOCCH3,可使-COOH的酸性大大降低。科学家的这一设计思路依据的原理是_________________________________________
②水杨酸到阿司匹林的反应类型是_________
(4)1982年拜尔公司将阿司匹林与聚甲基丙烯酸借助乙二醇嫁接起来,研制出长效缓释阿司匹林,可减少每天吃药次数,大大方便了人们对药物的使用。
①长效缓释阿司匹林在人体内释放出阿司匹林的反应类型是______________
②写出乙烯经2步合成乙二醇的化学方程式_______________________ 、________________
 (柳树皮) →
(柳树皮) → (水杨酸) →
(水杨酸) → (阿司匹林) →
(阿司匹林) → (长效缓释阿司匹林)
(长效缓释阿司匹林)(1)水杨酸的结构与性质
①水杨酸中含氧官能团的名称是
②下列关于水杨酸的说法正确的是
A.分子式为C7H7O3
B.1 mol水杨酸能与2 molNaOH反应
C.可发生加成、取代、消去反应
(2)水杨酸的合成

①由
 制
制 ,不采取甲苯直接与Br2直接反应,而是经过步骤①~③,目的是
,不采取甲苯直接与Br2直接反应,而是经过步骤①~③,目的是②步骤④~⑥的顺序能够改为水解、酸化、氧化?
(3)水杨酸具有解热镇痛的功效,但是其酸性很强,对人的肠胃有刺激性,容易引发胃溃疡,1897年德国化学家菲利克斯·霍夫曼对水杨酸的结构进行改造合成出阿司匹林。
①水杨酸的酸性主要来源于-COOH,将-OH转化为-OOCCH3,可使-COOH的酸性大大降低。科学家的这一设计思路依据的原理是
②水杨酸到阿司匹林的反应类型是
(4)1982年拜尔公司将阿司匹林与聚甲基丙烯酸借助乙二醇嫁接起来,研制出长效缓释阿司匹林,可减少每天吃药次数,大大方便了人们对药物的使用。
①长效缓释阿司匹林在人体内释放出阿司匹林的反应类型是
②写出乙烯经2步合成乙二醇的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】有机化学反应因反应条件不同,可生成不同的有机产品。
例如: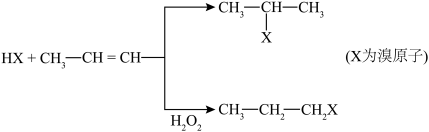
工业上利用上述信息,按下列路线合成结构简式为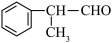 的物质,该物质是一种香料。
的物质,该物质是一种香料。
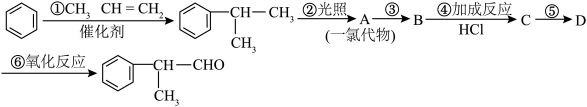
请根据上述路线,回答下列问题:
(1)A的结构简式可能为_________________ 。
(2)反应①的反应类型___________________ 。
(3)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是___________ ;
(4)这种香料具有多种同分异构体,其中某些物质有下列特征:①属于酚类②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写1种):____________ 。
例如:

工业上利用上述信息,按下列路线合成结构简式为
 的物质,该物质是一种香料。
的物质,该物质是一种香料。
请根据上述路线,回答下列问题:
(1)A的结构简式可能为
(2)反应①的反应类型
(3)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是
(4)这种香料具有多种同分异构体,其中某些物质有下列特征:①属于酚类②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写1种):
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】布洛芬具有降温和抑制肺部炎症的双重作用。一种制备布洛芬的合成路线如下:

已知:
①CH3CH2Cl CH3CH2MgCl
CH3CH2MgCl
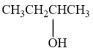
②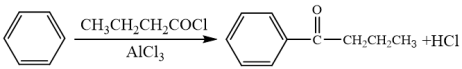
回答下列问题:
(1)A的化学名称为_______ 。
(2)E→F的反应类型为_______ ,H中官能团的名称为_______ 。
(3)E的分子中含有两个甲基,则E的结构简式为_______ 。
(4)I→K的化学方程式为_______ 。
(5)写出符合下列条件的D的同分异构体的结构简式_______ (不考虑立体异构)。
①能与FeCl3溶液发生显色反应;②分子中有一个手性碳原子;③苯环上有处于间位的2个取代基。
(6)写出以间二甲苯、CH3COCl和(CH3)2CHMgCl为原料制备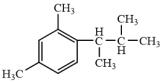 的合成路线
的合成路线_______ 。(无机试剂任选)

已知:
①CH3CH2Cl
 CH3CH2MgCl
CH3CH2MgCl
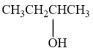
②

回答下列问题:
(1)A的化学名称为
(2)E→F的反应类型为
(3)E的分子中含有两个甲基,则E的结构简式为
(4)I→K的化学方程式为
(5)写出符合下列条件的D的同分异构体的结构简式
①能与FeCl3溶液发生显色反应;②分子中有一个手性碳原子;③苯环上有处于间位的2个取代基。
(6)写出以间二甲苯、CH3COCl和(CH3)2CHMgCl为原料制备
 的合成路线
的合成路线
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
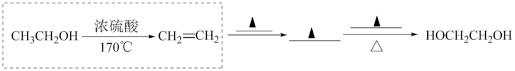
【推荐3】葡萄糖在酒化酶的催化下可以转变为乙醇,以乙醇为有机原料可以设计出如下转化路线流程图,其中 是高分子化合物。
是高分子化合物。

已知:RCHO+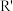 CH2CHO
CH2CHO
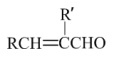 +H2O(
+H2O( 、
、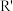 代表
代表 或烃基)
或烃基)
(1)乙烯 的反应类型为
的反应类型为___________ 。
(2) 的分子式为
的分子式为 ,写出其结构简式:
,写出其结构简式:___________ 。
(3) 的一种同系物分子式为
的一种同系物分子式为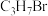 ,
,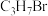 的同分异构体共有
的同分异构体共有___________ 种。
(4)手性碳原子是指与四个各不相同的原子或基团相连的碳原子,可用“*”标出,如图-1中含有1个手性碳原子。葡萄糖的结构简式如图-2所示。

①在如图-2中用“*”标出所有手性碳原子___________ 。
②向新制 中加入适量葡萄糖溶液,加热,可观察到的实验现象为
中加入适量葡萄糖溶液,加热,可观察到的实验现象为___________ 。
(5)仿照如下虚线方框示例,补充完整以乙醇为有机原料制备乙二醇的合成路线流程图___________ (无机试剂和有机溶剂任用,有机物用结构简式表示):
 是高分子化合物。
是高分子化合物。
已知:RCHO+
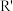 CH2CHO
CH2CHO
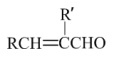 +H2O(
+H2O( 、
、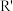 代表
代表 或烃基)
或烃基)(1)乙烯
 的反应类型为
的反应类型为(2)
 的分子式为
的分子式为 ,写出其结构简式:
,写出其结构简式:(3)
 的一种同系物分子式为
的一种同系物分子式为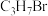 ,
,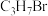 的同分异构体共有
的同分异构体共有(4)手性碳原子是指与四个各不相同的原子或基团相连的碳原子,可用“*”标出,如图-1中含有1个手性碳原子。葡萄糖的结构简式如图-2所示。

①在如图-2中用“*”标出所有手性碳原子
②向新制
 中加入适量葡萄糖溶液,加热,可观察到的实验现象为
中加入适量葡萄糖溶液,加热,可观察到的实验现象为(5)仿照如下虚线方框示例,补充完整以乙醇为有机原料制备乙二醇的合成路线流程图

您最近一年使用:0次

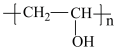 ,某同学设计其合成路线如下:
,某同学设计其合成路线如下: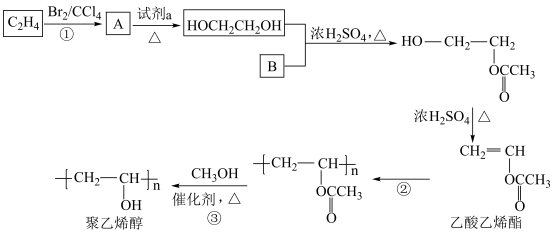
 溶液反应放出气体的有(不考虑立体异构):
溶液反应放出气体的有(不考虑立体异构):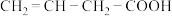 、
、

