下列判断错误的是( )
| A.Na2O2——有离子键和共价键 | B.HCl气体溶于水——共价键被破坏 |
| C.NaCl晶体溶于水——离子键被破坏 | D.氢氧化钠熔化——离子键和共价键均被破坏 |
更新时间:2018-05-21 17:49:22
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列原子间可形成离子键的是
| A.H和Cl | B.Na和F | C.Si和C | D.P和O |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列观点正确的是
| A.H2O2中只存在极性键 |
| B.在氧化钠中,只存在氧离子和钠离子的静电吸引作用 |
| C.某化合物熔融态能导电,该化合物中一定有离子键 |
| D.Na2O和Na2O2所含化学键类型完全相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列叙述中正确的是
| A.共价化合物中只含有共价键,离子化合物中只含有离子键 |
| B.在过渡元素中找优良催化剂和耐高温、耐腐蚀的合金材料 |
| C.只要有化学键的断裂或化学键的形成,就一定发生了化学反应 |
| D.元素周期律的实质是原子序数的周期性变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法不正确 的是
A.用电子式表示K2S的形成过程为: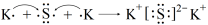 |
| B.MgCl2和NaOH中的化学键类型完全相同,都属于离子化合物 |
| C.CO2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 |
| D.反应2H2O+2F2=O2+4HF,同时有极性键和非极性键的断裂和形成 |
您最近一年使用:0次



