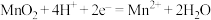人工光合系统装置(如图)可实现以CO2和H2O合成CH4。下列说法不正确的是( )
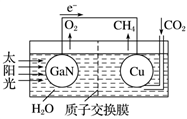

| A.该装置为原电池,且铜为负极 |
| B.电池工作时,H+向Cu电极移动 |
| C.GaN电极表面的电极反应式为2H2O-4e-===O2+4H+ |
D.反应CO2+2H2O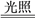 CH4+2O2中每消耗1 mol CO2转移4 mol e- CH4+2O2中每消耗1 mol CO2转移4 mol e- |
更新时间:2017-06-26 21:39:49
|
相似题推荐
多选题
|
较难
(0.4)
名校
【推荐1】在缺氧的深层潮湿土壤中,厌氧细菌会促进钢铁发生厌氧腐蚀,其原理如图所示。为抑制腐蚀的发生,通常将钢管、石墨电极分别与外接电源相连,使钢管表面形成致密的Fe3O4薄膜。下列说法不正确的是
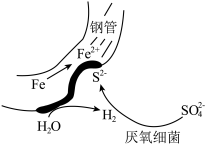

| A.上述保护方法为阴极电保护法 |
B.腐蚀过程中存在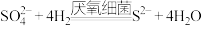 |
C.每生成1molFeS,电路中转移的电子数为 |
| D.通电后电子从钢管流向石墨电极,再经潮湿的土壤回到钢管 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】某测定O2含量的传感器工作原理如图所示。O2通过聚四氟乙烯膜进入传感器只与AlI3反应生成Al2O3和I2,RbAg4I5固体只传导Ag+,E为电位计。下列说法错误的是
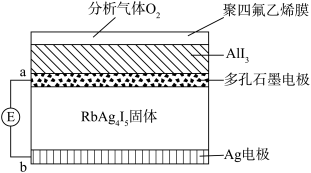

| A.电子由a极移动到b极 |
| B.RbAg4I5质量不发生变化 |
| C.b极的电极反应式为:Ag+I--e-=AgI |
| D.该传感器协同总反应方程式为:3O2+4AlI3+12Ag=2Al2O3+12AgI |
您最近一年使用:0次
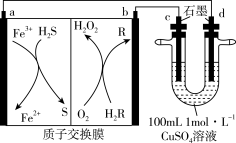
【推荐1】我国科学家研制一种新型化学电池成功实现废气的处理和能源的利用,用该新型电池电解 溶液,装置如图
溶液,装置如图 和R都是有机物
和R都是有机物 。下列说法正确的是
。下列说法正确的是
 溶液,装置如图
溶液,装置如图 和R都是有机物
和R都是有机物 。下列说法正确的是
。下列说法正确的是
A.原电池正极区,发生反应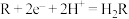 、 、 |
| B.原电池工作一段时间后,负极区的pH变大 |
| C.用该装置在铜上镀银,电极d为纯银 |
D.若消耗标准状况下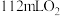 ,则电解后恢复至常温 ,则电解后恢复至常温 溶液的pH约为1 溶液的pH约为1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液。电池中发生的反应为2VCl2+BrCl2-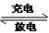 2VCl3+Br-。
2VCl3+Br-。
下列说法正确的是
 2VCl3+Br-。
2VCl3+Br-。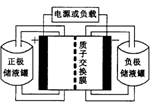
下列说法正确的是
| A.VCl2存储在正极储液罐内 |
| B.放电时H+从负极区移至正极区 |
| C.充电时电池的负极与电源的正极相连 |
| D.充电时阳极反应为Br-+2Cl--2e-=BrCl2- |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
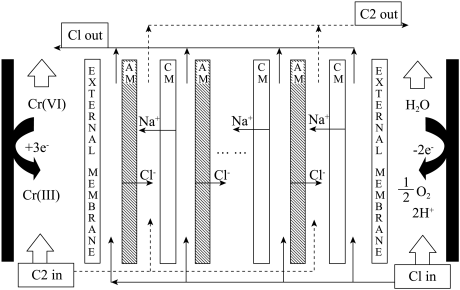
【推荐3】某课题组利用盐度梯度和氧化还原工艺成功设计了如图所示的电池装置,将酸性废水中存在的高毒性 转化为
转化为 后再经后续处理转化为
后再经后续处理转化为 离开溶液。设装置内温度恒定为
离开溶液。设装置内温度恒定为 。
。
已知:对于电池正极反应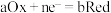 有
有 方程
方程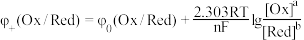
注:(1) 下,
下,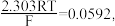 n为转移电子数;电势越高反应的趋势越大;
n为转移电子数;电势越高反应的趋势越大;
(2)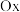 为氧化态物质,
为氧化态物质, 为还原态物质,
为还原态物质,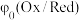 为定值;
为定值;
(3)对于除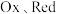 外还有其他如
外还有其他如 等参加反应的物质,它们的浓度的幂次方也要代入方程。
等参加反应的物质,它们的浓度的幂次方也要代入方程。
(参考数据: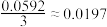 )
)
下列说法错误的是
 转化为
转化为 后再经后续处理转化为
后再经后续处理转化为 离开溶液。设装置内温度恒定为
离开溶液。设装置内温度恒定为 。
。
已知:对于电池正极反应
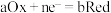 有
有 方程
方程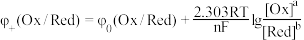
注:(1)
 下,
下,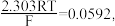 n为转移电子数;电势越高反应的趋势越大;
n为转移电子数;电势越高反应的趋势越大;(2)
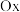 为氧化态物质,
为氧化态物质, 为还原态物质,
为还原态物质,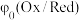 为定值;
为定值;(3)对于除
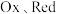 外还有其他如
外还有其他如 等参加反应的物质,它们的浓度的幂次方也要代入方程。
等参加反应的物质,它们的浓度的幂次方也要代入方程。(参考数据:
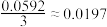 )
)下列说法错误的是
A.该电池利用溶液盐度梯度产生电势,“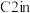 ”表示低浓度盐溶液 ”表示低浓度盐溶液 |
B.负极产生标准状况下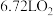 ,理论上转化 ,理论上转化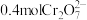 |
C.若要升高正极电势,可向正极区中加入 固体或升高正极区 固体或升高正极区 |
D.若正极区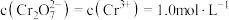 恒定,当正极区 恒定,当正极区 由1.0降低为0.5时,正极电势升高约 由1.0降低为0.5时,正极电势升高约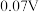 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】含氯苯的废水可通过加入适量乙酸钠,设计成微生物电池将氯苯转化为苯而除去,其原理如图所示。下列叙述正确的是
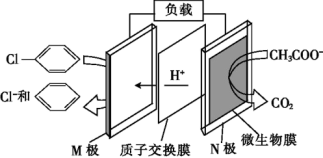

| A.氯苯被氧化生成苯 |
| B.N极为电池的负极 |
| C.M极的电极反应式为C6H5Cl+e-=C6H6+Cl- |
| D.每生成1molCO2,由N极区进入M极区的H+为4mol |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】金属锂燃料电池是一种新型电池,比锂离子电池具有更高的能量密度。它无电时也无需充电,只需更换其中的某些材料即可,其工作示意图如图,下列说法正确的是
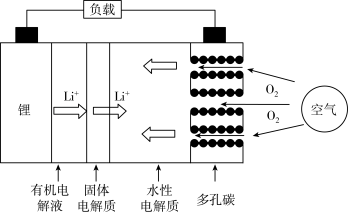

| A.放电时,通入空气的一极为负极 |
| B.放电时,电池反应为4Li+O2+2H2O=4LiOH |
| C.有机电解液可以是乙醇等无水有机物 |
| D.在更换锂电极的同时,要更换水性电解液 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示,下列说法正确的是
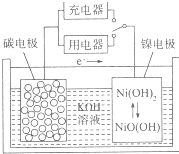

| A.放电时,正极质量增加 |
| B.充电时,溶液中OH﹣移向碳电极 |
| C.充电时,将电池的碳电极与外电源的负极相连 |
| D.放电时,电路中每转移2mol电子,碳电极上有1molH2被还原 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】为了探究镁铝在NaOH溶液中的放电情况,某研究小组设计了如图1所示的实验装置。反应过程中装置的电压变化如图2所示。下列说法正确的是
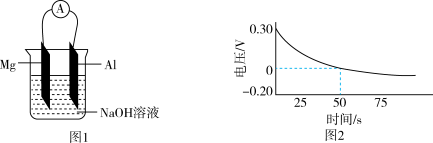

| A.镁电极始终为电池的负极 |
| B.50s后,原电池中电子流动方向发生改变 |
| C.判断原电池的正、负极既要依据金属活动性顺序,又要考虑与电解质溶液有关 |
| D.整个过程中正极的电极反应式均为:2H2O−2e−=H2↑+OH− |
您最近一年使用:0次

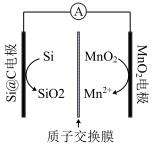
 会经质子交换膜由Si@C电极区移向
会经质子交换膜由Si@C电极区移向 电极区
电极区