某研究小组对铁生锈过行研究。

(1)甲同学设计了A、B、C组实验(如上图),探究铁生锈的条件。经过较长时间后,甲同学观察到的现象是:A中铁钉生锈;B中铁打不生锈;C中铁钉不生锈。
①通过上述实验现象分析,可得出铁生锈的外部条件是____________ ;
②铁钉发生电化学腐蚀的正极电极反应式为_____________ ;
③实验B所用的水要经过____ 处理;植物油的作用是____________ ;
④实验C中碱石灰的作用是___________ 。
(2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的表面升高,其原因是_________________ 。


(1)甲同学设计了A、B、C组实验(如上图),探究铁生锈的条件。经过较长时间后,甲同学观察到的现象是:A中铁钉生锈;B中铁打不生锈;C中铁钉不生锈。
①通过上述实验现象分析,可得出铁生锈的外部条件是
②铁钉发生电化学腐蚀的正极电极反应式为
③实验B所用的水要经过
④实验C中碱石灰的作用是
(2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的表面升高,其原因是

更新时间:2018-07-08 17:42:22
|
相似题推荐
【推荐1】天然气是一种清洁能源,但其中大多含有 、
、 等酸性气体和水汽,会腐蚀管道设备。已知:
等酸性气体和水汽,会腐蚀管道设备。已知: 时氢硫酸和碳酸的电离常数如下表:
时氢硫酸和碳酸的电离常数如下表:
(1)碳钢材质管道发生电化学腐蚀,作负极的物质是_______ 。
(2)用化学用语表示 溶液显酸性的原因
溶液显酸性的原因_______ 。
(3) 溶液可以去除
溶液可以去除 ,写出反应的离子方程式
,写出反应的离子方程式_______ 。
(4)用热碱液( 溶液)吸收天然气中的
溶液)吸收天然气中的 ,可将其转化为可溶性的
,可将其转化为可溶性的 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(5)我国科学家设计了一种 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,装置如下图所示。其中电极分别为
的高效去除,装置如下图所示。其中电极分别为 石墨烯(石墨烯包裹的
石墨烯(石墨烯包裹的 )和石墨烯。
)和石墨烯。

① 石墨烯是
石墨烯是_______ 极(填“阳”或“阴”)。
②石墨烯电极区发生反应为:
ⅰ.
ⅱ._______ 。
③ 协同转化总反应的化学方程式为
协同转化总反应的化学方程式为_______ , 在其中所起的作用是
在其中所起的作用是_______ 。
④工作时, 石墨烯电极区的
石墨烯电极区的 基本保持不变,结合化学用语解释原因
基本保持不变,结合化学用语解释原因_______ 。
 、
、 等酸性气体和水汽,会腐蚀管道设备。已知:
等酸性气体和水汽,会腐蚀管道设备。已知: 时氢硫酸和碳酸的电离常数如下表:
时氢硫酸和碳酸的电离常数如下表: | 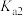 | |
 | 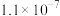 | 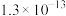 |
 | 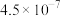 | 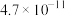 |
(1)碳钢材质管道发生电化学腐蚀,作负极的物质是
(2)用化学用语表示
 溶液显酸性的原因
溶液显酸性的原因(3)
 溶液可以去除
溶液可以去除 ,写出反应的离子方程式
,写出反应的离子方程式(4)用热碱液(
 溶液)吸收天然气中的
溶液)吸收天然气中的 ,可将其转化为可溶性的
,可将其转化为可溶性的 ,反应的化学方程式为
,反应的化学方程式为(5)我国科学家设计了一种
 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,装置如下图所示。其中电极分别为
的高效去除,装置如下图所示。其中电极分别为 石墨烯(石墨烯包裹的
石墨烯(石墨烯包裹的 )和石墨烯。
)和石墨烯。
①
 石墨烯是
石墨烯是②石墨烯电极区发生反应为:
ⅰ.

ⅱ.
③
 协同转化总反应的化学方程式为
协同转化总反应的化学方程式为 在其中所起的作用是
在其中所起的作用是④工作时,
 石墨烯电极区的
石墨烯电极区的 基本保持不变,结合化学用语解释原因
基本保持不变,结合化学用语解释原因
您最近一年使用:0次
【推荐2】根据下图填空:
(1)如图1为含有少量Zn杂质的粗银电解精炼银的示意图,则
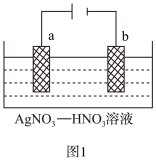
①___________ (填“a”或“b")极为含有杂质的粗银。
②电解一段时间后电解液中c(Ag+)浓度___________ (填“偏大”、“偏小”或“不变”)。
③若b极有少量红棕色气体生成,则生成该气体的电极反应式为___________ 。
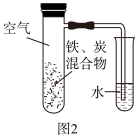
(2)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图2所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是___________。
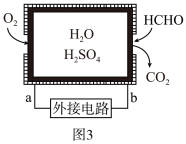
(3)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。某甲醛气体传感器的工作原理如图3所示,则b极是___________ 极。当电路中转移4×10-4 mol电子时,传感。器内参加反应的甲醛(HCHO)质量为___________ g。
(1)如图1为含有少量Zn杂质的粗银电解精炼银的示意图,则

①
②电解一段时间后电解液中c(Ag+)浓度
③若b极有少量红棕色气体生成,则生成该气体的电极反应式为
(2)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图2所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是___________。

| A.铁被氧化的电极反应式为Fe-2e-=Fe2+ |
| B.铁腐蚀过程中化学能全部转化为电能 |
| C.活性炭的存在会加速铁的腐蚀 |
| D.以水代替NaCl溶液,铁不能发生吸氧腐蚀 |

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】金属的腐蚀与防腐是科学研究的重点领域,现代防腐技术日益受到关注。回答下列问题:
(1)“经远舰”在海底多年,舰体腐蚀严重。舰体发生电化学腐蚀时,其正极的电极反应式为___________ (已知正常海水呈弱碱性);为保护舰体,科研人员提出将舰体与电源___________ (填“正极”或“负极”)相连,这种保护方法称为___________ 。
(2)金属铬具有优良的抗腐蚀性能。常在钢铁表面镀一层铬达到防腐的目的。一般电镀过程中,金属铬作为___________ (填“阳极”或“阴极”)材料。工业上常用沉淀法处理含 (橙色)和
(橙色)和 (黄色)的电镀废水,工艺流程如图所示:
(黄色)的电镀废水,工艺流程如图所示:
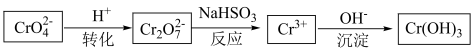
①“转化”过程存在平衡,下列能说明转化达到平衡状态的是___________ 。
A.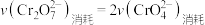 B.溶液颜色保持不变
B.溶液颜色保持不变
C. D.含铬微粒的总浓度保持不变
D.含铬微粒的总浓度保持不变
②“反应”过程中发生反应的离子方程式为___________ 。
③“沉淀”过程中,室温下当 恰好沉淀完全时,溶液的pH=
恰好沉淀完全时,溶液的pH=___________ 。(已知: ,c(Cr3+)≤10-5mol/L时沉淀完全)
,c(Cr3+)≤10-5mol/L时沉淀完全)
(3)钼酸钠和苯并三氮䂳(BTA)的混合液常作为碳钢的缓蚀剂。常温下,碳钢在不同浓度的硫酸和缓蚀剂介质中的腐蚀速率[单位: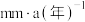 ]数据如图所示。
]数据如图所示。
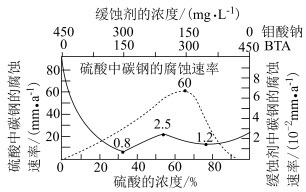
①要使碳钢的缓蚀效果最优,钼酸钠和BTA的浓度比应为___________ 。
②硫酸中碳钢的最高腐蚀速率和缓蚀剂中碳钢的最低腐蚀速率之比为___________ 。
(1)“经远舰”在海底多年,舰体腐蚀严重。舰体发生电化学腐蚀时,其正极的电极反应式为
(2)金属铬具有优良的抗腐蚀性能。常在钢铁表面镀一层铬达到防腐的目的。一般电镀过程中,金属铬作为
 (橙色)和
(橙色)和 (黄色)的电镀废水,工艺流程如图所示:
(黄色)的电镀废水,工艺流程如图所示:
①“转化”过程存在平衡,下列能说明转化达到平衡状态的是
A.
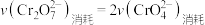 B.溶液颜色保持不变
B.溶液颜色保持不变C.
 D.含铬微粒的总浓度保持不变
D.含铬微粒的总浓度保持不变②“反应”过程中发生反应的离子方程式为
③“沉淀”过程中,室温下当
 恰好沉淀完全时,溶液的pH=
恰好沉淀完全时,溶液的pH= ,c(Cr3+)≤10-5mol/L时沉淀完全)
,c(Cr3+)≤10-5mol/L时沉淀完全)(3)钼酸钠和苯并三氮䂳(BTA)的混合液常作为碳钢的缓蚀剂。常温下,碳钢在不同浓度的硫酸和缓蚀剂介质中的腐蚀速率[单位:
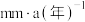 ]数据如图所示。
]数据如图所示。
①要使碳钢的缓蚀效果最优,钼酸钠和BTA的浓度比应为
②硫酸中碳钢的最高腐蚀速率和缓蚀剂中碳钢的最低腐蚀速率之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是用铝土矿(主要成分是 ,此外还含有少量
,此外还含有少量 、
、 等杂质)制备铝的工艺流程:
等杂质)制备铝的工艺流程:
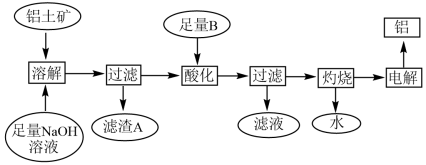
已知:溶液中的硅酸钠能与偏铝酸钠反应,生成硅铝酸盐沉淀,反应的化学方程式为 。
。
(1)铝土矿中的 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为___________ 。
(2)在工艺流程中“酸化”时,加入的最佳物质B是___________ ,理由是___________ 。
(3)工业上用 与C、
与C、 在高温条件下反应制取
在高温条件下反应制取 ,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为
,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为___________ 。
(4)某同学为验证铝与氧化铁发生铝热反应得到的熔融物中还含有 ,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有
,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有 。则物质甲是
。则物质甲是___________ (填化学式),该同学设计的实验方案___________ (填“合理”或“不合理”),原因是___________ (若合理,则不用填写)。
 ,此外还含有少量
,此外还含有少量 、
、 等杂质)制备铝的工艺流程:
等杂质)制备铝的工艺流程:
已知:溶液中的硅酸钠能与偏铝酸钠反应,生成硅铝酸盐沉淀,反应的化学方程式为
 。
。(1)铝土矿中的
 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为(2)在工艺流程中“酸化”时,加入的最佳物质B是
(3)工业上用
 与C、
与C、 在高温条件下反应制取
在高温条件下反应制取 ,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为
,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为(4)某同学为验证铝与氧化铁发生铝热反应得到的熔融物中还含有
 ,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有
,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有 。则物质甲是
。则物质甲是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学学习小组研究盐酸被MnO2氧化的条件,进行如下实验。
(1)已知:MnO2是碱性氧化物。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是____________ 。
(2)II中发生了分解反应,反应的化学方程式是___________ 。
(3)III中无明显现象的原因可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:
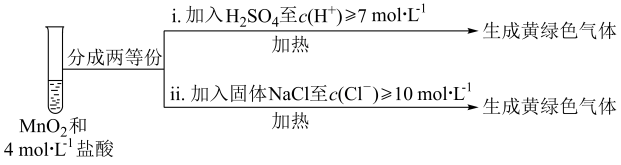
将实验III、IV作对比,得出的结论是_____________ ;将实验IV中i、ii作对比,得出的结论是__________________ 。
实验 | 操作 | 现象 |
I | 常温下将MnO2和12 mol/L浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
II | 将I中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
III | 加热MnO2和4 mol/L稀盐酸混合物 | 无明显现象 |
(1)已知:MnO2是碱性氧化物。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是
(2)II中发生了分解反应,反应的化学方程式是
(3)III中无明显现象的原因可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:

将实验III、IV作对比,得出的结论是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】以盐湖锂精矿(主要成分:Li2CO3,杂质:CaCO3)和盐湖卤水(含一定浓度LiCl和MgCl2)为原料均能制备碳酸锂(Li2CO3)。
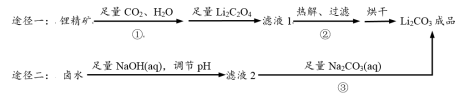
部分溶解度(g/100gH2O)数据见下表:
完成下列填空:
(1)步骤①主要反应的化学方程式为_______ ,反应在常温下进行,温度越高,锂精矿转化率越低的原因可能是_______ 。
(2)步骤②热解、过滤获得的沉淀表面有少量Li2C2O4,不经洗涤也不会影响Li2CO3纯度的原因用化学方程式表示为_______ 。
(3)步骤③的操作是过滤、_______ 洗涤(选填“冷水”或“热水”)、干燥;判断滤液2中Li+是否沉淀完全的方法是_______ 。
(4)Li2CO3(M=74g·mol-1)样品的纯度可用滴定法测定(杂质不参与反应)。反应原理:Li2CO3+2HCl→2LiCl+CO2↑+H2O,用盐酸标准液滴定Li2CO3样品的操作步骤顺序为c、a_______ 。
a.加入0.1~0.2mL甲基红-溴甲粉绿作指示剂;
b.煮沸去除CO2,再冷却到室温;
c.将样品置于锥形瓶中,加水溶解;
d.用盐酸标准液滴定至溶液由绿色变成酒红色;
e.继续滴定至酒红色(滴定突跃区域)即为终点。
(5)用含以下物理量的数学表达式表示Li2CO3的纯度ω=_______ 。
m-Li2CO3样品的质量(g);c-盐酸标准液的浓度(mol·L-1);V1-样品滴定时消耗盐酸的体积(mL);V0-滴定空白溶液(指不加样品进行滴定)时消耗盐酸的体积(mL)。
上述滴定操作中,若缺少步骤b,测定结果将_______ (选填“偏大”或“偏小”)。

部分溶解度(g/100gH2O)数据见下表:
| 温度(℃) | 0 | 20 | 80 |
| LiOH | - | 12.8 | - |
| Li2CO3 | 1.54 | 1.33 | 0.85 |
完成下列填空:
(1)步骤①主要反应的化学方程式为
(2)步骤②热解、过滤获得的沉淀表面有少量Li2C2O4,不经洗涤也不会影响Li2CO3纯度的原因用化学方程式表示为
(3)步骤③的操作是过滤、
(4)Li2CO3(M=74g·mol-1)样品的纯度可用滴定法测定(杂质不参与反应)。反应原理:Li2CO3+2HCl→2LiCl+CO2↑+H2O,用盐酸标准液滴定Li2CO3样品的操作步骤顺序为c、a
a.加入0.1~0.2mL甲基红-溴甲粉绿作指示剂;
b.煮沸去除CO2,再冷却到室温;
c.将样品置于锥形瓶中,加水溶解;
d.用盐酸标准液滴定至溶液由绿色变成酒红色;
e.继续滴定至酒红色(滴定突跃区域)即为终点。
(5)用含以下物理量的数学表达式表示Li2CO3的纯度ω=
m-Li2CO3样品的质量(g);c-盐酸标准液的浓度(mol·L-1);V1-样品滴定时消耗盐酸的体积(mL);V0-滴定空白溶液(指不加样品进行滴定)时消耗盐酸的体积(mL)。
上述滴定操作中,若缺少步骤b,测定结果将
您最近一年使用:0次



