下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式 填空回答以下问题:
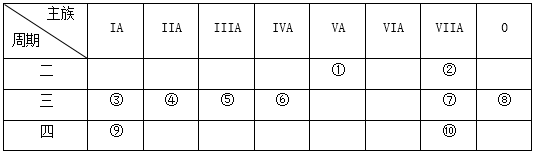
(1)在③~⑦中元素,原子半径最大的是_____________ ,其离子的结构示意图是__________________ 。
(2)表中的①~⑩中元素,非金属性最强的是_______ ,化学性质最稳定的是________ ,金属性最强的是__________ ,最高价氧化物的水化物的酸性最强的是(写该水化物的化学式)______________ 。
(3)⑦的氢化物的水溶液与①的氢化物的水溶液反应的离子方程式为___________________________ 。
(4)用一个化学反应说明⑦比⑩的单质化学性质活泼,写出反应的化学方程式:_____________________ 。

(1)在③~⑦中元素,原子半径最大的是
(2)表中的①~⑩中元素,非金属性最强的是
(3)⑦的氢化物的水溶液与①的氢化物的水溶液反应的离子方程式为
(4)用一个化学反应说明⑦比⑩的单质化学性质活泼,写出反应的化学方程式:
更新时间:2018-07-20 11:38:44
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,元素①-⑦是短周期的主族元素,请参照元素①-⑥在表中的位置,回答下列问题:
(1)写出⑥在元素周期表中的位置_____ 。
(2)②的气态氢化物的沸点____ ⑥的气态氢化物的沸点。(填大于、小于或等于)
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
_____ 。
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是_____ , 与该化合物晶体类型相同的是______ (请用相应的编号填写)。

A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为_____ ,化合物乙与过量盐酸反应的化学方程式为_____ 。
| ① | ② | |||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |
(1)写出⑥在元素周期表中的位置
(2)②的气态氢化物的沸点
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是



A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)原子半径最大的元素是_______ ,非金属性最强的元素是_______ ,形成化合物种类最多的元素是_______ 。(填写元素符号)
(2)元素的最高价氧化物对应的水化物中酸性最强的是_______ ,呈两性的氢氧化物是_______ 。(填写化学式)
(3)能说明⑧与⑨非金属性强弱的实验事实是____________________
(4)能说明④与⑤金属性强弱的实验事实是____________________
(5)表中能形成两性氢氧化物的元素是________ (填写元素符号),写出该元素的氢氧化物与④的最高价氧化物对应水化物反应的离子方程式:_________________________
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)原子半径最大的元素是
(2)元素的最高价氧化物对应的水化物中酸性最强的是
(3)能说明⑧与⑨非金属性强弱的实验事实是
(4)能说明④与⑤金属性强弱的实验事实是
(5)表中能形成两性氢氧化物的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】短周期主族元素A、B、C、D、E的原子序数依次增大。常温下,A、B组成的化合物是常见液体,C的原子半径是短周期主族元素中最大的,D最外层电子数等于电子层数的2倍。回答下列问题:
(1)B在元素周期表中的位置为________ ;A、B组成的原子个数比为1:1的化合物的电子式为________ 。
(2)B、C的简单离子中,半径较大的是________ (填离子符号);A、B、C三种元素组成的化合物中含有的化学键类型是________ 。
(3)C、D的最高价氧化物对应的水化物间反应的离子方程式为________ 。
(4)下列叙述能说明E的非金属性强于D的是________ (填序号)。
a.D的简单氢化物的稳定性强于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
(1)B在元素周期表中的位置为
(2)B、C的简单离子中,半径较大的是
(3)C、D的最高价氧化物对应的水化物间反应的离子方程式为
(4)下列叙述能说明E的非金属性强于D的是
a.D的简单氢化物的稳定性强于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为_________ ,基态Cu3+的核外电子排布式为______
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合做录音磁带磁粉原料的为________ (填序号)。
A.V2O5 B.CrO2
C.PbO D.ZnO
(3)屠呦呦因在抗疟药青蒿素研究中的杰出贡献,成为我国首获科学类诺贝尔奖的人。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为_______ 。

(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合做录音磁带磁粉原料的为
A.V2O5 B.CrO2
C.PbO D.ZnO
(3)屠呦呦因在抗疟药青蒿素研究中的杰出贡献,成为我国首获科学类诺贝尔奖的人。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)表中非金属性最强的元素名称为_______ ,它在元素周期表中的位置_______ 。
(2)③、⑤、⑥的原子半径由大到小的顺序为_______ 。
(3)①分别与④、⑧形成的简单氢化物中,沸点较高的是_______ 。
(4)②、⑦、③的最高价氧化物对应水化物的酸性由强到弱的顺序是_______ 。
(5)①、③、⑤三元素形成的简单的化合物的电子式为_______ 。
(6)工业上,用②的单质在高温下还原SiO2制备Si单质的化学方程式为_______ 。
| ① | ||||||||||
| ② | ③ | ④ | ||||||||
| ⑤ | ⑥ | ⑦ | ⑧ |
(1)表中非金属性最强的元素名称为
(2)③、⑤、⑥的原子半径由大到小的顺序为
(3)①分别与④、⑧形成的简单氢化物中,沸点较高的是
(4)②、⑦、③的最高价氧化物对应水化物的酸性由强到弱的顺序是
(5)①、③、⑤三元素形成的简单的化合物的电子式为
(6)工业上,用②的单质在高温下还原SiO2制备Si单质的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
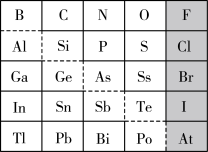
(1)Sn的最高正价为_______ ,I的最高价氧化物对应水化物的化学式为_______ ,Bi的最高价氧化物为_______ 。
(2)元素Ga在元素周期表中的位置为:_______ 。
(3)根据元素周期律等有关知识,推断:
①阴影部分元素的氢化物沸点最高的是_______ (填化学式)。
②N3-、O2-、Al3+、S2-,四种离子半径大小顺序:_______ (用离子符号排序)。
③H3AsO4、H2SeO4、H2SO4的酸性强弱顺序:_______ 。
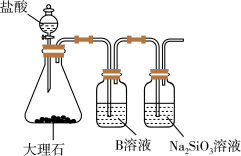
(4)查阅资料可知:硅酸(H2SiO3)是一种难溶于水的弱酸。为比较元素C和Si的非金属性强弱,用图所示装置进行实验。溶液B应该选用_______ 溶液,作用是_______ ,其中能说明C和Si非金属性强弱的化学方程式是:_______ 。

(1)Sn的最高正价为
(2)元素Ga在元素周期表中的位置为:
(3)根据元素周期律等有关知识,推断:
①阴影部分元素的氢化物沸点最高的是
②N3-、O2-、Al3+、S2-,四种离子半径大小顺序:
③H3AsO4、H2SeO4、H2SO4的酸性强弱顺序:
(4)查阅资料可知:硅酸(H2SiO3)是一种难溶于水的弱酸。为比较元素C和Si的非金属性强弱,用图所示装置进行实验。溶液B应该选用

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】X、Y、Z 为原子序数 1~20 号内的元素,将 4.7g X 的最高价氧化物 X2O 溶于 95.3g 水中,所 得溶液浓度为 5.6% 。Y 元素原子与 X 元素原子的最外电子层电子数相同,12g Y 的氢氧化物恰好被0.75 mol/L 的盐酸 400mL 所中和。Z、Y 的原子核外电子层数相同,16g ZO2气体在标准状况下的体积 为 5.6L。试求 X、Y、Z 元素名称。X______________ ,Y_______________ ,Z____________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y.W原子的最外层没有p电子,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子中p电子数比Y原子多2个.
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:__________________ .
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为__________ (用分子式表示).
(3)四种元素原子半径的由大到小为_________ (填元素符号).
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为
(3)四种元素原子半径的由大到小为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】短周期元素X、Y、Z在周期表中位置关系如图所示
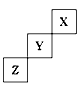
(1)X元素的名称是___________ 。
(2)Y在元素周期表中的位置是__________ ,它形成单质的化学式是_________ 。
(3)Z元素的原子结构示意图为__________ 。写出Z单质与铁反应的化学反应方程式:___________ 。
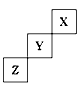
(1)X元素的名称是
(2)Y在元素周期表中的位置是
(3)Z元素的原子结构示意图为
您最近一年使用:0次



