短周期元素X、Y、Z在周期表中位置关系如图所示
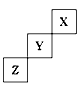
(1)X元素的名称是___________ 。
(2)Y在元素周期表中的位置是__________ ,它形成单质的化学式是_________ 。
(3)Z元素的原子结构示意图为__________ 。写出Z单质与铁反应的化学反应方程式:___________ 。
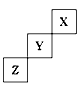
(1)X元素的名称是
(2)Y在元素周期表中的位置是
(3)Z元素的原子结构示意图为
更新时间:2015-05-12 17:08:36
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有A、B、C、D四种短周期主族元素,其原子序数依次增大,已知A、C位于同一主族,A元素在元素周期表中原子半径最小,B、D原子最外层电子数相等,且B、D原子序数之和是A、C原子序数之和的两倍。
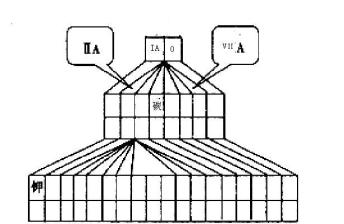
(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出A、B、C、D四种元素的元素符号。_____________
(2)图中将过渡元素涂黑。_______________
(3)由上述四种元素中的某几种所形成的具有漂白作用物质的化学式(写出两种):_______ 、______ 。

(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出A、B、C、D四种元素的元素符号。
(2)图中将过渡元素涂黑。
(3)由上述四种元素中的某几种所形成的具有漂白作用物质的化学式(写出两种):
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表的种类相当多,如大象式、回路式、能级式、亚历山大式等,教材上所附的长式周期表是目前使用最普遍的周期表。请回答下列问题:
(1)长式周期表中氢元素的位置争议最大,原因是_______
(2)有一种非常有趣的商业周期表如图所示。

①3:00时“时针”所指元素单质比11: 00时“时针”所指元素单质的还原性_______ (填“强”或“弱”)。
②8:00时“时针”和“分针”所指的两种元素形成的化合物所含化学键类型为_______ ,其与强酸溶液反应的离子方程式为 _______
(3)“亚历山大式周期表”的元素排列像一座连体三栋大楼(如图所示)。

下列有关其优点的说法中你不认可 的是_______ 。
A.较好地解决了氢元素所在族的问题
B.该周期表保留了长式周期表的优点,明确地表达周期律中族和周期的概念
C.携带和使用均比长才周期表方便
D.较好地处理了镧系和锕系元素,使周期表具有更好的连续性
(1)长式周期表中氢元素的位置争议最大,原因是
(2)有一种非常有趣的商业周期表如图所示。

①3:00时“时针”所指元素单质比11: 00时“时针”所指元素单质的还原性
②8:00时“时针”和“分针”所指的两种元素形成的化合物所含化学键类型为
(3)“亚历山大式周期表”的元素排列像一座连体三栋大楼(如图所示)。

下列有关其优点的说法中你
A.较好地解决了氢元素所在族的问题
B.该周期表保留了长式周期表的优点,明确地表达周期律中族和周期的概念
C.携带和使用均比长才周期表方便
D.较好地处理了镧系和锕系元素,使周期表具有更好的连续性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是____ ,只有负价而无正价的是______ ,还原性最强的单质是______ ,氧化性最强的单质是___ 。
(2)最高价氧化物的水化物中,既能和盐酸又能和氢氧化钠反应的是___ ,酸性最强的是____ ,碱性最强的是_____ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的_____ 。
(4)在A、B、C、D、E、F、G、H中,原子半径最大的是______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | F | H | I |
(2)最高价氧化物的水化物中,既能和盐酸又能和氢氧化钠反应的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在A、B、C、D、E、F、G、H中,原子半径最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据下表回答问题:
(1)甲元素最高价氧化物对应的水化物呈___________ 性(填“酸、碱”),乙元素最高价氧化物对应的水化物的化学式为___________ 。
(2)比较这甲、乙、丁三种元素的原子半径大小:___________ (填元素符号)。
(3)丙在周期表的位置为___________ 。
(4)甲元素最高价氧化物对应水化物与丁元素最高价氧化物反应的化学方程式为___________ 。
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 元素符号 | ① | Cl | O | Al |
原子结构示意图 | 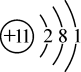 | 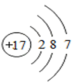 | 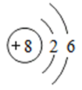 | 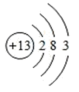 |
| 周期 | 三 | 三 | 二 | 三 |
| 族 | ⅠA | ⅦA | ③ | ⅢA |
(1)甲元素最高价氧化物对应的水化物呈
(2)比较这甲、乙、丁三种元素的原子半径大小:
(3)丙在周期表的位置为
(4)甲元素最高价氧化物对应水化物与丁元素最高价氧化物反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】六种短周期元素在周期表中的相对位置如下所示,其中E元素原子核外电子总数是其最外层电子数的3倍。关于元素周期表及这六种元素性质,请回答:

(1)这六种元素的氢化物中,最稳定的是___________ .(写化学式);
(2)AF2的结构式为_____________ .
(3)在一定条件下,由B单质与H2反应生成1 molG气体时,放出的热量为46.2 kJ,写出该反应的热化学方程式:_____________________ .
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式__________________________ .该反应中被氧化的G与参与反应的G的质量之比__________ .
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:__________ .

(1)这六种元素的氢化物中,最稳定的是
(2)AF2的结构式为
(3)在一定条件下,由B单质与H2反应生成1 molG气体时,放出的热量为46.2 kJ,写出该反应的热化学方程式:
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表短周期的一部分:
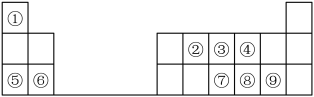
请按要求用化学用语 回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为___ ;
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程___ ;
(3)比元素⑦的原子序数多17的元素在周期表的位置为___ ;
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式___ ,若将其溶于水,破坏了其中的___ (填“离子键”、“共价键”或“离子键和共价键”);
(5)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4:1反应的离子方程式___ 。

请按要求
(1)元素④、⑥、⑨的离子半径由大到小的顺序为
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程
(3)比元素⑦的原子序数多17的元素在周期表的位置为
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式
(5)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4:1反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部位于元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成。现有a~g 7种短周期元素,是除氧、硫、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
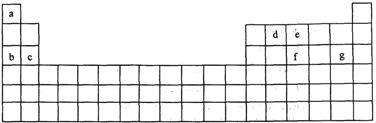
(1)元素的原子间反应最容易形成离子键的是下列中的( ) ,元素的原子间反应容易形成共价键的是下列中的( )
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是( ) 。
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为__________________ 。
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式_______ ,化学键类型为____ ,与稀盐酸反应的方程式为_____________________ .

(1)元素的原子间反应最容易形成离子键的是下列中的
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表与元素周期律是指导学生学好元素及其化合物知识的理论工具,回答下列问题。
(1)最活泼的非金属元素是_____ (填元素符号);短周期元素中共有____ 种金属元素。
(2)硫元素在元素周期表中的位置为________ 。
(3)用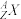 形式表示出中子数为10 的氧原子
形式表示出中子数为10 的氧原子________ 。
(4) 下表为元素周期表的一部分,请参照元素①~ ⑦在表中的位置,用化学用语回答下列问题:

则①、②、⑥的最高价氧化物对应的水化物的酸性由强到弱的顺序是______ (用化学式表示), ③形成的简单氢化物的结构式为_______ ,⑦的最高价氧化物的化学式_______ ,③与④形成的含有两种化学键物质的电子式为________ ,④、⑤两种元素的最高价氧化物对应水化物之间可发生反应,对应离子方程式为___________________ 。
(1)最活泼的非金属元素是
(2)硫元素在元素周期表中的位置为
(3)用
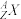 形式表示出中子数为10 的氧原子
形式表示出中子数为10 的氧原子(4) 下表为元素周期表的一部分,请参照元素①~ ⑦在表中的位置,用化学用语回答下列问题:

则①、②、⑥的最高价氧化物对应的水化物的酸性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在科技发展中发挥着重要的作用。完成下列填空:
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指_______ ,58是指_______ 。
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为_______ 。
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是_______ ,SiH4的空间构型为_______ 。
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为_______ ,T的电子式为_______ 。
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是_______ (选填编号)
a.SiO + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.
c.SiH4 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑
d.Si+O2 SiO2;C+O2
SiO2;C+O2 CO2
CO2
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是
a.SiO
 + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.

c.SiH4
 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑d.Si+O2
 SiO2;C+O2
SiO2;C+O2 CO2
CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y.W原子的最外层没有p电子,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子中p电子数比Y原子多2个.
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:__________________ .
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为__________ (用分子式表示).
(3)四种元素原子半径的由大到小为_________ (填元素符号).
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为
(3)四种元素原子半径的由大到小为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)原子半径最大的元素是_______ ,非金属性最强的元素是_______ ,形成化合物种类最多的元素是_______ 。(填写元素符号)
(2)元素的最高价氧化物对应的水化物中酸性最强的是_______ ,呈两性的氢氧化物是_______ 。(填写化学式)
(3)能说明⑧与⑨非金属性强弱的实验事实是____________________
(4)能说明④与⑤金属性强弱的实验事实是____________________
(5)表中能形成两性氢氧化物的元素是________ (填写元素符号),写出该元素的氢氧化物与④的最高价氧化物对应水化物反应的离子方程式:_________________________
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)原子半径最大的元素是
(2)元素的最高价氧化物对应的水化物中酸性最强的是
(3)能说明⑧与⑨非金属性强弱的实验事实是
(4)能说明④与⑤金属性强弱的实验事实是
(5)表中能形成两性氢氧化物的元素是
您最近一年使用:0次



