科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部位于元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成。现有a~g 7种短周期元素,是除氧、硫、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
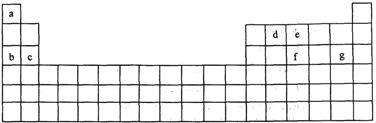
(1)元素的原子间反应最容易形成离子键的是下列中的( ) ,元素的原子间反应容易形成共价键的是下列中的( )
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是( ) 。
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为__________________ 。
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式_______ ,化学键类型为____ ,与稀盐酸反应的方程式为_____________________ .

(1)元素的原子间反应最容易形成离子键的是下列中的
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式
10-11高二下·福建厦门·单元测试 查看更多[1]
(已下线)2010—2011学年厦门市翔安第一中学高一下学期第二章单元测试化学试卷
更新时间:2016-12-09 01:54:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表列出了①~⑩十种元素在周期表中的位置:
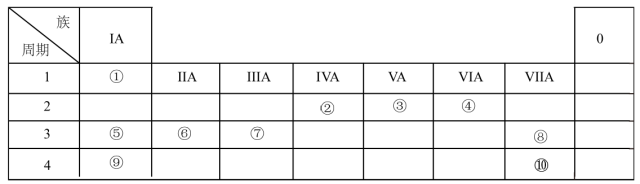
请按要求回答下列问题:
(1)元素⑤的原子结构示意图为___ ;元素②的最高价氧化物的电子式是___ 。
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是___ (填元素符号);这三种元素最高价氧化物对应水化物中碱性最强的是___ (填化学式)。
(3)③、④元素的简单氢化物的稳定性较弱的是___ (填化学式)。
(4)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:___ ;①与②所形成的最简单的烯烃与溴的四氯化碳溶液反应的化学方程式:___ 。

(5)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:___ 。
(6)写出元素⑨的单质与水反应的化学方程式:___ 。
(7)请从原子结构的角度解释,元素⑧非金属性比元素⑩强的原因:___ 。

请按要求回答下列问题:
(1)元素⑤的原子结构示意图为
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是
(3)③、④元素的简单氢化物的稳定性较弱的是
(4)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:

(5)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:
(6)写出元素⑨的单质与水反应的化学方程式:
(7)请从原子结构的角度解释,元素⑧非金属性比元素⑩强的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填写下列空白:
(1)已知某原子的核内有77个质子,质量数为191,则其核内的中子数为_________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)周期表中最活泼的非金属元素位于第_____________ 纵行。
(4)所含元素为18种的周期是第____________ 周期。
(5)4g D2和20g 18O的单质化合时最多能生成_______ g D2O,这些D2O分子中含___ mol中子。
(6)氯元素在自然界中有质量数为35和37的两种核素,氯元素的相对原子质量为35.5,则两核素在自然界中的含量之比约为______________ 。
(1)已知某原子的核内有77个质子,质量数为191,则其核内的中子数为
(2)周期表中位于第8纵行的铁元素属于第
(3)周期表中最活泼的非金属元素位于第
(4)所含元素为18种的周期是第
(5)4g D2和20g 18O的单质化合时最多能生成
(6)氯元素在自然界中有质量数为35和37的两种核素,氯元素的相对原子质量为35.5,则两核素在自然界中的含量之比约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】图是中学教材中元素周期表的一部分,其中标出A~F12种元素,试回答下列问题:
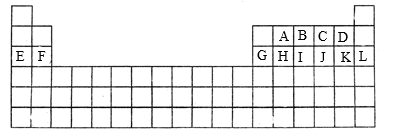
(1)在上表所列出的短周期 元素中
①原子半径最大的是(除稀有气体元素)_______ 。(填写元素符号)
②形成的气态氢化物最稳定的是_______ ;(填该氢化物化学式)
③最高价氧化物对应的水化物中酸性最强的是_______ (填该酸化学式)
④形成的阴离子还原性最弱的是_______ (填该离子符号) 该离子电子式为_______
(2)用电子式表示下列物质的形成过程F与D形成的化合物_______ ;
(3)若某元素的原子序数为116,则该元素在元素周期表中的位置是_______ 。
(4)铜与J的最高价氧化物的水化合物反应的方程式:_______

(1)在上表所列出的
①原子半径最大的是(除稀有气体元素)
②形成的气态氢化物最稳定的是
③最高价氧化物对应的水化物中酸性最强的是
④形成的阴离子还原性最弱的是
(2)用电子式表示下列物质的形成过程F与D形成的化合物
(3)若某元素的原子序数为116,则该元素在元素周期表中的位置是
(4)铜与J的最高价氧化物的水化合物反应的方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有A、B、C、D四种短周期主族元素,其原子序数依次增大,已知A、C位于同一主族,A元素在元素周期表中原子半径最小,B、D原子最外层电子数相等,且B、D原子序数之和是A、C原子序数之和的两倍。
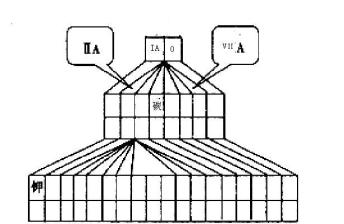
(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出A、B、C、D四种元素的元素符号。_____________
(2)图中将过渡元素涂黑。_______________
(3)由上述四种元素中的某几种所形成的具有漂白作用物质的化学式(写出两种):_______ 、______ 。

(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出A、B、C、D四种元素的元素符号。
(2)图中将过渡元素涂黑。
(3)由上述四种元素中的某几种所形成的具有漂白作用物质的化学式(写出两种):
您最近一年使用:0次
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
(1)上述元素属于第三周期,且可以做半导体材料的是_______ (填字母代号)。
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ·mol-1):
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_______ 。
②表中Y可能为以上13种元素中的_______ (填写字母)元素。用元素符号表示X和l形成化合物的电子式是_______ 。
(3)以上13种元素中,_______ (填写字母)元素原子失去核外第一个电子需要的能量最多。
(4)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中元素c位于_______ 区。
| b | |||||||||||||||||||
| h | j | ||||||||||||||||||
| a | c | f | i | l | m | ||||||||||||||
| e | g | ||||||||||||||||||
| d | k | ||||||||||||||||||
(1)上述元素属于第三周期,且可以做半导体材料的是
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ·mol-1):
| 锂 | X | Y | |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量
②表中Y可能为以上13种元素中的
(3)以上13种元素中,
(4)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中元素c位于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表短周期的一部分:
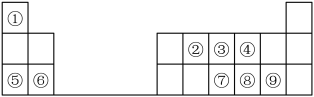
请按要求用化学用语 回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为___ ;
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程___ ;
(3)比元素⑦的原子序数多17的元素在周期表的位置为___ ;
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式___ ,若将其溶于水,破坏了其中的___ (填“离子键”、“共价键”或“离子键和共价键”);
(5)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4:1反应的离子方程式___ 。

请按要求
(1)元素④、⑥、⑨的离子半径由大到小的顺序为
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程
(3)比元素⑦的原子序数多17的元素在周期表的位置为
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式
(5)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4:1反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】1.H2O2、KCl、NaOH、Na2O2、HCl、O2中只含离子键的是_________ ,只含极性键的是__________ ,只含非极性键的是__________ ,既含离子键又含极性键的是__________ ,既含离子键又含非极性键的是___________ ,既有极性键又有非极性键的是________ 。
您最近一年使用:0次
【推荐2】化学应该明白“从生活中来,到生活中去”的道理。家庭厨卫用品中有许多常见的化学物质,括号内为厨卫用品的主要成分:①食盐(NaCl)②蔗糖③食醋(3-5%醋酸)④碱粉(Na2CO3)⑤小苏打粉(NaHCO3)⑥84消毒液(NaClO)⑦洁厕灵液(HCl)⑧净水剂固体(明矾)⑨铁锅(Fe)
回答下列问题:
(1)明矾的化学式为KAl(SO4)2·12H2O,属于___________ (填“纯净物”或“混合物”)。
(2)厨卫用品中,能够导电的有___________。
(3)小苏打的主要成分NaHCO3在水溶液的电离方程式为___________ ;84消毒液的主要成分NaClO中含有的化学键有___________ 。
(4)除去Na2CO3固体中的NaHCO3涉及的化学方程式是___________ 。
(5)实验室需要配制0.200mol/L的Na2CO3溶液450mL。配制上述溶液时,需要Na2CO3固体的质量为___________ g;如果定容时俯视刻度,则所配溶液的浓度___________ (用“偏高”、“偏低”和“无影响”填空)。
(6)用双线桥法表示下面反应的电子转移方向和数目___________ 。
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
此反应的还原产物和氧化产物的物质的量之比为___________ 。
回答下列问题:
(1)明矾的化学式为KAl(SO4)2·12H2O,属于
(2)厨卫用品中,能够导电的有___________。
| A.①②③⑥⑦ | B.④⑤⑥⑦⑨ | C.③④⑤⑥⑦⑨ | D.③⑥⑦⑨ |
(4)除去Na2CO3固体中的NaHCO3涉及的化学方程式是
(5)实验室需要配制0.200mol/L的Na2CO3溶液450mL。配制上述溶液时,需要Na2CO3固体的质量为
(6)用双线桥法表示下面反应的电子转移方向和数目
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
此反应的还原产物和氧化产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期数与主族序数相等。请用化学用语 回答下列问题:
(1)B元素在周期表中的位置为_______ ;由A、C、D三种元素组成的化合物中含有的化学键为_______ 。
(2)写出BC2的电子式:_______ 。
(3)元素E的单质与元素D的最高价氧化物的水化物反应的离子方程式:_______ 。
(4)常温下,A2C与元素D的单质反应后,所得溶液的pH_______ 7(填“<”、“=”或“>”)。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,灼烧该化合物时,火焰呈_______ 色, DA能与水反应放出氢气,若将1 mol DA和1 mol E单质混合加入足量的水,充分反应后生成的气体在标准状况下的体积是_______ L。
(1)B元素在周期表中的位置为
(2)写出BC2的电子式:
(3)元素E的单质与元素D的最高价氧化物的水化物反应的离子方程式:
(4)常温下,A2C与元素D的单质反应后,所得溶液的pH
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,灼烧该化合物时,火焰呈
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)写出下列微粒的电子式:NaOH__________ ;CS2_________ ;Na2S_________ NH3__________ ; NH4H________ ;
(2)用电子式表示下列物质的形成过程MgCl2______________________
(3)现有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl①只由离子键构成的物质是________________ 。
②只由极性键构成的物质是_______________ 。
③由极性键和非极性键构成的物质是________________ 。
④由离子键和极性键构成的物质是________________ 。
⑤由离子键和非极性键构成的物质是________________ 。
(2)用电子式表示下列物质的形成过程MgCl2
(3)现有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl①只由离子键构成的物质是
②只由极性键构成的物质是
③由极性键和非极性键构成的物质是
④由离子键和极性键构成的物质是
⑤由离子键和非极性键构成的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)纳米材料二氧化钛(TiO2)可做优良的催化剂。
据报道:“生态马路”是在铺设时加入一定量的TiO2, TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:

①b中破坏的是__________ (填“极性共价键”或“非极性共价键”)。
②H2O2能清除路面空气中的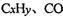 等,其主要是利用了H2O2的作用是
等,其主要是利用了H2O2的作用是_____________________________________________ (填“氧化性”或“还原性”)。
(2)某固体混合物中含有Na+、K+、Mg2+和Cl-、Br-五种微粒。
I.欲将钠、钾、镁三元素大致分离开来,并将氯、溴两元素大致分离开来,有以下方法和操作步骤可供选择(其中有的步骤可选两次)。
①溶于水制成稀溶液;②溶于水制成浓溶液;③通入足量CO2;④加入足量氯水;
⑤通入足量氨气; ⑥过滤; ⑦用四氯化碳萃取.
选取最合理的方法和步骤:(按顺序先后填写编号)___________________________ .
II.分离后剩余的水溶液中所含的主要物质是________________________________ .
III.在上述分离过程中分离出一种化合物晶体,欲得到干燥的该化合物固体,有两种方法可供选择:①.加热蒸发掉水分;②.将过滤得到的固体物质自然风干;正确的方法应选择______________________________________________ .
据报道:“生态马路”是在铺设时加入一定量的TiO2, TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:

①b中破坏的是
②H2O2能清除路面空气中的
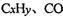 等,其主要是利用了H2O2的作用是
等,其主要是利用了H2O2的作用是(2)某固体混合物中含有Na+、K+、Mg2+和Cl-、Br-五种微粒。
I.欲将钠、钾、镁三元素大致分离开来,并将氯、溴两元素大致分离开来,有以下方法和操作步骤可供选择(其中有的步骤可选两次)。
①溶于水制成稀溶液;②溶于水制成浓溶液;③通入足量CO2;④加入足量氯水;
⑤通入足量氨气; ⑥过滤; ⑦用四氯化碳萃取.
选取最合理的方法和步骤:(按顺序先后填写编号)
II.分离后剩余的水溶液中所含的主要物质是
III.在上述分离过程中分离出一种化合物晶体,欲得到干燥的该化合物固体,有两种方法可供选择:①.加热蒸发掉水分;②.将过滤得到的固体物质自然风干;正确的方法应选择
您最近一年使用:0次
【推荐3】用正确的序号 填空:①12C、13C、14C;②正戊烷与新戊烷;③C2H6和C3H8;④O2和O3;⑤苯与乙苯;⑥ 和
和 ⑦
⑦ ;
;
(1)互为同位素的是___ ;互为同素异形体的是___ ;互为同分异构体的是___ ;互为同系物的是___ ;只含有极性键的是_____________ ;既含有极性键又含有非极性键的是_______ 。
(2)用系统命名法给下列有机物命名:
①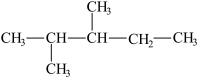
_____________ ;
②3,5-二甲基庚烷___________________________ ;
(3)丙烯的结构简式为____________________________________ ;
(4)写出乙苯的3个同分异构体的结构简式_________ ,___________ ,___________ ;
(5)写出下面的结构简式,羧基_________ 、羟基_________ 。
 和
和 ⑦
⑦ ;
;(1)互为同位素的是
(2)用系统命名法给下列有机物命名:
①

②3,5-二甲基庚烷
(3)丙烯的结构简式为
(4)写出乙苯的3个同分异构体的结构简式
(5)写出下面的结构简式,羧基
您最近一年使用:0次



