A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期数与主族序数相等。请用化学用语 回答下列问题:
(1)B元素在周期表中的位置为_______ ;由A、C、D三种元素组成的化合物中含有的化学键为_______ 。
(2)写出BC2的电子式:_______ 。
(3)元素E的单质与元素D的最高价氧化物的水化物反应的离子方程式:_______ 。
(4)常温下,A2C与元素D的单质反应后,所得溶液的pH_______ 7(填“<”、“=”或“>”)。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,灼烧该化合物时,火焰呈_______ 色, DA能与水反应放出氢气,若将1 mol DA和1 mol E单质混合加入足量的水,充分反应后生成的气体在标准状况下的体积是_______ L。
(1)B元素在周期表中的位置为
(2)写出BC2的电子式:
(3)元素E的单质与元素D的最高价氧化物的水化物反应的离子方程式:
(4)常温下,A2C与元素D的单质反应后,所得溶液的pH
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,灼烧该化合物时,火焰呈
更新时间:2022-02-24 20:52:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。
Ⅰ.雄黄(As4S4)的制备。
(1) 和
和 在盐酸中反应转化为
在盐酸中反应转化为 和
和 并放出
并放出 气体(反应前后硫元素化合价不变)。若
气体(反应前后硫元素化合价不变)。若 和
和 恰好完全反应,
恰好完全反应, 和
和 的物质的量之比为
的物质的量之比为___________ 。
(2)上述反应中的被氧化元素是___________ ,反应产生的气体可用___________ 吸收,若产生的 气体
气体 (标况下测定),则转移电子数为
(标况下测定),则转移电子数为___________ 。
Ⅱ.雌黄(As2S3)的性质。
 和
和 有如下反应:
有如下反应: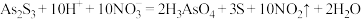
(3)请用单线桥法标出上述反应的电子转移_________ 。
(4)若生成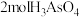 ,反应产物
,反应产物 与
与 (标准状况)混合后用水吸收恰好全部转化成浓
(标准状况)混合后用水吸收恰好全部转化成浓 ,需要
,需要
___________ L(标准状况下)。然后浓 与过量的碳加热进行反应,所产生的
与过量的碳加热进行反应,所产生的 的量
的量___________ 。(填选项)
a.小于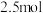 b.等于
b.等于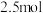 c.大于
c.大于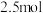 d.无法确定
d.无法确定
(5)已知 为直线型极性分子,该分子中含有
为直线型极性分子,该分子中含有___________ 。(填选项)
a.极性共价键 b.非极性共价键 c.离子键 d.金属键
Ⅰ.雄黄(As4S4)的制备。
(1)
 和
和 在盐酸中反应转化为
在盐酸中反应转化为 和
和 并放出
并放出 气体(反应前后硫元素化合价不变)。若
气体(反应前后硫元素化合价不变)。若 和
和 恰好完全反应,
恰好完全反应, 和
和 的物质的量之比为
的物质的量之比为(2)上述反应中的被氧化元素是
 气体
气体 (标况下测定),则转移电子数为
(标况下测定),则转移电子数为Ⅱ.雌黄(As2S3)的性质。
 和
和 有如下反应:
有如下反应: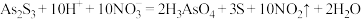
(3)请用单线桥法标出上述反应的电子转移
(4)若生成
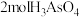 ,反应产物
,反应产物 与
与 (标准状况)混合后用水吸收恰好全部转化成浓
(标准状况)混合后用水吸收恰好全部转化成浓 ,需要
,需要
 与过量的碳加热进行反应,所产生的
与过量的碳加热进行反应,所产生的 的量
的量a.小于
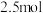 b.等于
b.等于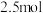 c.大于
c.大于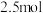 d.无法确定
d.无法确定(5)已知
 为直线型极性分子,该分子中含有
为直线型极性分子,该分子中含有a.极性共价键 b.非极性共价键 c.离子键 d.金属键
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在Cl2 + SO2 + 2H2O = 2HCl + H2SO4的反应中:
(1)氧化剂是______________ ,还原剂是__________________ ,
(2)若反应消耗7.1g Cl2,同时消耗标准状况下SO2的体积约为____________ L,反应生成H2SO4物质的量是___________ mol。
(1)氧化剂是
(2)若反应消耗7.1g Cl2,同时消耗标准状况下SO2的体积约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化还原反应在日常生活和工业生产中有重要应用。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:
(1)用“双线桥”标明该反应中电子转移的方向和数目。__________

(2)该反应中被氧化的元素是___________ ,还原产物是___________ 。
(3)该反应中氧化剂与还原剂的微粒个数比为___________ 。
Ⅱ.阅读下面一段材料并回答问题。
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为___________ 。
(5)下列关于K2FeO4的说法中,不正确的是___________ 。
a.是强氧化性的盐 b.固体保存需要防潮
b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式___________ 。
(7)将K2FeO4与水反应的化学方程式补充完整并配平:____________
___________ +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为___________ 个
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为___________ g。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:

(1)用“双线桥”标明该反应中电子转移的方向和数目。

(2)该反应中被氧化的元素是
(3)该反应中氧化剂与还原剂的微粒个数比为
Ⅱ.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】K2FeO4【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为
(5)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
 b.固体保存需要防潮
b.固体保存需要防潮c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式
(7)将K2FeO4与水反应的化学方程式补充完整并配平:
___________
 +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素 的原子得到3个电子,或元素
的原子得到3个电子,或元素 的原子失去2个电子后,他们的电子层结构都与
的原子失去2个电子后,他们的电子层结构都与 原子相同,则
原子相同,则 和
和 元素形成的化合物的化学式是
元素形成的化合物的化学式是______ 。
 的原子得到3个电子,或元素
的原子得到3个电子,或元素 的原子失去2个电子后,他们的电子层结构都与
的原子失去2个电子后,他们的电子层结构都与 原子相同,则
原子相同,则 和
和 元素形成的化合物的化学式是
元素形成的化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】X、Y、Z、M、N是原子序数小于18的五种元素,且原子序数依次增大。X原子中没有中子,Y元素最高正价与最低负价之和为0;M与X的原子最外层电子数相同;Z、N分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)Z2—的结构示意图______________ ;YZ2的电子式___________________ ;X2Z2的结构式________________ 。
(2)Z与N形成的化合物常温下是____________ 晶体;其熔融体_____ (能、不能)导电。
(1)Z2—的结构示意图
(2)Z与N形成的化合物常温下是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】U、V、W、X、Y、Z是原子序数依次增大的短周期元素。已知:
①WU4++XU-=WU3+U2X,各种反应物和生成物的电子总数都与Y+相等;
②Z的单质在X2中燃烧的产物可使品红溶液褪色;
③V的单质在X2中燃烧可生成VX和VX2两种气体;
④Y的单质是一种金属,该金属与X2反应可生成Y2X和Y2X2两种固体。
请回答下列问题:
(1)V、W、X形成的10电子氢化物中,沸点最高的是___________________ (写化学式)。
(2)U2X2与FeSO4按物质的量之比1:2溶于稀硫酸中,反应的离子方程式为__________ 。
(3)常温下,向pH=11的Y2VX3溶液中加入过量石灰乳,过滤后所得溶液pH=13,则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是______________________ 。

(4)已知由U、W两种元素组成的共价化合物联氨的球棍模型如图所示,则联氨分子的电子式为____________ 。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_______ (已知:N2H4+H+=N2H5+的K=8.7×107;Kw=1.0×10-14)。联氨与过量硫酸形成的酸式盐的化学式为______________ 。
①WU4++XU-=WU3+U2X,各种反应物和生成物的电子总数都与Y+相等;
②Z的单质在X2中燃烧的产物可使品红溶液褪色;
③V的单质在X2中燃烧可生成VX和VX2两种气体;
④Y的单质是一种金属,该金属与X2反应可生成Y2X和Y2X2两种固体。
请回答下列问题:
(1)V、W、X形成的10电子氢化物中,沸点最高的是
(2)U2X2与FeSO4按物质的量之比1:2溶于稀硫酸中,反应的离子方程式为
(3)常温下,向pH=11的Y2VX3溶液中加入过量石灰乳,过滤后所得溶液pH=13,则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是

(4)已知由U、W两种元素组成的共价化合物联氨的球棍模型如图所示,则联氨分子的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在第3周期中,从水或酸中置换氢的能力最强的元素的符号为_______ ,化学性质最稳定的元素的符号是_______ ,最高价氧化物对应水化物中酸性最强的物质的化学式是_______ ,碱性最强的物质的化学式是_______ ,显两性的氢氧化物的化学式是_______ ,该两性氢氧化物与烧碱溶液反应的离子方程式为_______ ;原子半径最小的元素的原子结构示意图_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大。A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是: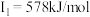 ,
,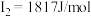 ,
,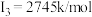 ,
,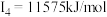 ;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
(1) 是一种常用的溶剂,为
是一种常用的溶剂,为______ 分子(填“极性”或“非极性”),该分子的VSEPR模型名称是_____ 。
(2)X形成的单质与NaOH溶液反应的离子方程式为_________ ,超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于_____ 晶体。
(3)X,氧、B元素的电负性由大到小的顺序为________ (用元素符号作答)。
(4)Z的基态原子核外电子排布式为_______ 。
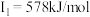 ,
,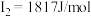 ,
,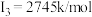 ,
,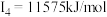 ;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:(1)
 是一种常用的溶剂,为
是一种常用的溶剂,为(2)X形成的单质与NaOH溶液反应的离子方程式为
(3)X,氧、B元素的电负性由大到小的顺序为
(4)Z的基态原子核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是部分短周期元素的信息,用化学用语回答下列问题。
(1)元素A在元素周期表中的位置为________ 。B的某种核素中中子数比质子数多1,则表示该核素的原子符号为_________________ 。
(2)写出钙与M原子个数比为1:2的化合物的电子式______________ 其中含有的化学键类型为__________ (填离子键、极性键或非极性键)。
(3)M2-、D+、G2-离子半径大小顺序是___ > > (用离子符号回答)。
(4)某同学设计实验证明A、B、F的非金属性强弱关系。
①溶液a和b分别为__________ ,_____________ 。
②溶液c中的离子方程式为____________________ 。
(5)将0.5molD2M2投入100mL3mol/LECl3溶液中,转移电子的物质的量为________________ 。
| 元素 | D | M | G | E |
| 性质 结构 信息 | 单质制成的高压 灯,发出的黄光透 雾力强、射程远 | 氢化物常温下呈液 态,M的双原子阴 离子有18个电子 | 原子核外M 层比L层少2 个电子 | +3价阳离子的 核外电子排布 与氖原子相同 |
| 元素代号 | A | B | F |
| 原子半径/nm | 0.077 | 0.075 | 0.117 |
| 主要化合价 | +4、-4 | +5、-3 | +4、4 |
(1)元素A在元素周期表中的位置为
(2)写出钙与M原子个数比为1:2的化合物的电子式
(3)M2-、D+、G2-离子半径大小顺序是
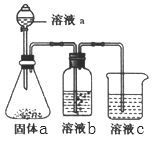
(4)某同学设计实验证明A、B、F的非金属性强弱关系。
①溶液a和b分别为
②溶液c中的离子方程式为
(5)将0.5molD2M2投入100mL3mol/LECl3溶液中,转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④H2SO4溶于水、⑤O2溶于水、⑥NaHSO4溶于水,未发生化学键破坏的是________ ;(填序号,下同)仅破坏离子键的是________ ;仅破坏共价键的是________ ;既破坏离子键又破坏共价键的是________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)下列属于吸热反应的是________ ;属于放热反应的是________ 。
①煅烧石灰石 ②木炭燃烧 ③酸碱中和 ④二氧化碳和碳高温反应
(2) 熔点较低,易升华,溶于醇和醚,其与
熔点较低,易升华,溶于醇和醚,其与 化学性质相似。由此可推断
化学性质相似。由此可推断 的化学键是
的化学键是________ (填“离子键”或“共价键”),其在固态时属于________ (填“原子”、“分子”或“离子”)晶体。
①煅烧石灰石 ②木炭燃烧 ③酸碱中和 ④二氧化碳和碳高温反应
(2)
 熔点较低,易升华,溶于醇和醚,其与
熔点较低,易升华,溶于醇和醚,其与 化学性质相似。由此可推断
化学性质相似。由此可推断 的化学键是
的化学键是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)下列几组物质中:
①18O2和16O2 ②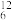 C和
C和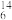 C ③正丁烷和异丁烷 ④红磷和白磷
C ③正丁烷和异丁烷 ④红磷和白磷
⑤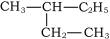 和
和 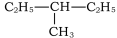 ⑥
⑥ 和
和
⑦CH4和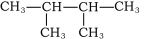
属于同位素的是________ (填序号,下同);属于同分异构体的是________ ;属于同系物的是________ 。
(2)下列各物质:①He ②NH3 ③H2O2 ④CaO ⑤KOH ⑥Na2O2 ⑦Al2O3 ⑧MgCl2中,只含共价键的是____________ ;既含离子键又含共价键的物质是____________ 。
(3)下列变化过程:①碘的升华 ②NaCl固体溶于水 ③蔗糖溶于水 ④HCl气体溶于水⑤烧碱熔化 ⑥氯化铵受热分解,其中化学键没有被破坏的是________ ;既破坏离子键又破坏共价键的是________ 。
①18O2和16O2 ②
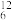 C和
C和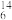 C ③正丁烷和异丁烷 ④红磷和白磷
C ③正丁烷和异丁烷 ④红磷和白磷⑤
 和
和 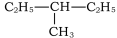 ⑥
⑥ 和
和
⑦CH4和
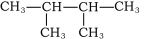
属于同位素的是
(2)下列各物质:①He ②NH3 ③H2O2 ④CaO ⑤KOH ⑥Na2O2 ⑦Al2O3 ⑧MgCl2中,只含共价键的是
(3)下列变化过程:①碘的升华 ②NaCl固体溶于水 ③蔗糖溶于水 ④HCl气体溶于水⑤烧碱熔化 ⑥氯化铵受热分解,其中化学键没有被破坏的是
您最近一年使用:0次



