在第3周期中,从水或酸中置换氢的能力最强的元素的符号为_______ ,化学性质最稳定的元素的符号是_______ ,最高价氧化物对应水化物中酸性最强的物质的化学式是_______ ,碱性最强的物质的化学式是_______ ,显两性的氢氧化物的化学式是_______ ,该两性氢氧化物与烧碱溶液反应的离子方程式为_______ ;原子半径最小的元素的原子结构示意图_______ 。
更新时间:2021-04-16 02:50:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl……
反应②中形成的化合物的电子式为_______ ;反应③中被破坏的化学键属于_______ 键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是_______ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第_______ 周期_______ 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是_______
a卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:
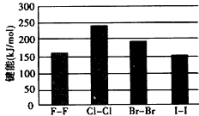
①非金属性强的卤素,其单质分子的化学键_______ 断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:_______
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl……
反应②中形成的化合物的电子式为
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
a卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:

①非金属性强的卤素,其单质分子的化学键
②卤素单质键能大小与键长的关系为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W是原子序数依次增大的短周期主族元素。通常状况下,X与W元素均能形成-1价的气态氢化物,Y为同周期主族元素中原子半径最大的元素,X、Z和W的原子最外层电子数之和为20。回答下列问题:
(1) W在元素周期表中的位置是__________ 。
(2)X和Y元素简单离子的半径较大的是________ (填离子符号);Z和W元素气态氢化物的稳定性较弱的是__________ (填化学式)。
(3)Y的氧化物中既含离子键又含共价键的是__________ (用电子式表示)。
(4)Z的最高价氧化物对应水化物的浓溶液(过量)和氧化亚铜共热,反应的化学方程式为________ 。
(1) W在元素周期表中的位置是
(2)X和Y元素简单离子的半径较大的是
(3)Y的氧化物中既含离子键又含共价键的是
(4)Z的最高价氧化物对应水化物的浓溶液(过量)和氧化亚铜共热,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】VIA 元素的各种性质可归纳整理如下:
回答下列问题:
(1)碲(Te)的氧化物分子式是____________________ 。
(2)硒酸与碲酸酸性较强的是____________________ (填化学式)。
(3)比较键能:H—S_____ H—Se(填“>”或“<”)。
(4)氢硒酸放在空气中,可能发生反应的化学方程式为______________________________ 。
(5)下图所示为 VIA 族元素单质与 H2反应过程中体系温度变化示意图,其中 a、b、c 分别表示VIA 族中某一元素的单质,下图为相同物质的量的单质与 H2反应过程中的体系温度变化。
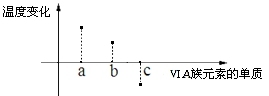
则:c 代表__________ 。(均写单质名称)
| 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点/°C | -218.4 | 113 | 271 | 450 |
| 单质沸点/°C | -183 | 444.6 | 685 | 1390 |
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
回答下列问题:
(1)碲(Te)的氧化物分子式是
(2)硒酸与碲酸酸性较强的是
(3)比较键能:H—S
(4)氢硒酸放在空气中,可能发生反应的化学方程式为
(5)下图所示为 VIA 族元素单质与 H2反应过程中体系温度变化示意图,其中 a、b、c 分别表示VIA 族中某一元素的单质,下图为相同物质的量的单质与 H2反应过程中的体系温度变化。

则:c 代表
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
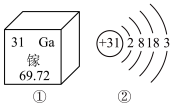
【推荐2】2019年是元素周期表年,镓是门捷列夫曾经预言的金属(类铝)。下图①是镓元素在元素周期表中的部分信息,②是镓原子的结构示意图。请回答:
A.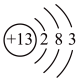 B.
B. 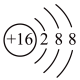 C.
C.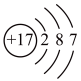 D.
D.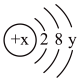
(1)镓原子的核电荷数为_______ ,镓元素的相对原子质量为_______ 。自然界中的镓共有两种稳定的同位素,其中69Ga的丰度为64.0%,则另一种镓的同位素质量数为_______ 。
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是_______ (填元素符号);微粒B的电子式为_______ ,则镓离子与B形成的化合物为_______ (填化学式)。
(3)D为某微粒的结构示意图,已知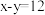 ,则x=
,则x=_______ ;写出C和D组成的化合物在水溶液中的电离方程式:_______ 。
(4)氮化镓(GaN)是第三代半导体材料,一般采用 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为_______ 。

A.
 B.
B.  C.
C. D.
D.
(1)镓原子的核电荷数为
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是
(3)D为某微粒的结构示意图,已知
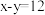 ,则x=
,则x=(4)氮化镓(GaN)是第三代半导体材料,一般采用
 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,回答下列有关问题:
(1)写出元素符号:⑨________ (填化学式,下同)
(2)在这些元素中,最活泼的金属元素是________ ,最活泼的非金属元素是________ 。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是________ ,呈两性的氢氧化物是________ 。
(4)写出③和⑧形成的化合物的电子式__________________ 。
(5)写出④和⑧所构成的化合物的化学键类型__________________ 。
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)写出元素符号:⑨
(2)在这些元素中,最活泼的金属元素是
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是
(4)写出③和⑧形成的化合物的电子式
(5)写出④和⑧所构成的化合物的化学键类型
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)N2的电子式为___________
(2)砷在元素周期表中的位置___________ ,
(3)2017年5月9日,中国科学院发布了113号、115号、117号及118号四种元素的中文名称,其中镆元素的“镆”取自古代剑名“镆铘”,Mc的质子数为___________ 。
(4)已知:含1molP原子的白磷转化为黑磷要放出39.3kJ的能量;转化为红磷要放出17.6kJ的能量;由此推知,其中最稳定的磷单质是___________ 。(填物质名称)
(5)氮和磷氢化物性质的比较:热稳定性:NH3___________ PH3(填“>”或“<”),沸点:N2H4___________ P2H4(填“>”或“<”)
(6)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似,写出PH3与HI反应产物的电子式___________ 。
(1)N2的电子式为
(2)砷在元素周期表中的位置
(3)2017年5月9日,中国科学院发布了113号、115号、117号及118号四种元素的中文名称,其中镆元素的“镆”取自古代剑名“镆铘”,Mc的质子数为
(4)已知:含1molP原子的白磷转化为黑磷要放出39.3kJ的能量;转化为红磷要放出17.6kJ的能量;由此推知,其中最稳定的磷单质是
(5)氮和磷氢化物性质的比较:热稳定性:NH3
(6)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似,写出PH3与HI反应产物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。根据下表中短周期元素的原子半径和主要化合价,回答表后的问题。
(1)上述元素中与元素⑧处于同一周期的有______________________ (填元素符号)
(2)元素①在元素周期表中的位置是_______________________
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为__________________ (填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:_________________________ 。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
-2 | -3 | -1 | -3 |
(1)上述元素中与元素⑧处于同一周期的有
(2)元素①在元素周期表中的位置是
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为
(4)请写出下列元素形成的常见化合物的电子式:
③⑤
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已知A、D位于同一主族,D是短周期中原子半径最大的。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是___________ (用元素符号填写)。
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写)。
(3)下列事实能说明G元素的非金属性比F元素的非金属性强的是(填序号)______
A.G单质与Na2S溶液反应溶液变浑浊
B.F的氢化物的酸性比G的氢化物酸性弱
C.G和F两元素的简单氢化物受热分解,前者的分解温度高
(4)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是___________ 。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是
(3)下列事实能说明G元素的非金属性比F元素的非金属性强的是(填序号)
A.G单质与Na2S溶液反应溶液变浑浊
B.F的氢化物的酸性比G的氢化物酸性弱
C.G和F两元素的简单氢化物受热分解,前者的分解温度高
(4)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素周期律的发现和元素周期表的诞生,开创了化学科学的新纪元。
Ⅰ.2019年是门捷列夫提出元素周期表150周年。下表为元素周期表的一部分,回答下列问题。
(1)中国青年化学家、北京大学教授雷晓光被国际组织推选为“元素④代言人”,④与①能形成10e-分子,用电子式表示该分子的形成过程:_______ 。
(2)⑤⑥⑧⑨中形成的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)用一个化学反应证明元素③比元素⑦的得电子能力强,该反应的离子方程式为_______ 。
II.短周期元素X、Y、Z原子序数依次增大,其中Y元素的一种同位素可用于文物年代的断定,且其最外层电子数等于X、Z最外层电子总和的一半。Y、Z可形成YZ4型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:
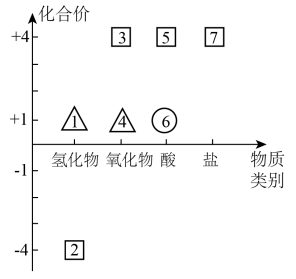
注:△、☐、○分别表示X、Y、Z形成的化合物。回答下列问题:
(4)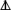 的化学式为
的化学式为_______ 。X在空气中燃烧可获得 ,与X相邻的同主族金属元素Q在空气中燃烧可获得
,与X相邻的同主族金属元素Q在空气中燃烧可获得_______ (填化学式);由此可判断,X、Q金属性较强的是_______ (填元素符号)。
(5)用合适的方程式证明 的酸性强于⑥
的酸性强于⑥_______ ,依据该事实_______ (填“能”或“不能”)判断出Y、Z的非金属性强弱,理由是_______ 。
(6)燃料电池是一种高效、环境友好的供电装置,下图是以 为燃料的电池工作原理示意图,a、b均为石墨电极。
为燃料的电池工作原理示意图,a、b均为石墨电极。
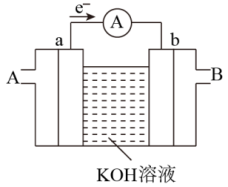
A口通入的气体为_______ (填化学式)。
Ⅰ.2019年是门捷列夫提出元素周期表150周年。下表为元素周期表的一部分,回答下列问题。
| IA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)⑤⑥⑧⑨中形成的简单离子半径由大到小的顺序是
(3)用一个化学反应证明元素③比元素⑦的得电子能力强,该反应的离子方程式为
II.短周期元素X、Y、Z原子序数依次增大,其中Y元素的一种同位素可用于文物年代的断定,且其最外层电子数等于X、Z最外层电子总和的一半。Y、Z可形成YZ4型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:

注:△、☐、○分别表示X、Y、Z形成的化合物。回答下列问题:
(4)
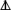 的化学式为
的化学式为 ,与X相邻的同主族金属元素Q在空气中燃烧可获得
,与X相邻的同主族金属元素Q在空气中燃烧可获得(5)用合适的方程式证明
 的酸性强于⑥
的酸性强于⑥(6)燃料电池是一种高效、环境友好的供电装置,下图是以
 为燃料的电池工作原理示意图,a、b均为石墨电极。
为燃料的电池工作原理示意图,a、b均为石墨电极。
A口通入的气体为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】国家卫生健康委员会发布公告称,富硒酵母、二氧化硅、硫黄等6种食品添加剂新品种安全性已通过审查,这些食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂,用于食品生产中,将更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为____ 。
(2)下列说法正确的是____ 。
A.热稳定性: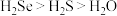 B.
B.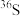 与
与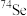 的中子数之和为60
的中子数之和为60
C.酸性: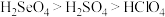 D.还原性:
D.还原性: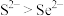
(3)短周期元素 、
、 、
、 、
、 、
、 、
、 都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示: 、
、 、
、 三种元素组成的化合物的电子式为
三种元素组成的化合物的电子式为____ 。
② 、
、 、
、 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是___ (用化学式表示),其结构示意图为___ 。
③ 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是____ (填化学式),此化合物可将碱性工业废水中的 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为____ 。
(1)富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为
(2)下列说法正确的是
A.热稳定性:
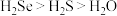 B.
B.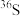 与
与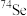 的中子数之和为60
的中子数之和为60C.酸性:
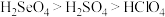 D.还原性:
D.还原性: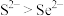
(3)短周期元素
 、
、 、
、 、
、 、
、 、
、 都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示: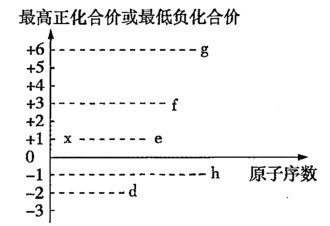
 、
、 、
、 三种元素组成的化合物的电子式为
三种元素组成的化合物的电子式为②
 、
、 、
、 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是③
 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素,D的原子半径在同周期元素中最小。
(1)A的元素符号____________ 。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是_____________ 。
(3)A、B形成的某化合物能与CO2发生氧化还原反应。每消耗1 mol CO2,转移的电子数为_________________________ 。
(4)B的最高价氧化物对应的水化物与D元素的单质在水溶液中反应的化学方程式是________________________________________ 。
(1)A的元素符号
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是
(3)A、B形成的某化合物能与CO2发生氧化还原反应。每消耗1 mol CO2,转移的电子数为
(4)B的最高价氧化物对应的水化物与D元素的单质在水溶液中反应的化学方程式是
您最近一年使用:0次



