国家卫生健康委员会发布公告称,富硒酵母、二氧化硅、硫黄等6种食品添加剂新品种安全性已通过审查,这些食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂,用于食品生产中,将更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为____ 。
(2)下列说法正确的是____ 。
A.热稳定性: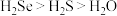 B.
B.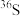 与
与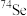 的中子数之和为60
的中子数之和为60
C.酸性: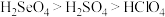 D.还原性:
D.还原性: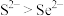
(3)短周期元素 、
、 、
、 、
、 、
、 、
、 都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示: 、
、 、
、 三种元素组成的化合物的电子式为
三种元素组成的化合物的电子式为____ 。
② 、
、 、
、 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是___ (用化学式表示),其结构示意图为___ 。
③ 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是____ (填化学式),此化合物可将碱性工业废水中的 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为____ 。
(1)富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为
(2)下列说法正确的是
A.热稳定性:
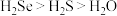 B.
B.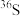 与
与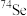 的中子数之和为60
的中子数之和为60C.酸性:
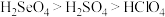 D.还原性:
D.还原性: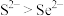
(3)短周期元素
 、
、 、
、 、
、 、
、 、
、 都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示: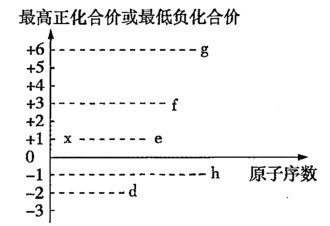
 、
、 、
、 三种元素组成的化合物的电子式为
三种元素组成的化合物的电子式为②
 、
、 、
、 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是③
 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为
更新时间:2020-09-06 09:50:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】我国科学家成功合成了含N 的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
(1)N在元素周期表中的位置是______ 。
(2)N 中,N原子之间的相互作用是
中,N原子之间的相互作用是______ (填“离子键”或“共价键”)。
(3)非金属性O强于N,用原子结构解释原因:______ ,得电子能力O大于N。
(4)砷(As)与氮位于同一主族,下列推断正确的是______ (填序号)。
① 砷元素的最低负化合价为−3价 ② 热稳定性:AsH3>NH3 ③ 砷的最高价氧化物对应的水化物属于酸
 的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。(1)N在元素周期表中的位置是
(2)N
 中,N原子之间的相互作用是
中,N原子之间的相互作用是(3)非金属性O强于N,用原子结构解释原因:
(4)砷(As)与氮位于同一主族,下列推断正确的是
① 砷元素的最低负化合价为−3价 ② 热稳定性:AsH3>NH3 ③ 砷的最高价氧化物对应的水化物属于酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素①~⑧在元素周期表中的位置如下,回答有关问题:

(1)写出⑦元素名称_____ ,画出⑥的离子结构示意图__________ ;写出②含有10个中子的核素的化学符号_________ 。
(2)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为_______________ 。(用化学式表示,下同)
(3)②③⑥元素氢化物的稳定性由强到弱的顺序为________ (填化学式)。
(4)表中能形成两性氢氧化物的元素是_______ (填元素符号)
(5)由②④⑥三种元素组成的一种盐在空气中放置会变质,请用化学方程式表示变质的反应____________________________________ 。
(6)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由_______________ 。

(1)写出⑦元素名称
(2)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为
(3)②③⑥元素氢化物的稳定性由强到弱的顺序为
(4)表中能形成两性氢氧化物的元素是
(5)由②④⑥三种元素组成的一种盐在空气中放置会变质,请用化学方程式表示变质的反应
(6)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)原子序数11-17的元素,自钠到氯,电子层数相同,最外层电子数从_______ 增加到_______ ,随着核电荷数依次递增,原子半径依次_______ ,核对外层电子的引力逐渐_______ ,失电子能力逐渐_______ ,得电子能力逐渐_______ ,因此,金属性逐渐_______ ,非金属性逐渐_______ 。
(2)元素金属性的强弱,可以从它的单质及水或酸反应置换氢的_______ 程度,以及它的最高价氧化物的水化物的_______ 强弱来判断。元素非金属性的强弱,可以从它的最高价氧化物的水化物的_______ 强弱,或它的单质跟H2生成气态氢化物的_______ 及氢化物的_______ 来判断。
(2)元素金属性的强弱,可以从它的单质及水或酸反应置换氢的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸工厂的酸性废水中砷(As)元素(主要以H3AsO3形式存在)含量极高,为控制砷的排放,某工厂采用化学沉降法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多2个电子层,砷在元素周期表的位置为____________ ,AsH3的稳定性比NH3的稳定性_________ (填“强”或“弱”)。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反应的离子方程式为_____________ 。
(2)电镀厂的废水中含有的CN-有剧毒,需要处理加以排放。
①已知HCN为一元弱酸,则NaCN溶液的pH_______ 7(填“>”、“=”或“<”)。
②处理含CN -废水的方法之一是在微生物的作用下,CN -被氧气氧化成 ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为________________ 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A—表示乳酸根离子)。
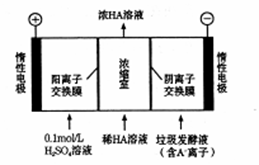
①阳极的电极反应式为_____________ 。
②简述浓缩室中得到浓乳酸的原理___________________________ 。
③电解过程中,采取一定的措施可控制阴极室的pH约为6~8,此时加入浓缩室的OH—可忽略不计。400mL10g/L的乳酸溶液通电一段时间后,浓度上升为145g/L(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为____ L(乳酸的摩尔质量为90g/mol)。
(1)硫酸工厂的酸性废水中砷(As)元素(主要以H3AsO3形式存在)含量极高,为控制砷的排放,某工厂采用化学沉降法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多2个电子层,砷在元素周期表的位置为
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反应的离子方程式为
(2)电镀厂的废水中含有的CN-有剧毒,需要处理加以排放。
①已知HCN为一元弱酸,则NaCN溶液的pH
②处理含CN -废水的方法之一是在微生物的作用下,CN -被氧气氧化成
 ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A—表示乳酸根离子)。

①阳极的电极反应式为
②简述浓缩室中得到浓乳酸的原理
③电解过程中,采取一定的措施可控制阴极室的pH约为6~8,此时加入浓缩室的OH—可忽略不计。400mL10g/L的乳酸溶液通电一段时间后,浓度上升为145g/L(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】图是元素周期表的一部分,回答下列有关问题:
(1)写出⑫的元素符号:_______ ,其原子序数为_______ 。
(2)在这些元素中,非金属性最强的元素是_______ (用元素符号填答)。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应的化学方程式_______ 。
(4)在④⑤⑦⑧形成的四个简单离子中,离子 半径由大到小的顺序是(用离子符号和“>”填答)_______
(5)设计一种简单实验确认④与⑤中,哪个金属性更强(只要写出实验方案即可),写出实验方案并预测结论:_______ ;
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)写出⑫的元素符号:
(2)在这些元素中,非金属性最强的元素是
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应的化学方程式
(4)在④⑤⑦⑧形成的四个简单离子中,
(5)设计一种简单实验确认④与⑤中,哪个金属性更强(只要写出实验方案即可),写出实验方案并预测结论:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】摩擦剂是牙膏的主体成分, 是一种常见的摩擦剂.
是一种常见的摩擦剂.
(1) 在元素周期表中的位置是
在元素周期表中的位置是_____________ .
(2)根据用途推测 在水中的溶解性:
在水中的溶解性:_____________ (填“易溶”或“难溶”).
(3)制备 的方法如下:
的方法如下:

①写出反应Ⅰ的离子方程式________________________ .
②比较酸性强弱:
_____________  (填“>”或“<”).
(填“>”或“<”).
③结合原子结构解释②中酸性关系: 和S电子层数相同,
和S电子层数相同,__________________________ .
(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡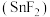 .
.
已知锡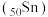 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是_____________ (填序号).
a. 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大
c. 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸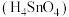 的酸性强于硅酸
的酸性强于硅酸
(5)工业上可以用木炭还原 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:_____________ ;该反应能否验证 和C的非金属性强弱?
和C的非金属性强弱?_____________ (填“能”、“不能”)
(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?_____________ (填“同意”、“不同意”);
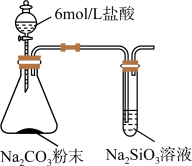
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案._____________
 是一种常见的摩擦剂.
是一种常见的摩擦剂.(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)根据用途推测
 在水中的溶解性:
在水中的溶解性:(3)制备
 的方法如下:
的方法如下:
①写出反应Ⅰ的离子方程式
②比较酸性强弱:

 (填“>”或“<”).
(填“>”或“<”).③结合原子结构解释②中酸性关系:
 和S电子层数相同,
和S电子层数相同,(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡
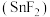 .
.已知锡
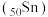 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是a.
 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大c.
 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸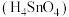 的酸性强于硅酸
的酸性强于硅酸(5)工业上可以用木炭还原
 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为: 和C的非金属性强弱?
和C的非金属性强弱?(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与
 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】为中学常见的单质或化合物,其相互转化关系如图甲所示
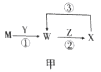

(1)若M为短周期金属单质,W、X均为含M元素的盐,且W溶液的pH<7.请指出Y物质的类别:_____________ ;并写出W溶液pH>7的离子方程式:_____________ ;写出反应③的离子方程式:_____________ 。
(2)若M是浅黄色化合物,常温下Y是无色气体;X中含有的阴、阳离子均为10电子粒子,则X中所含化学键的类型是_____________ ;将一定量的气体Y通入2LX的溶液中,向所得溶液中边逐滴加入稀盐酸,边振荡至过量,产生的气体与盐酸物质的量的关系如图乙(忽略气体的溶解和氯化氢的挥发)。请回答:O点溶液中所含溶质的化学式为_____________ ,a点溶液中各离子浓度由大到小的关系是_____________ 。
(3)若将(2)中的气体Y通入氢氧化钡溶液中得到不溶物N,N的Ksp=8.1×10-9.现将该沉淀放入0.1-1的BaCl2溶液中,其Ksp_____________ (填“增大”、“减小”或“不变”),组成不溶物N的阴离子在溶液中的浓度为_____________ mol/L。


(1)若M为短周期金属单质,W、X均为含M元素的盐,且W溶液的pH<7.请指出Y物质的类别:
(2)若M是浅黄色化合物,常温下Y是无色气体;X中含有的阴、阳离子均为10电子粒子,则X中所含化学键的类型是
(3)若将(2)中的气体Y通入氢氧化钡溶液中得到不溶物N,N的Ksp=8.1×10-9.现将该沉淀放入0.1-1的BaCl2溶液中,其Ksp
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】部分短周期元素的原子半径与元素的最高价及最低价的关系如图所示。
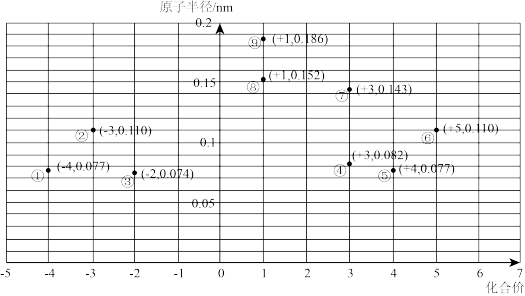
请填写下列空白:
(1)图中涉及________ 种元素,其中元素________ (用化学用语表示,下同 )的金属性最强。
(2)元素①的最简单氢化物的电子式为________ ;元素②的原子结构示意图为________ 。
(3)元素③和⑨对应的单质加热条件下反应的方程式为________________ 。
(4)元素④在周期表中的位置是________________ ;元素⑤、⑥对应的最高价氧化物的水化物酸性强弱关系为________ ;元素⑦和元素⑧两者核电荷数之差是________ 。

请填写下列空白:
(1)图中涉及
(2)元素①的最简单氢化物的电子式为
(3)元素③和⑨对应的单质加热条件下反应的方程式为
(4)元素④在周期表中的位置是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、
E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。
A原子的最外层电子数比次外层电子层多3个。D周期序数等于D原子最外层电子数。
E原子半径是同周期中最小的(除稀有气体外)根据以上信息回答下列问题:
(1)A元素在周期表中的位置_____________________ ;
(2)乙物质中存在的化学键类型是_________________ ;
(3)写出C与D的最高价氧化物对应的水化物相互间反应的离子方程式____________ ;
(4)E的单质通入C的最高价氧化物对应的水化物的溶液中反应生成的“84”消毒液的有效成分的化学式为_________ 。
E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。
A原子的最外层电子数比次外层电子层多3个。D周期序数等于D原子最外层电子数。
E原子半径是同周期中最小的(除稀有气体外)根据以上信息回答下列问题:
(1)A元素在周期表中的位置
(2)乙物质中存在的化学键类型是
(3)写出C与D的最高价氧化物对应的水化物相互间反应的离子方程式
(4)E的单质通入C的最高价氧化物对应的水化物的溶液中反应生成的“84”消毒液的有效成分的化学式为
您最近一年使用:0次



