下列解释实验现象的反应方程式正确的是
| A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2=Na2O2 |
| B.向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2- =Ag2S↓+2Cl- |
| C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+CO2=2Na2CO3+O2 |
| D.FeCl2溶液中滴加NaClO溶液生成红褐色沉淀:2Fe2+ + ClO- + 5H2O= 2Fe(OH)3↓+Cl-+ 4H+ |
17-18高二下·辽宁盘锦·期末 查看更多[2]
更新时间:2018-07-26 16:25:54
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下列离子方程式书写正确的是
| A.钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ |
| B.铁粉投入到硫酸铜溶液中: Fe +Cu2+=Fe2++Cu |
| C.AlCl3溶液中加入足量的氨水: Al3++ 3OH-= Al(OH)3↓ |
| D.澄清石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列离子反应方程式正确的是
| A.向NH4HCO3溶液中加过量的NaOH溶液:NH4++OH-=NH3↑+H2O |
| B.将氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
| C.在碳酸氢镁溶液中加入足量Ca(OH)2溶液: Mg2++HCO3-+Ca2++2OH-===MgCO3↓+CaCO3↓+2H2O |
| D.向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全Al3++SO42-+Ba2++3OH-===BaSO4↓+Al(OH)3↓ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】近日,中科院上海硅酸盐研究所施剑林团队报道了MnOOH催化谷胱甘肽自氧化产生活性氧。某小组以菱锰矿(主要成分为 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下:
②几种金属离子沉淀的pH如表所示:
下列叙述正确的是
 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下: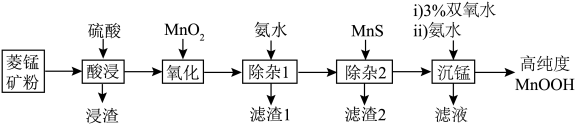
②几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 4.0 | 7.6 | 8.1 |
| 完全沉淀的pH | 3.7 | 9.6 | 5.2 | 9.2 | 10.1 |
A.滤渣1的成分是 和 和 |
B.“氧化”反应的离子方程式为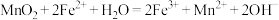 |
C.“除杂2”的原理是 |
D.双氧水氧化 ,滤液一定显酸性 ,滤液一定显酸性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,有pH=1的某溶液中可能含有Na+、Fe3+、Fe2+、I-、Cl-、 中的某几种,现取100 mL该溶液进行如图实验:根据实验结果,下列判断正确的是
中的某几种,现取100 mL该溶液进行如图实验:根据实验结果,下列判断正确的是

 中的某几种,现取100 mL该溶液进行如图实验:根据实验结果,下列判断正确的是
中的某几种,现取100 mL该溶液进行如图实验:根据实验结果,下列判断正确的是
| A.Fe3+与Fe2+至少有一种 |
B.不能确定Na+和Cl-是否存在, 一定不存在 一定不存在 |
| C.Fe2+,I-、Cl-三种离子一定存在 |
| D.由于通入了氯气,加入硝酸银产生沉淀不能确定溶液中一定有Cl- |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列实验方案设计正确的是
| 编号 | 目的 | 方案设计 |
| A | 检验固体试样中有 | 在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体试样中不可能存在 |
| B | 探究S与Cl的金属性强弱 | 向NaHS溶液中滴入稀盐酸,观察是否有生成臭鸡蛋气味气体( )。 )。 |
| C | 探究浓度对化学反应速率的影响 | 向两支试管分别加入 和 和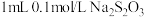 溶液,向盛有 溶液,向盛有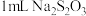 溶液试管中加入 溶液试管中加入 蒸馏水,再同时向两支试管中加 蒸馏水,再同时向两支试管中加 ,收集生成的 ,收集生成的 气体,比较生成气体的多少 气体,比较生成气体的多少 |
| D | 探究 的还原性 的还原性 | 在试管中加入少量酸性 溶液,然后向试管中逐滴加入 溶液,然后向试管中逐滴加入 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】下列离子方程式中,不正确的是
| A.等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使 -完全沉淀:2Ba2+ + 4OH- + Al3+ + 2SO42-= 2BaSO4↓+ AlO2- + 2H2O -完全沉淀:2Ba2+ + 4OH- + Al3+ + 2SO42-= 2BaSO4↓+ AlO2- + 2H2O |
| C.向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2+ + 2HCO-3 + 4OH- = Mg(OH)2↓+ 2CO32-+ 2H2O |
| D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2+ + 4H+ + NO3-= 3Fe3+ + NO↑+ 2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】下列实验方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究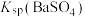 和 和 大小 大小 | 室温下,向浓度均为 的 的 和 和 混合溶液中滴加 混合溶液中滴加 溶液 溶液 | 出现白色沉淀,说明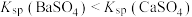 |
| B | 比较 、 、 结合 结合 能力的大小 能力的大小 | 室温下,用pH试纸分别测量0.1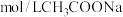 溶液和 溶液和 溶液的pH 溶液的pH | 测得 溶液和NaCN溶液的pH分别为9和11,说明 溶液和NaCN溶液的pH分别为9和11,说明 结合 结合 的能力更强 的能力更强 |
| C | 探究浓度对平衡的影响 | 向试管中加入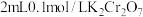 溶液,滴加5~10滴 溶液,滴加5~10滴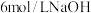 溶液 溶液 | 溶液由黄色变为橙色,说明加入氢氧化钠溶液后平衡向生成 的方向移动 的方向移动 |
| D | 验证铁的吸氧腐蚀 | 将除锈后的铁钉用浓盐酸浸泡后,放入连有导管的具支试管中,塞上橡胶塞,将导管末端浸入水中 | 几分钟后,导管中水柱上升,说明铁发生了吸氧腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列由实验操作及现象能够得出相应结论的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向ZnS(白色)悬浊液中加入少量 溶液,有黑色沉淀(CuS)生成 溶液,有黑色沉淀(CuS)生成 | 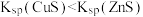 |
| B | 将石灰石与盐酸反应产生的气体直接通入水玻璃中,生成白色沉淀 | 非金属性: |
| C | 向盛有 溶液的试管中边滴入 溶液的试管中边滴入 水溶液边振荡,有白色沉淀生成 水溶液边振荡,有白色沉淀生成 | 生成的白色沉淀为 |
| D | 取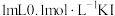 溶液,加入 溶液,加入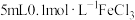 溶液,加入 溶液,加入 萃取分液后,向水层滴入 萃取分液后,向水层滴入 溶液,溶液变成红色 溶液,溶液变成红色 |  与 与 所发生的反应为可逆反应 所发生的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



