实验室现需配制物质的量浓度为1mol•L﹣1的NaOH溶液480mL。
(1)配制该溶液的实验步骤包括:
a.计算需要氢氧化钠固体的质量;
b.称量氢氧化钠固体;
c.将烧杯中的溶液注入________ ;
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却;
e.盖好瓶塞,反复上下颠倒摇匀;
f.继续向容量瓶中加蒸馏水至刻度线下________ 时,改用________ 滴加蒸馏水至凹液面与刻度线相切。
②上述步骤的正确操作顺序是________ 。
(2)要配制此溶液,需要称量NaOH固体的质量为________ 克。
(3)下列操作会使所配制溶液浓度偏大的有_______ 。
A、溶解固体溶质时,未冷却至室温即转入容量瓶进行定容
B、定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线
C、容量瓶中原有少量蒸馏水
D、定容时观察液面仰视
(4)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请用化学方程式解释原因__________________________ 。
(1)配制该溶液的实验步骤包括:
a.计算需要氢氧化钠固体的质量;
b.称量氢氧化钠固体;
c.将烧杯中的溶液注入
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却;
e.盖好瓶塞,反复上下颠倒摇匀;
f.继续向容量瓶中加蒸馏水至刻度线下
②上述步骤的正确操作顺序是
(2)要配制此溶液,需要称量NaOH固体的质量为
(3)下列操作会使所配制溶液浓度偏大的有
A、溶解固体溶质时,未冷却至室温即转入容量瓶进行定容
B、定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线
C、容量瓶中原有少量蒸馏水
D、定容时观察液面仰视
(4)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请用化学方程式解释原因
更新时间:2018-09-03 14:54:09
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】现有质量分数为98%、密度为1.84g·cm-3的浓硫酸来配制500mL、0.2mol·L-1的稀硫酸。可提供选择的仪器有:①玻璃棒;②烧瓶;③烧杯;④胶头滴管;⑤量筒;⑥容量瓶;⑦托盘天平;⑧药匙。请回答下列问题:
(1)上述仪器中,在配制500mL、0.2mol·L-1的稀硫酸时用不到的有___________ (填代号)。
(2)经计算,需浓硫酸的体积为___________ mL。
(3)将浓硫酸加适量蒸馏水稀释后,冷却片刻,随后全部转移到___________ mL的容量瓶中,转移时应用玻璃棒引流。转移完毕后,用少量蒸馏水洗涤___________ 2~3次,加蒸馏水到瓶颈刻度1-2cm的地方改用胶头滴管滴加,使溶液的___________ ,振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,下列操作中:错误的是___________ ,能引起所配制溶液浓度偏低的有___________ (填代号)。
A.定容时,仰视刻度线
B.洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
C.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
D.转移前,容量瓶中含有少量蒸馏水
E.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
F.将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
G.未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
(1)上述仪器中,在配制500mL、0.2mol·L-1的稀硫酸时用不到的有
(2)经计算,需浓硫酸的体积为
(3)将浓硫酸加适量蒸馏水稀释后,冷却片刻,随后全部转移到
(4)在配制过程中,其他操作都准确,下列操作中:错误的是
A.定容时,仰视刻度线
B.洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
C.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
D.转移前,容量瓶中含有少量蒸馏水
E.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
F.将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
G.未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】现用18.4 mol/L的浓H2SO4来配制500 mL 0.2 mol/L的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥托盘天平 ⑦药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时不需要使用的有___________ (填代号),还缺少的仪器是______________________ 。
(2)经计算,需浓H2SO4的体积为___________ ,量取浓硫酸时应选用___________ (选填①10 mL、②50 mL、③100 mL三种规格)的量筒。
(3)将所配制的稀H2SO4进行测定,发现浓度大于0.2 mol/L。请你分析配制过程中可能引起浓度偏高的原因_____________________ (多选题)
A.定容时液面低于刻度线
B.未冷却到室温就定容
C.定容时液面高于刻度线
D.量取浓硫酸时俯视读数
(1)上述仪器中,在配制稀H2SO4时不需要使用的有
(2)经计算,需浓H2SO4的体积为
(3)将所配制的稀H2SO4进行测定,发现浓度大于0.2 mol/L。请你分析配制过程中可能引起浓度偏高的原因
A.定容时液面低于刻度线
B.未冷却到室温就定容
C.定容时液面高于刻度线
D.量取浓硫酸时俯视读数
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某次实验中预计需要使用480mL0.1mol/L的纯碱溶液,如图是某同学在实验室配制该溶液的流程图,回答下列问题:_______ 。
(2)本次配制应选择的最主要仪器为______ (只写1个)。
(3)指出所给流程图中的操作有两个明显的不正确,请简要描述出不正确点:_______ 。
(4)在配制上述溶液实验中,下列操作引起所配纯碱溶液浓度偏低的有_______ 。
(5)下列说法错误的是_______ 。

(2)本次配制应选择的最主要仪器为
(3)指出所给流程图中的操作有两个明显的不正确,请简要描述出不正确点:
(4)在配制上述溶液实验中,下列操作引起所配纯碱溶液浓度偏低的有
| A.砝码生锈 |
| B.在烧杯中溶解搅拌时,溅出少量溶液 |
| C.没有用蒸馏水洗涤烧杯2~3次,并将洗液移入容量瓶中 |
| D.容量瓶中原来存有少量蒸馏水 |
(5)下列说法错误的是
| A.通常容量瓶上有温度、规格(体积)、0刻线,这三个标识 |
| B.容量瓶使用前要先检查气密性,然后再清洗、烘干 |
| C.定容时加水超过刻度线,需要重新配制 |
| D.振荡摇匀后发现液面低于刻度线,必须重新配制 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】实验室用NaOH固体配制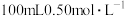 的NaOH溶液,填空并请回答下列问题:
的NaOH溶液,填空并请回答下列问题:
(1)配制 的NaOH溶液,应称取NaOH的质量
的NaOH溶液,应称取NaOH的质量___________ g,需要的仪器有___________ 、___________ 、量筒、胶头滴管、玻璃棒、托盘天平(带砝码)、药匙。
(2)容量瓶上需标有以下五项中的___________ ;
①温度②容量③浓度④刻度线⑤压强
(3)实验用到玻璃棒,其作用分别是:___________ 、___________ ;
(4)溶液配制时,一般可分为以下几个步骤:
①摇匀②转移③洗涤④定容⑤冷却
正确的操作顺序为(必要时可重复):
计算、称量、溶解___________ 装瓶、贴标签;
(5)下列配制的溶液浓度偏低的是___________ ;
A.称量NaOH时,将NaOH放在纸上称重
B.定容时俯视刻度线
C.配制前,容量瓶中有少量蒸馏水
D.配制时,NaOH未冷却直接定容
E.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
F.加蒸馏水时不慎超过了刻度线
(6)某同学用该氢氧化钠溶液去中和20.00mL未知浓度的盐酸,恰好消耗氢氧化钠溶液18.00mL,则盐酸的物质的量浓度为___________ 。
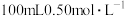 的NaOH溶液,填空并请回答下列问题:
的NaOH溶液,填空并请回答下列问题:(1)配制
 的NaOH溶液,应称取NaOH的质量
的NaOH溶液,应称取NaOH的质量(2)容量瓶上需标有以下五项中的
①温度②容量③浓度④刻度线⑤压强
(3)实验用到玻璃棒,其作用分别是:
(4)溶液配制时,一般可分为以下几个步骤:
①摇匀②转移③洗涤④定容⑤冷却
正确的操作顺序为(必要时可重复):
计算、称量、溶解
(5)下列配制的溶液浓度偏低的是
A.称量NaOH时,将NaOH放在纸上称重
B.定容时俯视刻度线
C.配制前,容量瓶中有少量蒸馏水
D.配制时,NaOH未冷却直接定容
E.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
F.加蒸馏水时不慎超过了刻度线
(6)某同学用该氢氧化钠溶液去中和20.00mL未知浓度的盐酸,恰好消耗氢氧化钠溶液18.00mL,则盐酸的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某同学在实验室欲配制物质的量浓度均为1.0 mol/L的NaOH溶液和稀H2SO4各450mL。提供的试剂是:NaOH固体和98%的浓H2SO4(密度为1.84 g/cm3)及蒸馏水。
(1)配制两种溶液时都需要的玻璃仪器是_______ 。
(2)应用托盘天平称量NaOH_______ g,应用量筒量取浓H2SO4_______ mL。
(3)配制时,先要检查容量瓶是否漏水,其方法是_______ 。
(4)浓硫酸溶于水的正确操作方法是_______ 。
(5)在配制上述溶液实验中,下列操作引起结果偏低的有_______
A.该学生在量取浓硫酸时,俯视刻度线
B.称量固体NaOH时,将砝码和物品的位置颠倒(没有使用游码)
C.溶解H2SO4操作时没有冷却至室温就立即完成后面的配制操作。
D.在烧杯中溶解搅拌时,溅出少量溶液
E.没有用蒸馏水洗烧杯2—3次,并将洗液移入容量瓶中
F.将量筒洗涤2—3次,并全部转移至容量瓶中
G.容量瓶中原来存有少量蒸馏水
H.胶头滴管加水定容时俯视刻度
(1)配制两种溶液时都需要的玻璃仪器是
(2)应用托盘天平称量NaOH
(3)配制时,先要检查容量瓶是否漏水,其方法是
(4)浓硫酸溶于水的正确操作方法是
(5)在配制上述溶液实验中,下列操作引起结果偏低的有
A.该学生在量取浓硫酸时,俯视刻度线
B.称量固体NaOH时,将砝码和物品的位置颠倒(没有使用游码)
C.溶解H2SO4操作时没有冷却至室温就立即完成后面的配制操作。
D.在烧杯中溶解搅拌时,溅出少量溶液
E.没有用蒸馏水洗烧杯2—3次,并将洗液移入容量瓶中
F.将量筒洗涤2—3次,并全部转移至容量瓶中
G.容量瓶中原来存有少量蒸馏水
H.胶头滴管加水定容时俯视刻度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
(1)在如图所示仪器中,配制上述溶液肯定不需要的是________________ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是______________________ 。
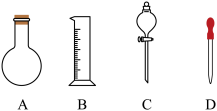
(2)在容量瓶的使用方法中,下列操作不正确的是_____________________ 。
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称量NaOH固体__________ g。称量NaOH固体需注意选择用___________________ 盛装NaOH固体。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度____________ 0.1mol/L(填“大于”、“小于”或“等于”)。
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为____ mL,如果实验室有15mL、20mL、50mL量筒,应选用___ mL量筒最好。
(1)在如图所示仪器中,配制上述溶液肯定不需要的是

(2)在容量瓶的使用方法中,下列操作不正确的是
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称量NaOH固体
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL、0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有________________________ (填代号)。
(2)经计算,需浓H2SO4的体积为_________________ mL。
(3)将浓H2SO4加适量蒸馏水稀释后,冷却片刻,随后全部转移到500mL的容量瓶中,转移时应用________________ 引流。转移完毕,用少量蒸馏水洗涤烧杯2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度1 cm~2 cm处。改用_______________ 加蒸馏水到瓶颈刻度的地方,使溶液的凹面正好跟刻度线相平。振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,下列操作中:错误的是_________ ,能引起误差偏高的有__________ (填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑦定容时,俯视刻度线
(1)上述仪器中,在配制稀H2SO4时用不到的有
(2)经计算,需浓H2SO4的体积为
(3)将浓H2SO4加适量蒸馏水稀释后,冷却片刻,随后全部转移到500mL的容量瓶中,转移时应用
(4)在配制过程中,其他操作都准确,下列操作中:错误的是
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑦定容时,俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室需要配制0.5 mol/L的烧碱溶液450mL,根据溶液配制的过程,回答下列问题:
(1)实验中除了托盘天平(带砝码)、药匙、量筒和玻璃棒外,还需要的其他玻璃仪器有:____________ 。
(2)根据计算得知,所需NaOH固体的质量为___________ g。
(3)配制溶液的过程中,有以下操作,其中正确的是_________ (填代号)。
A.将氢氧化钠固体放在纸片上称量
B.在烧杯中溶解氧氧化钠固体后,立即将溶液倒入容量瓶中
C.将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中
(4)玻璃捧在该实验中的作用有:①__________ ,②____________ 。
(1)实验中除了托盘天平(带砝码)、药匙、量筒和玻璃棒外,还需要的其他玻璃仪器有:
(2)根据计算得知,所需NaOH固体的质量为
(3)配制溶液的过程中,有以下操作,其中正确的是
A.将氢氧化钠固体放在纸片上称量
B.在烧杯中溶解氧氧化钠固体后,立即将溶液倒入容量瓶中
C.将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中
(4)玻璃捧在该实验中的作用有:①
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】向AgNO3溶液中逐滴加入某盐酸(少量)。充分反应后,过滤,所得滤液质量与原AgNO3溶液质量相同。试回答下列问题:
(1)请写出发生反应的化学方程式:___ 。
(2)实验室欲用10.0mol/L的盐酸配制450mL0.1mol/L的盐酸,则在实验过程中需要使用的玻璃仪器有___ 。
(3)下列操作会使所配制的溶液中溶质的物质的量浓度偏高的是___ (填字母)。
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.定容时仰视刻度线
C.定容时俯视刻度线
D.定容后摇匀,发现液面低于刻度线,再滴加几滴水至刻度线
E.使用前容量瓶底部有少量蒸馏水
F.稀释后,未冷却就立刻转移至容量瓶中
(1)请写出发生反应的化学方程式:
(2)实验室欲用10.0mol/L的盐酸配制450mL0.1mol/L的盐酸,则在实验过程中需要使用的玻璃仪器有
(3)下列操作会使所配制的溶液中溶质的物质的量浓度偏高的是
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.定容时仰视刻度线
C.定容时俯视刻度线
D.定容后摇匀,发现液面低于刻度线,再滴加几滴水至刻度线
E.使用前容量瓶底部有少量蒸馏水
F.稀释后,未冷却就立刻转移至容量瓶中
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】现用98%的浓硫酸(ρ=1.84 g/cm3)配制浓度为3.68mol/L的稀硫酸100mL,并利用所配得的溶液进行相关实验。
(1)该同学准备的实验用品有:量筒、烧杯、玻璃棒、胶头滴管,还缺少的玻璃仪器是_____________ 。
(2)正确的实验操作顺序为______ → → → → → 。(填选项字母编号)
A.用量筒量取浓H2SO4 B.反复颠倒摇匀 C.用胶头滴管加水至刻度
D.洗涤所用仪器并转移洗涤液 E.稀释浓H2SO4 F.将溶液转入容量瓶
(3)原浓硫酸溶液的物质的量浓度是_________ ,配制过程所需浓硫酸的体积为_________ mL
(4)配制过程的下列操作会引起所得溶液的浓度偏低的是________________ 。(填选项字母编号)
A.定容时俯视读数 B.量取浓硫酸的量筒有少量的水分
C.未冷却至室温就注水定容 D.原浓硫酸溶液敞口放置很长时间
(5)取25ml所配得的硫酸溶液与浓度为4mol/L的BaCl2混合,请设计一个简单的方案证明混合液中还含有硫酸根离子:________________________________________________ 。
(1)该同学准备的实验用品有:量筒、烧杯、玻璃棒、胶头滴管,还缺少的玻璃仪器是
(2)正确的实验操作顺序为
A.用量筒量取浓H2SO4 B.反复颠倒摇匀 C.用胶头滴管加水至刻度
D.洗涤所用仪器并转移洗涤液 E.稀释浓H2SO4 F.将溶液转入容量瓶
(3)原浓硫酸溶液的物质的量浓度是
(4)配制过程的下列操作会引起所得溶液的浓度偏低的是
A.定容时俯视读数 B.量取浓硫酸的量筒有少量的水分
C.未冷却至室温就注水定容 D.原浓硫酸溶液敞口放置很长时间
(5)取25ml所配得的硫酸溶液与浓度为4mol/L的BaCl2混合,请设计一个简单的方案证明混合液中还含有硫酸根离子:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】欲配制0.2mol/L 的NaOH溶液980mL,有以下仪器:
①烧杯②漏斗③托盘天平(带砝码)④玻璃棒⑤胶头滴管
(1)配制时,必须使用的仪器有____________ (填代号),还缺少的玻璃仪器是____________________ 。该实验中两次用到玻璃棒,其作用分别是____________________ ,____________________ 。
(2)使用容量瓶前必须进行的一步操作是_____________________ 。
(3)根据计算应用托盘天平称量NaOH_______ g。
(4)请你分析下列哪些操作会引起所配浓度偏大________ (填写字母)。
A.将NaOH放在滤纸上称量
B.称取NaOH的砝码已生锈
C.容量瓶未干燥即用来配制溶液
D.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容;
E.往容量瓶转移时,有少量液体溅出
F.在容量瓶中定容时视线如图所示
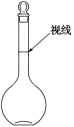
G.烧杯未进行洗涤
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
(5)若定容时不小心使液面超过了刻度线,应采取的措施是_____________
①烧杯②漏斗③托盘天平(带砝码)④玻璃棒⑤胶头滴管
(1)配制时,必须使用的仪器有
(2)使用容量瓶前必须进行的一步操作是
(3)根据计算应用托盘天平称量NaOH
(4)请你分析下列哪些操作会引起所配浓度偏大
A.将NaOH放在滤纸上称量
B.称取NaOH的砝码已生锈
C.容量瓶未干燥即用来配制溶液
D.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容;
E.往容量瓶转移时,有少量液体溅出
F.在容量瓶中定容时视线如图所示

G.烧杯未进行洗涤
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
(5)若定容时不小心使液面超过了刻度线,应采取的措施是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】利用课堂上学到的知识来解决生活中的问题是我们学习的重要目的。
(1)某化学实验兴趣小组自行购置了鸡蛋、食醋等生活用品,进行了如下探究。
①甲同学将鸡蛋壳(主要成分为 )泡进食醋中,发现有气泡产生,请写出该反应的离子方程式
)泡进食醋中,发现有气泡产生,请写出该反应的离子方程式___________ ;
②乙同学将鸡蛋清配制成溶液,向溶液中投射一条光束,看见一条光亮的“通路”,这种现象被称作___________ 。
③丙同学测出从超市购买的食醋中醋酸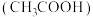 含量为
含量为 ,则食醋中醋酸含量为
,则食醋中醋酸含量为___________ 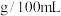 ,属于
,属于___________ 醋(填“酿造”或“配制”,已知:酿造醋的国家标准为醋酸含量必须大于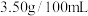 ,而配制醋仅为
,而配制醋仅为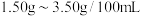 )。
)。
(2)下图是化学实验室浓盐酸试剂标签上的部分内容。
丁同学计划用该浓盐酸配制 的稀盐酸,可供选用的仪器有:①量筒;②烧瓶;③烧杯;④药匙;⑤玻璃棒;⑥试剂瓶。
的稀盐酸,可供选用的仪器有:①量筒;②烧瓶;③烧杯;④药匙;⑤玻璃棒;⑥试剂瓶。
请回答下列问题:
①经计算,配制 的稀盐酸需要量取上述浓盐酸的体积为
的稀盐酸需要量取上述浓盐酸的体积为___________  (结果保留1位小数)。
(结果保留1位小数)。
②配制稀盐酸时,还缺少的仪器有___________ 。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是___________ 。
a.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
b.定容时俯视容量瓶刻度线
c.转移溶液后,未洗涤烧杯和玻璃棒
d.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(1)某化学实验兴趣小组自行购置了鸡蛋、食醋等生活用品,进行了如下探究。
①甲同学将鸡蛋壳(主要成分为
 )泡进食醋中,发现有气泡产生,请写出该反应的离子方程式
)泡进食醋中,发现有气泡产生,请写出该反应的离子方程式②乙同学将鸡蛋清配制成溶液,向溶液中投射一条光束,看见一条光亮的“通路”,这种现象被称作
③丙同学测出从超市购买的食醋中醋酸
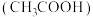 含量为
含量为 ,则食醋中醋酸含量为
,则食醋中醋酸含量为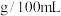 ,属于
,属于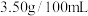 ,而配制醋仅为
,而配制醋仅为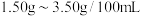 )。
)。(2)下图是化学实验室浓盐酸试剂标签上的部分内容。
盐酸化学纯( ) )化学式:  相对分子质黑:36.5 密度约   的质量分数:36.5% 的质量分数:36.5% |
 的稀盐酸,可供选用的仪器有:①量筒;②烧瓶;③烧杯;④药匙;⑤玻璃棒;⑥试剂瓶。
的稀盐酸,可供选用的仪器有:①量筒;②烧瓶;③烧杯;④药匙;⑤玻璃棒;⑥试剂瓶。请回答下列问题:
①经计算,配制
 的稀盐酸需要量取上述浓盐酸的体积为
的稀盐酸需要量取上述浓盐酸的体积为 (结果保留1位小数)。
(结果保留1位小数)。②配制稀盐酸时,还缺少的仪器有
③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是a.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
b.定容时俯视容量瓶刻度线
c.转移溶液后,未洗涤烧杯和玻璃棒
d.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
您最近一年使用:0次



