高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,
①该反应中的氧化剂是__________ ,还原剂是__________ ,每生成1 mol Na2FeO4转移__________ mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用:____________________________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:___________________________ 。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?_____________________________________________ 。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,
①该反应中的氧化剂是
②简要说明K2FeO4作为水处理剂时所起的作用:
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?
更新时间:2018-09-13 09:19:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】阅读下面一段材料并回答问题。
(1)K2FeO4中铁元素的化合价为___________ 。
(2)制备K2FeO4需要在___________ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于K2FeO4的说法中,不正确的是___________ 。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)将K2FeO4与水反应的化学方程式补充完整:___________ 。
4K2FeO4+口H2O=口Fe(OH)3(胶体)+口__________+口KOH
(5)消毒净化500m3水,至少需要K2FeO4的质量为___________ kg。[M(K2FeO4)=198g/mol]
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状]暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气 K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准…… |
(2)制备K2FeO4需要在
(3)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)将K2FeO4与水反应的化学方程式补充完整:
4K2FeO4+口H2O=口Fe(OH)3(胶体)+口__________+口KOH
(5)消毒净化500m3水,至少需要K2FeO4的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在抗击新冠肺炎疫情的战役中,病毒在不断发生变异,现有疫苗对变异病毒的有效性有待进一步的验证,因此民众的防疫意识不能松懈。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。最新的研究表明新冠病毒可能通过气溶胶传播。气溶胶属于____ (填“胶体”或“溶液”);常利用____ 区分溶液和胶体,其原理是分散质粒子对光的作用。
(2)为有效防止新冠病海的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
b. KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2O
c.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
①写出反应a对应的离子方程式:____ 。[已知HCl(浓)可拆分为H+和Cl-]
②配平反应b的方程式:(答题卡上只写系数)____ 。
 KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O。
H2O。
③用双线桥法标明c反应方程式中电子转移的方向和数目____ 。
④当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是____ 反应(填“a”、“b”、“c”下同);当得到等质量的Cl2时,消耗HCl的质量最多的是____ 反应。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。最新的研究表明新冠病毒可能通过气溶胶传播。气溶胶属于
(2)为有效防止新冠病海的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑b.
 KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2Oc.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
①写出反应a对应的离子方程式:
②配平反应b的方程式:(答题卡上只写系数)
 KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O。
H2O。③用双线桥法标明c反应方程式中电子转移的方向和数目
④当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是
您最近一年使用:0次
【推荐1】钢铁“发蓝”是在钢铁的表面形成一层四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应。完成下列填空:
(1)其技术过程中有如下的化学方程式:
①____ Fe+____ NaNO2+____ NaOH—____ Na2FeO2+____ H2O+____ NH3↑;
②6Na2FeO2 + NaNO2 + 5H2O =3Na2Fe2O4 + NH3↑ + 7NaOH;
③Na2FeO2 + Na2Fe2O4 + 2 H2O = Fe3O4 + 4 NaOH;
试配平方程式①,并标出电子转移的方向和数目_____________ 。
(2)在讨论上述三个反应时,甲、乙、丙三位同学各自提出了他们的看法,其中说法正确的是_____________ 。
甲同学:该生产过程中不会产生污染问题
乙同学:只要是有NaNO2 参与的反应,它都是充当氧化剂角色的
丙同学:每一步过程中涉及到的化学反应都可归属于氧化还原反应原理
(3)若整个过程共获得67.2升氨气(标况下)则电子转移________ mol。
(4)若获得1mol Fe3O4,则反应过程中NaOH的量将多________ (填“消耗”或“产出”)________ mol。
(1)其技术过程中有如下的化学方程式:
①
②6Na2FeO2 + NaNO2 + 5H2O =3Na2Fe2O4 + NH3↑ + 7NaOH;
③Na2FeO2 + Na2Fe2O4 + 2 H2O = Fe3O4 + 4 NaOH;
试配平方程式①,并标出电子转移的方向和数目
(2)在讨论上述三个反应时,甲、乙、丙三位同学各自提出了他们的看法,其中说法正确的是
甲同学:该生产过程中不会产生污染问题
乙同学:只要是有NaNO2 参与的反应,它都是充当氧化剂角色的
丙同学:每一步过程中涉及到的化学反应都可归属于氧化还原反应原理
(3)若整个过程共获得67.2升氨气(标况下)则电子转移
(4)若获得1mol Fe3O4,则反应过程中NaOH的量将多
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。根据所学知识回答下列问题:
(1) 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为___________ (填化学式),标准状况下,每生成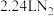 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为___________  。
。
(2)在一定条件下, 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被___________ (填“氧化”或“还原”), 中
中 的化合价是
的化合价是___________ 价。
(3)某一反应体系有反应物和生成物共七种物质: 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。
①该反应中的还原剂是___________ (填化学式,下同),被还原的物质为___________ 。
②写出该反应的化学方程式:___________ 。
(1)
 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为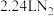 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为 。
。(2)在一定条件下,
 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被 中
中 的化合价是
的化合价是(3)某一反应体系有反应物和生成物共七种物质:
 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。①该反应中的还原剂是
②写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】新冠病毒曾经伤害人类,也是曾经让你最为惧怕的病毒,但它却只不过是蛋白质包裹着的DNA而已,使用适当浓度的84消毒液、双氧水等消毒剂即可将其杀死。但是两者混合使用,消毒效果几乎降为零。此外,84消毒液呈碱性,可以通过氯气与氢氧化钠溶液的反应来制得,这是你知道的。
(1)写出上述两种消毒剂中有效成分的电子式。___________ 、___________
(2)如图所示是家用制取84消毒液的装置,以石墨为电极电解由进口输入的饱和食盐水,则阳极为___________ (填写“电极1”“电极2”)。

将湿润的淀粉碘化钾试纸靠近出口处,未显蓝色。此制备过程的总反应为___________
(3)上述两种消毒剂混合使用,有无毒气体产生,则___________
(1)写出上述两种消毒剂中有效成分的电子式。
(2)如图所示是家用制取84消毒液的装置,以石墨为电极电解由进口输入的饱和食盐水,则阳极为

将湿润的淀粉碘化钾试纸靠近出口处,未显蓝色。此制备过程的总反应为
(3)上述两种消毒剂混合使用,有无毒气体产生,则___________
| A.该反应中,过氧化氢做氧化剂 |
| B.可以通过焰色反应,确认该反应已进行完全 |
| C.若生成2.24 L标况下的氧气,则消耗14.9 g NaClO |
D.残留液中滴加 溶液,有白色沉淀生成 溶液,有白色沉淀生成 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】CN-可以造成水体污染,某小组采用如下方法对污水进行处理。
Ⅰ 双氧水氧化法除NaCN。
双氧水氧化法除NaCN。
(1)NaCN的电子式为____________________________ 。
(2)碱性条件下加入双氧水除CN-,可得到纯碱和一种无色无味的无毒气体,该反应的离子方程式为________________ 。
Ⅱ.CN-和Cr2O72-联合废水处理法。

(3)②中反应后无气体放出,该反应的离子方程式为_____________________ 。
(4)步骤③中,每处理0.4mol Cr2O72-,至少消耗Na2S2O3________ mol。
Ⅰ
 双氧水氧化法除NaCN。
双氧水氧化法除NaCN。(1)NaCN的电子式为
(2)碱性条件下加入双氧水除CN-,可得到纯碱和一种无色无味的无毒气体,该反应的离子方程式为
Ⅱ.CN-和Cr2O72-联合废水处理法。

(3)②中反应后无气体放出,该反应的离子方程式为
(4)步骤③中,每处理0.4mol Cr2O72-,至少消耗Na2S2O3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)储氢纳米碳管具有广泛的用途,电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒,这种碳纳来颗粒可用氧化气化法提纯,反应的化学方程式如下(未配平):C+K2Cr2O7+H2SO4=CO2↑+K2SO4+Cr2(SO4)3+H2O。回答下列问题:
①配平上述反应方程式并用单线桥标出反应中电子转移方向和数目______ 。
②上述反应的离子方程式是_____ 。
③离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO 的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是
的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是______ 。
A.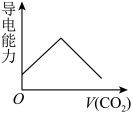 B.
B. C.
C.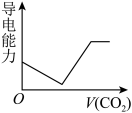 D.
D.
④若反应中电子转移了NA个,则产生的气体在标况下的体积为______ L;请写出Na2O2与该反应氧化产物反应的化学方式______ 。
(2)磷酸(H3PO4)、次磷酸(H3PO2)是精细磷化工产品,具有较强还原性,回答下列问题:
①H3PO2是一元中强酸,NaH2PO2为______ (填“正盐”或“酸式盐”)。
②H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于对器皿实现化学镀银,利用H3PO2进行化学镀银反应中,氧化产物为H3PO4,则氧化剂与还原剂的物质的量之比为______ 。
(1)储氢纳米碳管具有广泛的用途,电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒,这种碳纳来颗粒可用氧化气化法提纯,反应的化学方程式如下(未配平):C+K2Cr2O7+H2SO4=CO2↑+K2SO4+Cr2(SO4)3+H2O。回答下列问题:
①配平上述反应方程式并用单线桥标出反应中电子转移方向和数目
②上述反应的离子方程式是
③离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO
 的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是
的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是A.
 B.
B. C.
C. D.
D.
④若反应中电子转移了NA个,则产生的气体在标况下的体积为
(2)磷酸(H3PO4)、次磷酸(H3PO2)是精细磷化工产品,具有较强还原性,回答下列问题:
①H3PO2是一元中强酸,NaH2PO2为
②H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于对器皿实现化学镀银,利用H3PO2进行化学镀银反应中,氧化产物为H3PO4,则氧化剂与还原剂的物质的量之比为
您最近一年使用:0次

 ;②复合膨松剂;③
;②复合膨松剂;③ ;④
;④ 胶体;⑤液态氯化氢;⑥澄清石灰水;⑦
胶体;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧金属钠;⑨氨气;⑩酒精
;⑧金属钠;⑨氨气;⑩酒精 、
、 、H+、H2O和
、H+、H2O和 。已知在该反应中氧化反应只有Cr3+→
。已知在该反应中氧化反应只有Cr3+→

