用氯化钠固体配制1.00mol/L的NaCl溶液500mL,回答下列问题
(1)请写出该实验的实验步骤
①计算,②________ ,③________ ,④_________ ,⑤洗涤,⑥________ ,⑦ 摇匀。
(2)所需仪器为:容量瓶(规格:__________ )、托盘天平、还需要那些玻璃仪器才能完成该实验,请写出:_______________ 。
使用容量瓶前必须进行的操作是______________ 。
(3)试分析下列操作对所配溶液的浓度有何影响 。(填“偏高”“偏低”“无影响”)
①为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至容量瓶定容。对所配溶液浓度的影响:___________
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶浓度的影响:_________ 。
③某同学从该溶液中取出50mL,其中NaCl的物质的量浓度为_________ 。
(1)请写出该实验的实验步骤
①计算,②
(2)所需仪器为:容量瓶(规格:
使用容量瓶前必须进行的操作是
(3)试分析下列操作
①为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至容量瓶定容。对所配溶液浓度的影响:
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶浓度的影响:
③某同学从该溶液中取出50mL,其中NaCl的物质的量浓度为
更新时间:2018-09-26 16:07:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室用固体烧碱配制0.1mol/L的NaOH溶液480mL,请回答:
(1)经计算需要用托盘天平称取质量_______ g NaOH固体,NaOH固体放在_______ (填“滤纸”或“烧杯”)上称量。
(2)有以下仪器:①烧杯②药匙 ③250mL容量瓶 ④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平 ⑦量筒,配制时肯定不需要的仪器是_______ (填序号),除已有仪器外,配制上述溶液还需要的玻璃仪器是_______ 。
(3)配制溶液时,在计算、称量、溶解、冷却后还有以下几个步骤,其正确的操作顺序为_______ (填序号)。
①洗涤 ②振荡摇匀 ③定容 ④颠倒摇匀 ⑤转移
(4)配制过程中,下列操作会引起结果偏低的是______ (填序号)
A.未洗涤烧杯、玻璃棒
B.定容时俯视刻度
C.容量瓶不干燥,含有少量蒸馏水
D.NaOH溶液未冷却至室温就转移到容量瓶
E. 用托盘天平称取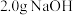 固体时所用时间较长;
固体时所用时间较长;
(1)经计算需要用托盘天平称取质量
(2)有以下仪器:①烧杯②药匙 ③250mL容量瓶 ④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平 ⑦量筒,配制时肯定不需要的仪器是
(3)配制溶液时,在计算、称量、溶解、冷却后还有以下几个步骤,其正确的操作顺序为
①洗涤 ②振荡摇匀 ③定容 ④颠倒摇匀 ⑤转移
(4)配制过程中,下列操作会引起结果偏低的是
A.未洗涤烧杯、玻璃棒
B.定容时俯视刻度
C.容量瓶不干燥,含有少量蒸馏水
D.NaOH溶液未冷却至室温就转移到容量瓶
E. 用托盘天平称取
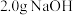 固体时所用时间较长;
固体时所用时间较长;
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
(一)该浓盐酸的物质的量浓度为__ mol/L。
(二)某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为0.3mol/L稀盐酸,可供选用的仪器有①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒,请回答下列问题:
(1)配制稀盐酸时,上述仪器中不需要使用的有__  选填序号
选填序号 ,还缺少的仪器有
,还缺少的仪器有__  写仪器名称
写仪器名称 。
。
(2)下列对容量瓶及其使用方法的描述中正确的是__ 。
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.容量瓶可用来长期储存溶液
D.使用前要检查容量瓶是否漏水
(3)该学生需要量取__ mL上述浓盐酸来配制。
(4)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)__ ;
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
(5)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”)。
I.用量筒量取浓盐酸时俯视观察凹液面___ ;
II.用量筒量取浓盐酸后,洗涤量筒2—3次,洗涤液也转移到容量瓶__ ;
III.溶液注入容量瓶前没有恢复到室温就进行定容__ ;
IV.用量筒量取浓盐酸时,仰视读数__ ;
V.容量瓶中原有少量蒸馏水__ ;
VI.定容时加水超过刻度线,用胶头滴管吸取多余的液体至刻度线_ ;
VII.定容、摇匀后少量溶液外流___ 。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.2g/cm3 HCl质量分数:36.5% |
(二)某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为0.3mol/L稀盐酸,可供选用的仪器有①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒,请回答下列问题:
(1)配制稀盐酸时,上述仪器中不需要使用的有
 选填序号
选填序号 ,还缺少的仪器有
,还缺少的仪器有 写仪器名称
写仪器名称 。
。(2)下列对容量瓶及其使用方法的描述中正确的是
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.容量瓶可用来长期储存溶液
D.使用前要检查容量瓶是否漏水
(3)该学生需要量取
(4)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
(5)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”)。
I.用量筒量取浓盐酸时俯视观察凹液面
II.用量筒量取浓盐酸后,洗涤量筒2—3次,洗涤液也转移到容量瓶
III.溶液注入容量瓶前没有恢复到室温就进行定容
IV.用量筒量取浓盐酸时,仰视读数
V.容量瓶中原有少量蒸馏水
VI.定容时加水超过刻度线,用胶头滴管吸取多余的液体至刻度线
VII.定容、摇匀后少量溶液外流
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为蒸馏实验装置.
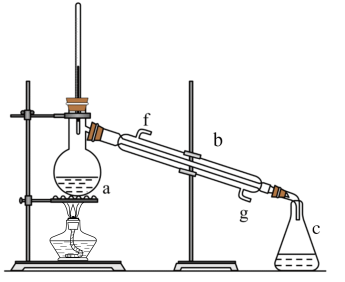
(1)写出下列仪器的名称:a.__ b.__ ;
(2)实验过程中,需要通冷水,图中的进水方向是__ 进(填图中字母);
(3)若利用装置分离四氯化碳和酒精的混合物,还缺少的用品是__ .
(4)若用装置制蒸馏水,实验时a中除加入少量自来水外,还需加入少量__ ,其作用是防止暴沸.
II.(5)现需配制0.1mol•L﹣1NaOH溶液480mL,根据此,回答下列问题:
①配制氢氧化钠溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和__ .
②实验时需要称量氢氧化钠__ g;
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)__ .
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,上下颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④配制0.1mol•L﹣1NaOH溶液的实验中,如果出现以下操作,会导致配制溶液的浓度偏大的有__ (填写字母).
A.称量时用了生锈的砝码 B.未洗涤溶解NaOH的烧杯
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.容量瓶未干燥即用来配制溶液 E.定容时仰视刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.

(1)写出下列仪器的名称:a.
(2)实验过程中,需要通冷水,图中的进水方向是
(3)若利用装置分离四氯化碳和酒精的混合物,还缺少的用品是
(4)若用装置制蒸馏水,实验时a中除加入少量自来水外,还需加入少量
II.(5)现需配制0.1mol•L﹣1NaOH溶液480mL,根据此,回答下列问题:
①配制氢氧化钠溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和
②实验时需要称量氢氧化钠
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,上下颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④配制0.1mol•L﹣1NaOH溶液的实验中,如果出现以下操作,会导致配制溶液的浓度偏大的有
A.称量时用了生锈的砝码 B.未洗涤溶解NaOH的烧杯
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.容量瓶未干燥即用来配制溶液 E.定容时仰视刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】(1)用18mol·L-1的硫酸配制1.00 mol·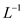 的硫酸100mL。若实验仪器有:
的硫酸100mL。若实验仪器有:
A.100mL量筒、B.托盘天平、C.玻璃棒、D.50mL容器瓶、E. 10mL量筒、F.胶头滴管、G. 50mL烧杯、H. 100mL容量瓶。
实验时应选用仪器是________________ (填字母);
(2)在容量瓶的使用方法中,下列操作不正确的是___________ (填字母);
A.使用容量瓶前检查其是否漏水。
B.容量瓶用蒸馏水洗净后,再用待配溶液洗涤。
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1—2cm处,用胶头滴管滴加蒸馏水到刻度线。
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1—2cm处,用胶头滴管滴加蒸馏水到刻度线。
E.盖好瓶盖,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(3)浓H2SO4稀释时应该________________________________ ;
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“不变”)
①稀释硫酸后的烧杯未洗涤:____________ ;
②未经冷却趁热将溶液注入容量瓶中:____________ ;
③摇匀后发现液面低于刻度线再加水:____________ ;
④容量瓶中原有少量蒸馏水:_____________ 。
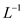 的硫酸100mL。若实验仪器有:
的硫酸100mL。若实验仪器有:A.100mL量筒、B.托盘天平、C.玻璃棒、D.50mL容器瓶、E. 10mL量筒、F.胶头滴管、G. 50mL烧杯、H. 100mL容量瓶。
实验时应选用仪器是
(2)在容量瓶的使用方法中,下列操作不正确的是
A.使用容量瓶前检查其是否漏水。
B.容量瓶用蒸馏水洗净后,再用待配溶液洗涤。
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1—2cm处,用胶头滴管滴加蒸馏水到刻度线。
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1—2cm处,用胶头滴管滴加蒸馏水到刻度线。
E.盖好瓶盖,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(3)浓H2SO4稀释时应该
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“不变”)
①稀释硫酸后的烧杯未洗涤:
②未经冷却趁热将溶液注入容量瓶中:
③摇匀后发现液面低于刻度线再加水:
④容量瓶中原有少量蒸馏水:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某校环保小组学生处理污水样品时,需要配制450mL0.1mol/L硫酸。
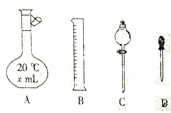
(1)如图所示仪器中,配制上述溶液肯定不需要的仪器是_____ (填字母),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是______ (填仪器名称)。
(2)如果用5.0mol/L的硫酸来配制上述硫酸,则需该硫酸的体积为_____ 。
(3)在容量瓶的使用方法中,下列操作正确的是____ (填字母)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水接近标线l~2cm处,用滴管加蒸馏水至标线
D.定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(4)定容时,若仰视刻度线,则所配溶液物质的量浓度___ (填“偏大”“偏小”“不变”)。
(1)如图所示仪器中,配制上述溶液肯定不需要的仪器是

(2)如果用5.0mol/L的硫酸来配制上述硫酸,则需该硫酸的体积为
(3)在容量瓶的使用方法中,下列操作正确的是
A.使用容量瓶前检查它是否漏水
B.容量瓶用水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水接近标线l~2cm处,用滴管加蒸馏水至标线
D.定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(4)定容时,若仰视刻度线,则所配溶液物质的量浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】配制一定物质的量浓度的溶液是化学实验室的基本实验操作之一。回答下列问题:
(1)用质量分数36.5%、密度约为1.2 g· cm-3的浓盐酸配制0.5 mol·L-1的盐酸溶液450 mL,应最好选用__________ mL 量筒。
A.15 mL B.20 mL C.50 mL D.100mL
(2)配制上述溶液,除用到量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器是_______ 。
(3)配制时,其正确的操作顺序是_________ (用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有水的烧杯中加入浓盐酸稀释
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(4)下面操作造成所配的溶液浓度偏高的是________ (填序号)。
A.转移时没有洗涤烧杯、玻璃棒
B.向容量瓶加水定容时眼睛俯视液面
C.用量筒量浓盐酸后洗涤量筒并将洗涤液转移到容量瓶
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
(1)用质量分数36.5%、密度约为1.2 g· cm-3的浓盐酸配制0.5 mol·L-1的盐酸溶液450 mL,应最好选用
A.15 mL B.20 mL C.50 mL D.100mL
(2)配制上述溶液,除用到量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器是
(3)配制时,其正确的操作顺序是
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有水的烧杯中加入浓盐酸稀释
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(4)下面操作造成所配的溶液浓度偏高的是
A.转移时没有洗涤烧杯、玻璃棒
B.向容量瓶加水定容时眼睛俯视液面
C.用量筒量浓盐酸后洗涤量筒并将洗涤液转移到容量瓶
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室要配制100mL1.0mol·L-1的NaCl溶液,试回答下列各题。
(1)经计算,应该用托盘天平称取NaCl固体_________ g。
(2)若用NaCl固体配制溶液,下列仪器中,不需要用到的是_________ (填序号)。
A.锥形瓶,B.200mL容量瓶,C.烧杯,D.胶头滴管,E.药匙,F.托盘天平,G.洗瓶
(3)若要实施配制,除上述仪器外,尚缺的仪器或用品是_________ 、_________ ;
(4)在使用前必须检查容量瓶是否______ 。
(5)配制过程有以下操作:A.移液 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀。其正确的操作顺序应是_________ (填序号)。
(6)下列四项错误操作会导致所得溶液浓度偏高的是______ (填序号)。
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(7)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度:______ ;
(1)经计算,应该用托盘天平称取NaCl固体
(2)若用NaCl固体配制溶液,下列仪器中,不需要用到的是
A.锥形瓶,B.200mL容量瓶,C.烧杯,D.胶头滴管,E.药匙,F.托盘天平,G.洗瓶
(3)若要实施配制,除上述仪器外,尚缺的仪器或用品是
(4)在使用前必须检查容量瓶是否
(5)配制过程有以下操作:A.移液 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀。其正确的操作顺序应是
(6)下列四项错误操作会导致所得溶液浓度偏高的是
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(7)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图表示配制 220 mL 0.100 mol·L-1Na2SO4溶液的几个关键实验步骤和操作,据图回答下列问题:

(1)步骤E中将一玻璃仪器上下颠倒数次,该仪器的名称是_________ ,规格_________ 。
(2)步骤B通常称为转移,步骤A通常称为__________ 。
(3)将上述实验步骤A→F按实验过程先后次序排列______________ 。
(4)下列操作对所配制溶液浓度的影响:
样品溶解后未冷却就直接转移到容量瓶中,并马上进行配制,__________ 。
摇匀后,发现凹液面低于刻度线大约1mm,_________ 。(填偏高、偏低、无影响)

(1)步骤E中将一玻璃仪器上下颠倒数次,该仪器的名称是
(2)步骤B通常称为转移,步骤A通常称为
(3)将上述实验步骤A→F按实验过程先后次序排列
(4)下列操作对所配制溶液浓度的影响:
样品溶解后未冷却就直接转移到容量瓶中,并马上进行配制,
摇匀后,发现凹液面低于刻度线大约1mm,
您最近一年使用:0次



