下列说法正确的是
| A.已知NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l) ΔH = - 57.3 kJ/mol ,则含有40.0g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3kJ的热量。 |
| B.已知2C(s)+2O2(g)=2CO2(g) ΔH=akJ/mol,2C(s)+2O2(g)=2CO (g) ΔH =b kJ/mol,则a>b。 |
| C.取50mL 0.55mol/LNaOH(aq)和50mL 0.50mol/L HCl(aq)进行中和热的测定实验,用温度计测定HCl(aq)起始温度后,直接测定NaOH(aq)的温度,会使中和热ΔH偏小 |
| D.已知P(白磷,s)=P(红磷,s) ΔH<0,则白磷比红磷稳定。 |
更新时间:2018-10-24 20:51:46
|
相似题推荐
单选题
|
适中
(0.65)
真题
【推荐1】下列实验方法合理的是
| A.可用水鉴别己烷、四氯化碳、乙醇三种无色液体 |
| B.油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油充分分离 |
| C.可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 |
| D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,下列实验探究方案能达到探究目的的是
选项 | 探究方案 | 探究目的 |
A | 向5mL0.lmol/LKI溶液中加入1mL0.1mol/L | 化学反应有一定限度 |
B | 用玻璃棒蘸取待测溶液滴在pH试纸上,与标准比色卡对照读数 | 测定新制氯水的pH |
C | 分别向2支盛有等体积、等浓度的 | 探究浓度对反应速率的影响 |
D | 分别取50mL0.5mol/L硫酸、氢氧化钡两溶液在量热器中充分反应,测定反应前后最大温度差 | 测定中和热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用稀盐酸与稀 溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是
溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是
 溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是
溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是| A.酸、碱混合前应分别测量其温度 |
| B.酸碱混合时,应将碱溶液一次性快速加入到酸中 |
| C.实验中应上下抽动玻璃搅拌器 |
D.用量筒取盐酸时若仰视读数,则测得的反应热 偏大 偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知强酸与强碱的稀溶液发生中和反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,向0.1 L 0.2 mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀盐酸,恰好完全反应。则其焓变ΔH1、ΔH2、ΔH3的关系是
| A.ΔH1>ΔH2>ΔH3 | B.ΔH1>ΔH3>ΔH2 | C.ΔH1=ΔH3>ΔH2 | D.ΔH1<ΔH3<ΔH2 |
您最近一年使用:0次
【推荐1】现有如下3个热化学方程式:
H2(g)+ O2(g)=H2O(g) ΔH1=-akJ/mo ①
O2(g)=H2O(g) ΔH1=-akJ/mo ①
H2(g)+ O2(g)=H2O(l) ΔH2=-bkJ/mol ②
O2(g)=H2O(l) ΔH2=-bkJ/mol ②
2H2(g)+O2(g)=2H2O(l) ΔH3=-ckJ/mol ③
则由下表所列的原因能推导出后面结论的是
H2(g)+
 O2(g)=H2O(g) ΔH1=-akJ/mo ①
O2(g)=H2O(g) ΔH1=-akJ/mo ①H2(g)+
 O2(g)=H2O(l) ΔH2=-bkJ/mol ②
O2(g)=H2O(l) ΔH2=-bkJ/mol ②2H2(g)+O2(g)=2H2O(l) ΔH3=-ckJ/mol ③
则由下表所列的原因能推导出后面结论的是
| 选项 | 原因 | 结论 |
| A | H2的燃烧是放热反应 | a、b、c均大于0 |
| B | ①和②中物质的化学计量数均相同 | a=b |
| C | ③中H2O的状态不同,化学计最数不同 | a、b、c不会有任何等量或不等量关系 |
| D | ③的化学计量数是②的2倍 | ΔH2<ΔH1 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
B.由C(石墨,s)=C(金刚石,s)  可知金刚石比石墨稳定 可知金刚石比石墨稳定 |
| C.同温同压下,H2(g)+ Cl2(g)=2HCl(g)在光照条件和点燃条件下的ΔH 相同 |
D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH = -38.6 kJ·mol- 1 2NH3(g) ΔH = -38.6 kJ·mol- 1 |
您最近一年使用:0次

 溶液充分反应后用苯萃取2~3次,取水层滴加KSCN溶液观察溶液颜色变化
溶液充分反应后用苯萃取2~3次,取水层滴加KSCN溶液观察溶液颜色变化 溶液的试管中同时加入2mL5%
溶液的试管中同时加入2mL5% 溶液
溶液 和1.5mol
和1.5mol  置于密闭容器中充分反应生成
置于密闭容器中充分反应生成 (g),放热19.3kJ,则其热化学方程式为
(g),放热19.3kJ,则其热化学方程式为
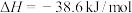
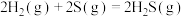
 ,
,
 ,则
,则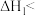

 的燃烧热为890.3kJ/mol,则101kPa时,
的燃烧热为890.3kJ/mol,则101kPa时,

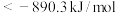

 和
和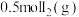 )置于密闭容器中充分反应生成HI(g)放热akJ,其热化学方程式为:
)置于密闭容器中充分反应生成HI(g)放热akJ,其热化学方程式为: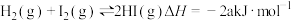

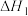 ,
,
 ,则
,则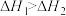
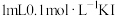 溶液中加入
溶液中加入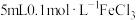 溶液,振荡,加苯萃取后,向水层中加入5滴KSCN溶液,观察实验现象
溶液,振荡,加苯萃取后,向水层中加入5滴KSCN溶液,观察实验现象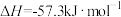 ,则
,则 和
和 反应的中和热
反应的中和热