有关物质的量的计算是中学化学的重要部分,请回答下列有关物质的量的计算问题。
(1)在标准状况下,67.2 L CO2是__________ mol,质量为_______ g,含有__________ 个CO2分子,其中含有__________ mol氧原子。
(2)在标准状况下,1.7 g氨气所占的体积约为_________ L,它与同条件下_____ mol H2S含有相同的氢原子数。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______ ,R的相对原子质量为__________ 。
(4)实验室常用浓硫酸的质量分数为98%,密度为1.80 g·mL−1,其物质的量浓度是_______ 。
(5)标准状况下,将V L A气体(摩尔质量为M g/mol)完全溶于0.1 L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为_______ mol/L。
A. B.
B. C.
C.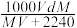 D.
D.
(1)在标准状况下,67.2 L CO2是
(2)在标准状况下,1.7 g氨气所占的体积约为
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为
(4)实验室常用浓硫酸的质量分数为98%,密度为1.80 g·mL−1,其物质的量浓度是
(5)标准状况下,将V L A气体(摩尔质量为M g/mol)完全溶于0.1 L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为
A.
 B.
B. C.
C.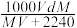 D.
D.
更新时间:2018-11-08 18:46:10
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入 、
、 的混合气体和1 mol空气,此时活塞的位置如图所AB示。
的混合气体和1 mol空气,此时活塞的位置如图所AB示。
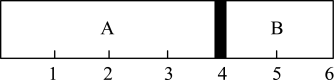
(1)A室混合气体的物质的量为_______ ,所含分子总数为_______ 。
(2)若将 、
、 的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来
的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来 、
、 的体积之比可能为
的体积之比可能为_______ 。
(3)若实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的_______ 倍。将A室 、
、 的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在_______ 刻度,容器内气体压强与反应前气体压强之比为_______ 。
 、
、 的混合气体和1 mol空气,此时活塞的位置如图所AB示。
的混合气体和1 mol空气,此时活塞的位置如图所AB示。
(1)A室混合气体的物质的量为
(2)若将
 、
、 的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来
的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来 、
、 的体积之比可能为
的体积之比可能为(3)若实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的
 、
、 的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,生成1.16 g白色沉淀。再向所得的悬浊液中逐滴加入1.00 mol/L 的盐酸溶液,加入盐酸溶液的体积与生成沉淀的关系如下图所示。试回答:
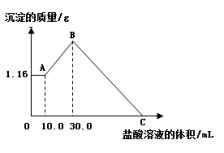
(1)写出A点到B点发生反应的离子方程式_____________________________ 。
(2)C点加入盐酸溶液的体积为_____________ 。
(3)原混合物中MgCl2的物质的量是_________ ,NaOH的质量是_____________ 。

(1)写出A点到B点发生反应的离子方程式
(2)C点加入盐酸溶液的体积为
(3)原混合物中MgCl2的物质的量是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】SO2、CO、NO、NH3是中学中常见的几种气体。
(1)质量之比为32:7:30的三种气体SO2、CO、NO,分子数之比为_______ ,氧原子数之比为_______ 。
(2)标准状况下,4.25g NH3的体积为______ L,它与标准状况下_____ L H2S含有相同数目的氢原子。
(3)将标准状况下6.72L SO2通入1L 0.6mol/L NaOH溶液中,左后得到的溶质是______ ,该溶质的物质的量浓度为________ mol/L(忽略通入气体后溶液体积的变化)。
(1)质量之比为32:7:30的三种气体SO2、CO、NO,分子数之比为
(2)标准状况下,4.25g NH3的体积为
(3)将标准状况下6.72L SO2通入1L 0.6mol/L NaOH溶液中,左后得到的溶质是
您最近一年使用:0次
【推荐1】请按要求完成下列各题:
(1)黑火药爆炸时发生反应:2KNO3+S+3C═K2S+N2↑+3CO2↑,其中被还原的元素是___ ,被氧化的元素是___ 。
(2)配平以下方程式:___ K2Cr2O7+___ HCl═___ KCl+___ CrCl3+___ Cl2↑+___ H2O
(3)已知19.2gCu与过量的200ml5mol/L稀硝酸充分反应,反应方程式如下,请计算(忽略反应前后溶液体积的变化).
3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
①转移电子的物质的量为___ mol;标准状况下,产生NO气体的体积为___ mL。
②反应后,NO3-的物质的量浓度为___ mol/L。
(1)黑火药爆炸时发生反应:2KNO3+S+3C═K2S+N2↑+3CO2↑,其中被还原的元素是
(2)配平以下方程式:
(3)已知19.2gCu与过量的200ml5mol/L稀硝酸充分反应,反应方程式如下,请计算(忽略反应前后溶液体积的变化).
3Cu+8HNO3
 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O①转移电子的物质的量为
②反应后,NO3-的物质的量浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】28g KOH固体必须溶解在________ g水中,才能使每200个水分子中有1个K+,所得溶液的密度为ρg/cm3,则该溶液中OH-的物质的量浓度为________ 。(保留到小数点后两位)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠________ g。
(2)钠—钾合金可在核反应堆中用作热交换液。5.05 g钠—钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。________
②计算并确定该钠-钾合金的化学式。______________
(3)氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2―→2Al(OH)3↓+Na2CO3+H2O,已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112 L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比。_____________
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠
(2)钠—钾合金可在核反应堆中用作热交换液。5.05 g钠—钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式。
(3)氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2―→2Al(OH)3↓+Na2CO3+H2O,已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112 L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比。
您最近一年使用:0次



