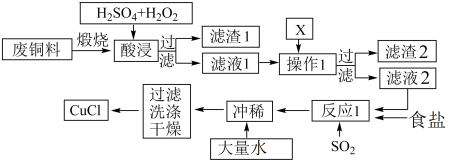
(1)把对应物质的字母代码填入括号内.
A.水玻璃 B.明矾 C.浓硫酸 D.过氧化钠 E.新制氯水 F.小苏打 G 次氯酸钙
①能使石蕊试液先变红后褪色___________ 。
②能做木材防火剂___________ 。
③能做处理胃酸过多的一种药剂____________ 。
(2)综合考虑经济、技术、环保等方面因素,设计以铜为原料制取硫酸铜的最佳路线图。如: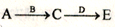
路线图为:________________ 。
A.水玻璃 B.明矾 C.浓硫酸 D.过氧化钠 E.新制氯水 F.小苏打 G 次氯酸钙
①能使石蕊试液先变红后褪色
②能做木材防火剂
③能做处理胃酸过多的一种药剂
(2)综合考虑经济、技术、环保等方面因素,设计以铜为原料制取硫酸铜的最佳路线图。如:
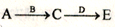
路线图为:
更新时间:2018-01-26 22:57:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某同学在复习元素化合物的性质时,做了如下学习笔记,请你一起完成。
氯气的颜色为__________ ;由氯的原子结构示意图推测,氯气具有很强的______ 性。为了证明推测是否正确,进行如下实验:
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕黄色烟。该反应的化学方程式是___________ 。
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生______ 色的火焰,瓶口有白雾的现象。
由实验I、II可知,上述推测_____ (填“正确”或“不正确”)。
III:将氯气溶于水,制得氯水。下列物质不能与新制氯水反应的是_____ 。
A.Na2CO3溶液 B.FeCl2溶液 C.AgNO3 溶液 D.CuCl2溶液
氯气的颜色为
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕黄色烟。该反应的化学方程式是
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生
由实验I、II可知,上述推测
III:将氯气溶于水,制得氯水。下列物质不能与新制氯水反应的是
A.Na2CO3溶液 B.FeCl2溶液 C.AgNO3 溶液 D.CuCl2溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】把对应物质的字母代码填入括号内.
E.新制氯水 F.小苏打 G.二硫化碳 H.次氯酸钙
1.漂白粉或漂粉精的有效成分( )
2.常温下能使铝铁钝化( )
3.能使石蕊试液先变红后褪色( )
4.能做木材防火剂( )
5.能做净水剂( ) 6.能做供氧剂( )
7.能做处理胃酸过多的一种药剂( )
8.能作为处理试管内壁沾有硫磺的一种试剂( )
| A.水玻璃 | B.明矾 | C.浓硫酸 | D.过氧化钠 |
E.新制氯水 F.小苏打 G.二硫化碳 H.次氯酸钙
1.漂白粉或漂粉精的有效成分
2.常温下能使铝铁钝化
3.能使石蕊试液先变红后褪色
4.能做木材防火剂
5.能做净水剂
7.能做处理胃酸过多的一种药剂
8.能作为处理试管内壁沾有硫磺的一种试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】1929年,吴蕴初先生在上海创建了天原化工厂,它是中国最早的氯碱工业。下图给出了部分生产流程:
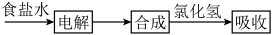
(1)写出电解饱和食盐水的化学方程式___________ ,阳极产生的气体如何检验?___________ 。工业上常用电解生成的产物氯气和氢气燃烧的方法制取氯化氢气体,写出 溶于水后电离方程式
溶于水后电离方程式___________ 。
(2)实验测得产生的氢气体积(已折算成标准状况)为5.60mL,电解后溶液的体积恰好为50.0mL,则溶液中 的浓度为
的浓度为___________ 。
(3)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的 、
、 、
、 及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的
及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的 溶液 ③加适量的盐酸④加过量的
溶液 ③加适量的盐酸④加过量的 溶液⑤加过量的
溶液⑤加过量的 溶液,操作正确的顺序是___________(选填字母)。
溶液,操作正确的顺序是___________(选填字母)。
(4)新制的氯水中存在多种微粒。
①将氯气溶于水后制得氯水,新制的氯水显浅黄绿色,说明氯水中有___________ (填微粒符号)存在。
②向氯水中滴加硝酸银溶液,有白色沉淀生成,证明氯水中含___________ (填微粒符号)。
③用pH计测出,氯水的 ,说明了氯水中含
,说明了氯水中含___________ (填微粒符号)。
(5)工业上通常把氯气通入石灰乳中可以制得漂粉精,其中有效成份为___________ (写名称),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):___________ 。

(1)写出电解饱和食盐水的化学方程式
 溶于水后电离方程式
溶于水后电离方程式(2)实验测得产生的氢气体积(已折算成标准状况)为5.60mL,电解后溶液的体积恰好为50.0mL,则溶液中
 的浓度为
的浓度为(3)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的
 、
、 、
、 及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的
及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤②加过量的 溶液 ③加适量的盐酸④加过量的
溶液 ③加适量的盐酸④加过量的 溶液⑤加过量的
溶液⑤加过量的 溶液,操作正确的顺序是___________(选填字母)。
溶液,操作正确的顺序是___________(选填字母)。| A.①④②⑤③ | B.④⑤②①③ | C.②⑤④①③ | D.⑤②④③① |
(4)新制的氯水中存在多种微粒。
①将氯气溶于水后制得氯水,新制的氯水显浅黄绿色,说明氯水中有
②向氯水中滴加硝酸银溶液,有白色沉淀生成,证明氯水中含
③用pH计测出,氯水的
 ,说明了氯水中含
,说明了氯水中含(5)工业上通常把氯气通入石灰乳中可以制得漂粉精,其中有效成份为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)Na2SiO3的水溶液俗称______________ ,是制备硅胶和木材防火剂的原料。
(2)许多人喜欢佩戴玉石饰品。玉石的主要成分基本属于硅酸盐,例如和田玉(Ca2Mg5H2Si8O24)可表示为氧化物形式2CaO·5MgO·8SiO2·H2O,则南阳玉(CaAl2Si2O8)表示为氧化物形式是________________ 。
(3)光导纤维在强碱性条件下容易发生“断路”,试用离子方程式解释其原因_____________________________________________ 。
(4)蔗糖与浓硫酸反应生成的黑色(单质)物质会继续与浓硫酸作用产生两种气体,当转移2mol电子时,生成标准状况下的气体共_______ L。
(2)许多人喜欢佩戴玉石饰品。玉石的主要成分基本属于硅酸盐,例如和田玉(Ca2Mg5H2Si8O24)可表示为氧化物形式2CaO·5MgO·8SiO2·H2O,则南阳玉(CaAl2Si2O8)表示为氧化物形式是
(3)光导纤维在强碱性条件下容易发生“断路”,试用离子方程式解释其原因
(4)蔗糖与浓硫酸反应生成的黑色(单质)物质会继续与浓硫酸作用产生两种气体,当转移2mol电子时,生成标准状况下的气体共
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请按照要求回答下列各小题:
(1)被称为“水玻璃”的是溶液___ (填化学式),其电离方程式为___ 。
(2)随着生产力的发展,硫酸的生产工艺几经改进,目前工业上主要采用接触法制硫酸,其中产生SO2的设备的名称是___ 。
(3) 已知:2H++2CrO
 Cr2O
Cr2O +H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是
+H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是___ ;操作B的名称是___ 。
(1)被称为“水玻璃”的是溶液
(2)随着生产力的发展,硫酸的生产工艺几经改进,目前工业上主要采用接触法制硫酸,其中产生SO2的设备的名称是
(3) 已知:2H++2CrO

 Cr2O
Cr2O +H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是
+H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)写出地壳中含量最高的元素的符号:_______ 。
(2)写出通信中硅的氧化物的一种用途:_______ 。
(3)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为 。
。
①该反应中Si元素的化合价为_______ 价。
②其中还原产物的化学式为_______ 。
③高温真空环境中,C与SiO2反应也可以生成SiC,写出该反应的化学方程式:_______ 。
(4)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作_______ ;设计简单实验比较醋酸与H2SiO3酸性的强弱:_______ 。
(1)写出地壳中含量最高的元素的符号:
(2)写出通信中硅的氧化物的一种用途:
(3)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为
 。
。①该反应中Si元素的化合价为
②其中还原产物的化学式为
③高温真空环境中,C与SiO2反应也可以生成SiC,写出该反应的化学方程式:
(4)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学反应。
(1)请你写出发酵粉中的主要钠盐的化学式______________ 。
(2)请你写出下列反应的化学方程式。(注意反应条件并配平)
工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉(主要成分是氯化钙和次氯酸钙)________________________________________ 。
(3)请你写出下列反应的离子方程式。
胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多____________ 。
将铁加入硫酸铜溶液中炼铜(湿法炼铜)_________________ 。
(1)请你写出发酵粉中的主要钠盐的化学式
(2)请你写出下列反应的化学方程式。(注意反应条件并配平)
工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉(主要成分是氯化钙和次氯酸钙)
(3)请你写出下列反应的离子方程式。
胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多
将铁加入硫酸铜溶液中炼铜(湿法炼铜)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】补齐物质与其用途的连线___________ 。
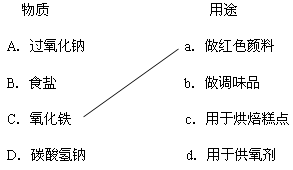

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠俗称小苏打,其水溶液显____________ 性(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为___________________ 。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者____________ 后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的方法是____________ (填“加热”或“溶解过滤”)。
(1)碳酸氢钠俗称小苏打,其水溶液显
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
(3)除去碳酸钠固体中碳酸氢钠的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并进行相关探究。
【资料查阅】

【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)D装置的作用_________________ 。
(2)装置D中发生的氧化还原反应的离子方程式是________________ 。
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是____________ 。
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuO杂质,根据资料信息分析:则产生的原因是__________________ 。
【资料查阅】

【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)D装置的作用
(2)装置D中发生的氧化还原反应的离子方程式是
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuO杂质,根据资料信息分析:则产生的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】CuSO4是一种重要化工原料,其制备和有关性质如图所示。

(1)途径①②③,更好体现绿色化学思想的是______________ 。
(2)物质Y具有的性质是_________ (填“氧化性”或“还原性”)。
(3)混合气体X既能使品红溶液褪色又能使带火星木条复燃,则混合气体X的成分是_________ 。
(4)途径①所用混酸中H2SO4与HNO3物质的量之比是_________ 。并写出发生反应的离子方程式:__________________ 。

(1)途径①②③,更好体现绿色化学思想的是
(2)物质Y具有的性质是
(3)混合气体X既能使品红溶液褪色又能使带火星木条复燃,则混合气体X的成分是
(4)途径①所用混酸中H2SO4与HNO3物质的量之比是
您最近一年使用:0次