在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是
| A.V (N2)=0.2mol•L﹣1•min﹣1 | B.V (N2)=0.1mol•L﹣1•min﹣1 |
| C.V (NH3)=0.1mol•L﹣1•min﹣1 | D.V (H2)=0.3mol•L﹣1•min﹣1 |
更新时间:2018-12-09 10:57:47
|
【知识点】 化学反应速率与化学计量数之间的关系解读
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】对于4NH3(g) + 3O2(g) = 2N2(g) + 6 H2O(g) 的反应来说,以下化学反应速率的表示中反应速率最快的是
| A.v(NH3)=0.6 mol• L-1•min-1 | B.v(O2) =0.4 mol• L-1•min-1 |
| C.v(N2)=0.2 mol• L-1•min-1 | D.v(H2O) =0.3 mol• L-1•min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向某密闭容器中加入0.3mol A、0.1mol C和一定量B的混合气体,在一定条件下发生反应,各物质的浓度随时间变化如图甲所示(t0~t1阶段的c(B)变化未画出),图乙为t2时刻改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段各改变一种不同的反应条件。下列说法中正确的是


| A.若t1="15" s,t0~t1阶段B的平均反应速率为0.004 mol·L-1·s-1 |
| B.t4~t5阶段改变的条件是减小压强 |
| C.该容器的容积为2 L,B的起始物质的量为0.02 mol |
D.t5~t6阶段,容器内A的物质的量减少了0.06 mol,容器与外界的热交换为a kJ,则该反应的热化学方程式为3A(g) B(g)+2C(g) △H=-50a kJ·mol-1 B(g)+2C(g) △H=-50a kJ·mol-1 |
您最近一年使用:0次

 在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为:①
在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为:① ;②
;②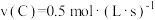 ;③
;③ ,三种情况下该反应速率大小的关系正确的是
,三种情况下该反应速率大小的关系正确的是 ②
②

