为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。

(1)甲装置中,a电极的反应式为_______________________________ 。
(2)乙装置中,阴极区产物为____________ 。
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为________ (填“正”或“负”)极,该装置内发生反应的化学方程式为________________ 、______________ 。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为____________ (不考虑气体的溶解)。
(5)某工厂采用电解法处理含 Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为 Cr3+,Cr3+在阴极区生成 Cr(OH)3 沉淀除去,工作原理如图
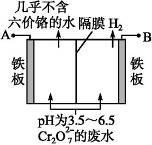
①写出电解时阴极的电极反应式______________________________ 。
②写出 Cr2O72-被还原为 Cr3+的离子方程式____________________________ 。

(1)甲装置中,a电极的反应式为
(2)乙装置中,阴极区产物为
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为
(5)某工厂采用电解法处理含 Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为 Cr3+,Cr3+在阴极区生成 Cr(OH)3 沉淀除去,工作原理如图

①写出电解时阴极的电极反应式
②写出 Cr2O72-被还原为 Cr3+的离子方程式
更新时间:2018-12-17 10:30:03
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】高锰酸钾广泛用作氧化剂。现有一个氧化还原反应的体系中共有KMnO4、MnSO4、H2O、Fe2(SO4)3、
FeSO4、H2SO4、K2SO4七种物质。
Ⅰ.写出一个包含上述七种物质的氧化还原反应方程式(需要配平):____________ 。
Ⅱ.某研究性学习小组根据上述反应设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol/L,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。
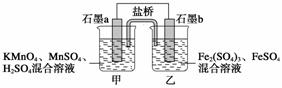
回答下列问题:
(1)此原电池的正极是石墨__________ (填“a”或“b”),发生________ 反应。
(2)电池工作时,盐桥中的SO42-移向________ (填“甲”或“乙”)烧杯。
(3)乙烧杯中的电极反应式分别为__________________ 。
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________ mol。
FeSO4、H2SO4、K2SO4七种物质。
Ⅰ.写出一个包含上述七种物质的氧化还原反应方程式(需要配平):
Ⅱ.某研究性学习小组根据上述反应设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol/L,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。

回答下列问题:
(1)此原电池的正极是石墨
(2)电池工作时,盐桥中的SO42-移向
(3)乙烧杯中的电极反应式分别为
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。

(1)若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:__________________________________ 。
②若在标准状况下有2.24 L NO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为__ mol。
(2)某小组在右室装有10 L 0.2 mol·L−1硝酸溶液,用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。
①实验前,配制10 L 0.2 mol·L−1硝酸溶液需量取____ mL、密度为1.4 g·mL−1、质量分数为63%的浓硝酸。
②电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中含3 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28 L H2。计算原气体中NO和NO2的体积比___ (假设尾气不含氮氧化物,写出计算过程)。

(1)若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:
②若在标准状况下有2.24 L NO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为
(2)某小组在右室装有10 L 0.2 mol·L−1硝酸溶液,用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。
①实验前,配制10 L 0.2 mol·L−1硝酸溶液需量取
②电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中含3 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28 L H2。计算原气体中NO和NO2的体积比
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】电化学在我们的生产、生活中占有越来越重要的地位。
(1)①燃料电池是一种绿色环保、高效的化学电源。下图为甲醇燃料电池,则负极反应式为_________ 。
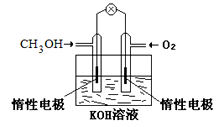
②常温下用甲醇燃料电池电解 饱和食盐水,则电解的化学方程式为
饱和食盐水,则电解的化学方程式为______ 。电解一段时间后,当溶液的 为13时,消耗
为13时,消耗 的质量为
的质量为_____ g。(忽略溶液体积变化,不考虑损耗)
③用甲醇燃料电池电解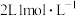 硫酸铜溶液,一段时间后,两极共收集到标准状况下的气体
硫酸铜溶液,一段时间后,两极共收集到标准状况下的气体 ,则电路中共转移
,则电路中共转移______  电子。
电子。
(2)利用电化学原理,将 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 废水,如图所示;电解过程中溶液发生反应:
废水,如图所示;电解过程中溶液发生反应: 。
。

左池工作时, 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用,则石墨Ⅱ附近发生的电极反应式为
,可循环使用,则石墨Ⅱ附近发生的电极反应式为________ 。
(1)①燃料电池是一种绿色环保、高效的化学电源。下图为甲醇燃料电池,则负极反应式为

②常温下用甲醇燃料电池电解
 饱和食盐水,则电解的化学方程式为
饱和食盐水,则电解的化学方程式为 为13时,消耗
为13时,消耗 的质量为
的质量为③用甲醇燃料电池电解
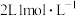 硫酸铜溶液,一段时间后,两极共收集到标准状况下的气体
硫酸铜溶液,一段时间后,两极共收集到标准状况下的气体 ,则电路中共转移
,则电路中共转移 电子。
电子。(2)利用电化学原理,将
 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 废水,如图所示;电解过程中溶液发生反应:
废水,如图所示;电解过程中溶液发生反应: 。
。
左池工作时,
 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用,则石墨Ⅱ附近发生的电极反应式为
,可循环使用,则石墨Ⅱ附近发生的电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入NH30.4mol,甲室中充入HCl、N2的混合气体,静止时隔板位置如图所示。已知甲、乙两室中气体的质量之差为17.3g。

(1)甲室中HCl、N2的质量之比为__________________ 。
(2)将隔板a去掉,一段时间后,隔板b将稳定位于刻度“________ ’’处(填数字,不考虑固体物质产生的压强),此时体系的平均相对分子质量为________ 。
Ⅱ.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
(1)表中硫酸的质量分数为________ (不写单位,用含c1、ρ1,的代数式表示)。
(2)物质的量浓度为c1 mol•L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为________ mol•L-1。
(3)将物质的量浓度分别为c2 mol•L-1和0.2c2 mol•L-1的氨水等质量混合,所得溶液的物质的量浓度__________ 0.6c2 mol•L-1(填“大于”、“小于”或“等于”)(设混合后溶液的体积变化忽略不计)
Ⅲ.电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。
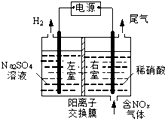
若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:_________________________________ 。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜的H+为________ mol。

(1)甲室中HCl、N2的质量之比为
(2)将隔板a去掉,一段时间后,隔板b将稳定位于刻度“
Ⅱ.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶质的物质的量浓度/mol•L-1 | 溶液的密度/g•cm-3 | |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为
(2)物质的量浓度为c1 mol•L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为
(3)将物质的量浓度分别为c2 mol•L-1和0.2c2 mol•L-1的氨水等质量混合,所得溶液的物质的量浓度
Ⅲ.电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。

若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜的H+为
您最近一年使用:0次
【推荐2】磷酸铁锂电池是指用磷酸铁锂(LiFePO4)作为正极材料的锂离子电池,属于一种新型锂离子二次电池,主要用作动力电池,具有安全性高、寿命长、容量大、高温性能好、无记忆效应和无污染等特点。磷酸铁锂可以由磷酸二氢锂、三氧化二铁和过量炭粉通过高温固相反应制备,反应中产生还产生H2O和CO。LiFePO4电池的工作原理是:电池充电时,正极(橄榄石结构的LiFePO4)部分转化为磷酸铁(设摩尔转化率为x),放出的锂离子(Li+)通过聚合物隔膜向负极(石墨)迁移,还原并嵌入石墨形成复合材料C6Lix;电池放电时,锂离子又从负极中脱出来,穿过隔膜回到正极材料中。(注:锂离子电池就是因锂离子在充放电时来回迁移而命名的,所以锂离子电池又称“摇椅电池”)
(1)请写出制备磷酸铁锂的化学方程式:___________
(2)请写出磷酸铁锂电池充电、放电时的总反应方程式:___________
(3)现有10g磷酸二氢锂,全部用于制备磷酸铁锂作为正极材料,则制成的磷酸铁锂电池理论上最多有多大的电池容量(即最大可放出多少电量)?答:___________ (mAh)。(注:1摩尔电子所带的电量约为96500库仑,3.6库仑=1mAh。)
(1)请写出制备磷酸铁锂的化学方程式:
(2)请写出磷酸铁锂电池充电、放电时的总反应方程式:
(3)现有10g磷酸二氢锂,全部用于制备磷酸铁锂作为正极材料,则制成的磷酸铁锂电池理论上最多有多大的电池容量(即最大可放出多少电量)?答:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】电化学知识给人类的生活和工业生产带来极大的方便。回答下列问题:
(1)碱性锌锰电池的总反应式为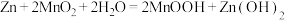 。负极材料为
。负极材料为___________ ,该电池正极反应式为___________ 。___________ 。
(3)用如图装置电解硫酸钾溶液,可获得H2、O2、硫酸和氢氧化钾溶液。X电极上发生的电极反应为___________ 。氢氧化钾溶液从___________ 口导出(填“A”或“D”),M、N交换膜中属于阳离子交换膜的是___________ (填“M”或“N”)。
(4)如图所示,若电解10min时,测得银电极的质量减少5.40g。试回答下列问题:___________ (填“正”或“负”)极。
②通电10min时,B中共收集到392mL(标准状况)气体,溶液体积为200mL(电解前后溶液的体积变化忽略不计),则通电前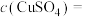
___________ mol/L,如果电解后要使该电解液复原,可以加入物质的化学式为___________ 。
(1)碱性锌锰电池的总反应式为
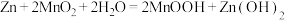 。负极材料为
。负极材料为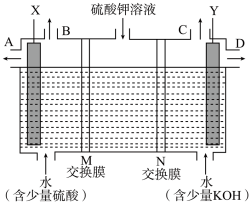
(3)用如图装置电解硫酸钾溶液,可获得H2、O2、硫酸和氢氧化钾溶液。X电极上发生的电极反应为
(4)如图所示,若电解10min时,测得银电极的质量减少5.40g。试回答下列问题:
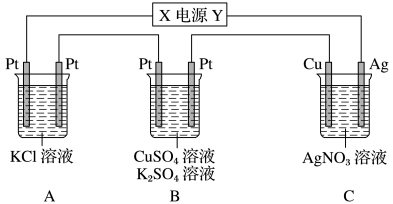
②通电10min时,B中共收集到392mL(标准状况)气体,溶液体积为200mL(电解前后溶液的体积变化忽略不计),则通电前
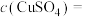
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】Al2O3、Al(OH)3都是重要化工原料。根据要求回答问题:
Ⅰ、电解法制高品质Al(OH)3装置如下(中间用离子交换膜隔开):
4Na[Al(OH)4]+2H2O 4Al(OH)3↓+4NaOH+O2↑+2H2↑
4Al(OH)3↓+4NaOH+O2↑+2H2↑
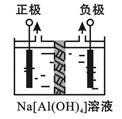
(1)产物Al(OH)3在___________ 区(填“阴极”或“阳极”)沉积;
(2)电解中转移2mol e-时,将制得___________ mol的Al(OH)3。
Ⅱ、制取纳米Al2O3需要纯净的硫酸铝。现有0.05mol·L-1硫酸铝溶液,经检测,含有Fe2+、Fe3+。可按下述操作提纯:往溶液中加足量H2O2充分反应,再用试剂X调节溶液pH=3.5.(室温下,0.1mol·L-1的Fe2+、Al3+开始沉淀的pH分别为7.0和3.7,Fe3+完全沉淀的pH=3.2)
(3)纳米氧化铝分散在分散剂中将形成胶体。则纳米氧化铝的直径约为___________ m。
(4)检验硫酸铝溶液含有Fe3+时,所采用的试剂及现象是___________ 。
(5)往溶液中加入H2O2的作用是___________ (用离子方程式表示)。
(6)加入的X试剂(填选项编号)是___________ 。
A.CuO B.Al(OH)3 C.NaOH D.NaHCO3
若调节后溶液的pH偏离3.5,可能带来的后果是___________ 。
Ⅰ、电解法制高品质Al(OH)3装置如下(中间用离子交换膜隔开):
4Na[Al(OH)4]+2H2O
 4Al(OH)3↓+4NaOH+O2↑+2H2↑
4Al(OH)3↓+4NaOH+O2↑+2H2↑
(1)产物Al(OH)3在
(2)电解中转移2mol e-时,将制得
Ⅱ、制取纳米Al2O3需要纯净的硫酸铝。现有0.05mol·L-1硫酸铝溶液,经检测,含有Fe2+、Fe3+。可按下述操作提纯:往溶液中加足量H2O2充分反应,再用试剂X调节溶液pH=3.5.(室温下,0.1mol·L-1的Fe2+、Al3+开始沉淀的pH分别为7.0和3.7,Fe3+完全沉淀的pH=3.2)
(3)纳米氧化铝分散在分散剂中将形成胶体。则纳米氧化铝的直径约为
(4)检验硫酸铝溶液含有Fe3+时,所采用的试剂及现象是
(5)往溶液中加入H2O2的作用是
(6)加入的X试剂(填选项编号)是
A.CuO B.Al(OH)3 C.NaOH D.NaHCO3
若调节后溶液的pH偏离3.5,可能带来的后果是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、CO、SO2等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。
Ⅰ.CO可用于合成甲醇
(1)已知CO、H2、CH3OH(g)的燃烧热△H分别为:-283.0kJ/mol、-285.8 kJ/mol、-764.5kJ/mol,则CO(g)+2H2(g) CH3OH(g)的△H=
CH3OH(g)的△H=________ 。
(2)将lmolCO和2molH2充入密闭容器中发生上述反应。其他条件相同时.CO的平衡转化率与压强(P)和温度(T)的关系如图所示。

① A、B两点CH3OH的质量分数ω(A)_____ ω(B )(填“>”、“<”或“=”)。
② C、D两点的逆反应速率:v(C)_____ v(D)(同上)。
③ 200℃ 时,测得E点的容器容积为10L。该温度下,反应的平街常数K=_______ ;保持温度和容积不变,再向容器中充入lmolCO、lmolH2和xmolCH3OH时,若使v正>v逆,则x的取值范围为________ 。
Ⅱ. CO2的综合利用
(3)CO2转化为甲醇有广泛应用前景。T℃时,在容积为lL的恒容密闭容器中,充入lmolCO2和3molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,达到平衡状态,其它条件不变,下列措施中能使
CH3OH(g)+H2O(g) △H<0,达到平衡状态,其它条件不变,下列措施中能使 增大的是
增大的是______ (填选项字母)。
A.升高温度 B.再充入1molCH3OH(g)和1molH2O(g)
C.加入催化剂 D.再充入一定量H2O
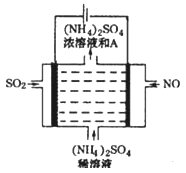
Ⅲ.(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_____ ,阴极的电极反应式是_____________ 。
Ⅰ.CO可用于合成甲醇
(1)已知CO、H2、CH3OH(g)的燃烧热△H分别为:-283.0kJ/mol、-285.8 kJ/mol、-764.5kJ/mol,则CO(g)+2H2(g)
 CH3OH(g)的△H=
CH3OH(g)的△H=(2)将lmolCO和2molH2充入密闭容器中发生上述反应。其他条件相同时.CO的平衡转化率与压强(P)和温度(T)的关系如图所示。

① A、B两点CH3OH的质量分数ω(A)
② C、D两点的逆反应速率:v(C)
③ 200℃ 时,测得E点的容器容积为10L。该温度下,反应的平街常数K=
Ⅱ. CO2的综合利用
(3)CO2转化为甲醇有广泛应用前景。T℃时,在容积为lL的恒容密闭容器中,充入lmolCO2和3molH2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0,达到平衡状态,其它条件不变,下列措施中能使
CH3OH(g)+H2O(g) △H<0,达到平衡状态,其它条件不变,下列措施中能使 增大的是
增大的是A.升高温度 B.再充入1molCH3OH(g)和1molH2O(g)
C.加入催化剂 D.再充入一定量H2O
Ⅲ.(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】根据电化学知识回答下列问题。
Ⅰ、某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。

(1)X极与电源的_____ (填正或负)极相连,氢气从____ (选填A、 B、C或D)口导出。
(2)离子交换膜只允许一类离子通过,则M为________ (填阴离子或阳离子,下同)交换膜,N为________ 交换膜。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池正极的电极反应式为___________________
Ⅱ、铅蓄电池是常见的二次电池,其放电反应和充电反应表示如下:Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
写出它放电时正极的电极反应式______________________________________ ;
充电时阴极的电极反应式______________________________________________ 。
Ⅰ、某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。

(1)X极与电源的
(2)离子交换膜只允许一类离子通过,则M为
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池正极的电极反应式为
Ⅱ、铅蓄电池是常见的二次电池,其放电反应和充电反应表示如下:Pb(s)+PbO2(s)+2H2SO4(aq)
 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)写出它放电时正极的电极反应式
充电时阴极的电极反应式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙烧杯中X为阳离子交换膜。请按要求回答相关问题:
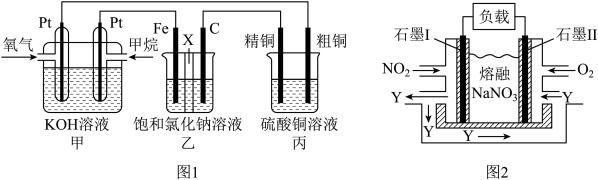
(1)甲烷燃料电池负极电极反应式是___________ ;正极电极反应式是___________________
(2)石墨(C)为__________ 极,其电极反应式为____________________________ ;乙中总反应的离子方程式为__________________________________________________
(3)若在标准状况下,有2.24 L氧气参加反应,则丙装置中阴极析出铜的质量为_________ g ;
(4)若将甲装置中的甲烷换成甲醇(CH3OH),KOH溶液换成稀硫酸,则负极电极反应式为___________ ,消耗等量氧气时,需要甲烷与甲醇的物质的量之比为_________ 。
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图2,该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为________________________________

(1)甲烷燃料电池负极电极反应式是
(2)石墨(C)为
(3)若在标准状况下,有2.24 L氧气参加反应,则丙装置中阴极析出铜的质量为
(4)若将甲装置中的甲烷换成甲醇(CH3OH),KOH溶液换成稀硫酸,则负极电极反应式为
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图2,该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】工业废水中常含有一定量有毒的 和
和 ,需进行处理后再排放。处理含
,需进行处理后再排放。处理含 和
和 的工业废水常用的方法有两种。
的工业废水常用的方法有两种。
方法一:还原沉淀法。
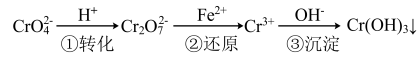
(1)请写出第①步中 与
与 在溶液中存在的平衡:
在溶液中存在的平衡:___________ ,下列能说明该反应达到平衡状态的是___________ (填标号)。
A. 与
与 的物质的量相等
的物质的量相等
B.溶液颜色不变
C.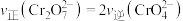
(2)第②步中,每 可还原
可还原___________  ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
方法二:电解法。用石墨和Fe作电极电解含 的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近
的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近 将
将 还原为
还原为 ,最后
,最后 以
以 形式沉淀。
形式沉淀。
(3)在电解除铬的过程中,石墨电极为___________ (填“阴极”或“阳极”),Fe电极的电极反应式为___________ 。
(4)在阴极附近溶液pH升高的原因是___________ (填电极反应式及必要的文字)。
(5)当Fe电极质量减小3.36g时,理论上可处理___________ (填含a的表达式)L含 的酸性废水。
的酸性废水。
 和
和 ,需进行处理后再排放。处理含
,需进行处理后再排放。处理含 和
和 的工业废水常用的方法有两种。
的工业废水常用的方法有两种。方法一:还原沉淀法。

(1)请写出第①步中
 与
与 在溶液中存在的平衡:
在溶液中存在的平衡:A.
 与
与 的物质的量相等
的物质的量相等B.溶液颜色不变
C.
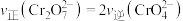
(2)第②步中,每
 可还原
可还原 ,该反应的离子方程式为
,该反应的离子方程式为方法二:电解法。用石墨和Fe作电极电解含
 的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近
的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近 将
将 还原为
还原为 ,最后
,最后 以
以 形式沉淀。
形式沉淀。(3)在电解除铬的过程中,石墨电极为
(4)在阴极附近溶液pH升高的原因是
(5)当Fe电极质量减小3.36g时,理论上可处理
 的酸性废水。
的酸性废水。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理, 其中乙装置中 X 为阳离子交换膜。
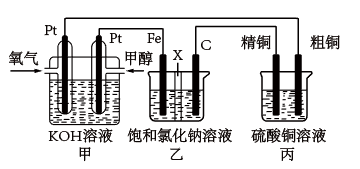
根据要求回答相关问题:
(1)写出负极的电极反应式_____
(2)写出石墨电极的电极反应式_____________
(3)反应一段时间后,乙装置中生成氢氧化钠主要在_________ (填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_________ ,反应一段时间,硫酸铜溶液浓度将_____ (填“增大”“减小”或“不变”)。
(5)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁电极上生成的气体的分子数目为_____ ;丙装置中阴极析出铜的质量为_____ 。

根据要求回答相关问题:
(1)写出负极的电极反应式
(2)写出石墨电极的电极反应式
(3)反应一段时间后,乙装置中生成氢氧化钠主要在
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为
(5)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁电极上生成的气体的分子数目为
您最近一年使用:0次



