下列有八种物质:
①CH4 ②CH3CH2OH ③N2 ④HCl ⑤CO2⑥CH3CH3 ⑦C2H4 ⑧C2H2。请按要求回答下列问题(填写编号):
(1)只有σ键的有________________ ,既有σ键又有π键的有__________ 。
(2)只含有极性键的化合物有______ ,既含有极性键,又含有非极性键的化合物有___ 。
(3)含有双键的有__________ ,含有叁键的有__________ 。
①CH4 ②CH3CH2OH ③N2 ④HCl ⑤CO2⑥CH3CH3 ⑦C2H4 ⑧C2H2。请按要求回答下列问题(填写编号):
(1)只有σ键的有
(2)只含有极性键的化合物有
(3)含有双键的有
18-19高二上·贵州安顺·阶段练习 查看更多[2]
更新时间:2018-12-18 15:03:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】含氯化合物有广泛的应用。
I.
(1)氯原子的核外有___________ 种能量不同的电子,氯化铵的电子式为___________ 。
(2)周期表中有3种主族元素与氯元素相邻,它们的气态氢化物的热稳定性由强至弱的顺序为___________ (用分子式表示)。通常状况下,Cl2、Br2、I2依次是气体、液体、固体,从结构的角度分析其原因:___________ 。
Ⅱ.ClO2是一种高效消毒剂,用KClO3和浓HCl可制得它:
(3)请完成该制备反应的化学方程式___________ 。
_______KClO3+____HCl(浓)=_____Cl2↑+_____ClO2↑+_____KCl+______。
若反应产生8.96LClO2(标准状况)时,则转移电子数为___________ 。
(4)Ca(ClO)2是漂白粉的有效成分,Ca(ClO)2中存在的化学键为___________ 。工业制漂白粉的气体原料来自于氯碱工业电解饱和食盐水设备的___________ (填电极名称)。
I.
(1)氯原子的核外有
(2)周期表中有3种主族元素与氯元素相邻,它们的气态氢化物的热稳定性由强至弱的顺序为
Ⅱ.ClO2是一种高效消毒剂,用KClO3和浓HCl可制得它:
(3)请完成该制备反应的化学方程式
_______KClO3+____HCl(浓)=_____Cl2↑+_____ClO2↑+_____KCl+______。
若反应产生8.96LClO2(标准状况)时,则转移电子数为
(4)Ca(ClO)2是漂白粉的有效成分,Ca(ClO)2中存在的化学键为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)有下列各组物质:A. 和
和 B.
B.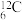 和
和 C.
C. 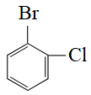 和
和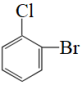 D.甲烷和新戊烷 E.
D.甲烷和新戊烷 E. 和
和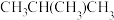 F.
F.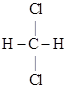 和
和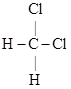 (填字母)
(填字母)
①_______ 组两物质间互为同位素。
②_______ 组两物质间互为同素异形体。
③_______ 组两物质属于同系物。
④_______ 组两物质互为同分异构体。
⑤_______ 组是同一物质。
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④ 溶于水、⑤
溶于水、⑤ 溶于水、⑥
溶于水、⑥ 溶于水、⑦
溶于水、⑦ 溶于水。仅破坏离子键的是
溶于水。仅破坏离子键的是_______ (填序号,下同);仅破坏共价键的是_______ ;既破坏离子键又破坏共价键的是_______ 。
(3)写出下列物质的电子式:
_______ ,
_______ 。
(1)有下列各组物质:A.
 和
和 B.
B.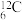 和
和 C.
C.  和
和 D.甲烷和新戊烷 E.
D.甲烷和新戊烷 E. 和
和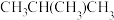 F.
F.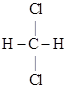 和
和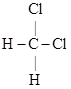 (填字母)
(填字母)①
②
③
④
⑤
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④
 溶于水、⑤
溶于水、⑤ 溶于水、⑥
溶于水、⑥ 溶于水、⑦
溶于水、⑦ 溶于水。仅破坏离子键的是
溶于水。仅破坏离子键的是(3)写出下列物质的电子式:


您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)有下列各组物质:A.O2和O3;B. 和
和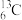 ;C.冰醋酸和乙酸:D.甲烷和庚烷;E.CH3CH2CH2CH3和CH3CH(CH3)CH3;F.淀粉和纤维素;G.
;C.冰醋酸和乙酸:D.甲烷和庚烷;E.CH3CH2CH2CH3和CH3CH(CH3)CH3;F.淀粉和纤维素;G. 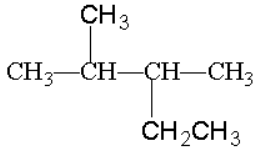 和
和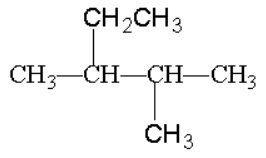 H.
H.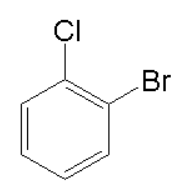 和
和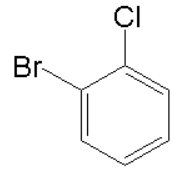 ,用序号填空:
,用序号填空:
①_________ 组两物质间互为同位素。
②_________ 组两物质间互为同素异形体。
③_________ 组两物质属于同系物。
④________ 组两物质互为同分异构体。
⑤_________ 组是同一物质。
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④H2SO4溶于水、⑤O2溶于水、⑥NaHSO4溶于水、⑦Na2O2溶于水,
未发生化学键破坏的是_________ ;(填序号,下同)仅破坏离子键的是 _________ ;仅破坏共价键的是 _________ ;既破坏离子键又破坏共价键的是 _________ 。
 和
和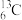 ;C.冰醋酸和乙酸:D.甲烷和庚烷;E.CH3CH2CH2CH3和CH3CH(CH3)CH3;F.淀粉和纤维素;G.
;C.冰醋酸和乙酸:D.甲烷和庚烷;E.CH3CH2CH2CH3和CH3CH(CH3)CH3;F.淀粉和纤维素;G.  和
和 H.
H. 和
和 ,用序号填空:
,用序号填空:①
②
③
④
⑤
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④H2SO4溶于水、⑤O2溶于水、⑥NaHSO4溶于水、⑦Na2O2溶于水,
未发生化学键破坏的是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮的化合物应用广泛。
(1)Reineckesalt的结构如图所示:
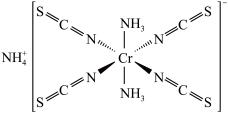
其中配位原子为___________ (填元素符号),阳离子的空间结构为___________ , 中碳原子杂化方式为
中碳原子杂化方式为___________ 。
(2)重铬酸铵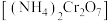 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
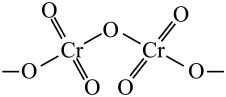
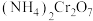 中N、O、Cr三种元素第一电离能由大到小的顺序是
中N、O、Cr三种元素第一电离能由大到小的顺序是___________ (填元素符号)
(3) 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物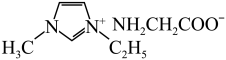 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是___________ 。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。
①下列微粒中存在“离域 键”的是
键”的是___________ 。
A. B.
B.  C.
C.  D.
D.
② 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为___________ 。
(5)符号“ ”没有给出的信息是___________。
”没有给出的信息是___________。
(6)下列实验事实不能用氢键来解释的是___________。
(1)Reineckesalt的结构如图所示:

其中配位原子为
 中碳原子杂化方式为
中碳原子杂化方式为(2)重铬酸铵
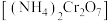 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
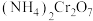 中N、O、Cr三种元素第一电离能由大到小的顺序是
中N、O、Cr三种元素第一电离能由大到小的顺序是(3)
 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物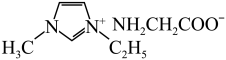 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。①下列微粒中存在“离域
 键”的是
键”的是A.
 B.
B.  C.
C.  D.
D.
②
 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为(5)符号“
 ”没有给出的信息是___________。
”没有给出的信息是___________。| A.能层 | B.能级 |
| C.电子云在空间的伸展方向 | D.电子的自旋方向 |
(6)下列实验事实不能用氢键来解释的是___________。
A. 比 比 稳定 稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.双氰胺结构简式如图。
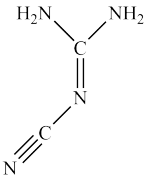
(1)双氰胺的晶体类型为_______ 。
(2)双氰胺所含元素中,_______ (填元素名称)元素基态原子核外未成对电子数最多。
(3)双氰胺分子中σ键和π键数目之比为_______ 。
Ⅱ.硼的最简单氢化物——乙硼烷球棍模型如下图,由它制取硼氢化锂的反应为2LiH+B2H6=2LiBH4
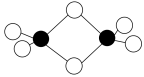
(4)乙硼烷分子中硼原子的杂化轨道类型为_______ 。
(5)BH 为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为
为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为_______ (填序号)。
A.离子键 B.金属键 C.氢键 D.配位键 E.极性键 F.非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为_______ (填元素符号)。
(7)碳的最简单氢化物是CH4,而硼的最简单氢化物不是BH3,其原因为_______ 。

(1)双氰胺的晶体类型为
(2)双氰胺所含元素中,
(3)双氰胺分子中σ键和π键数目之比为
Ⅱ.硼的最简单氢化物——乙硼烷球棍模型如下图,由它制取硼氢化锂的反应为2LiH+B2H6=2LiBH4

(4)乙硼烷分子中硼原子的杂化轨道类型为
(5)BH
 为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为
为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为A.离子键 B.金属键 C.氢键 D.配位键 E.极性键 F.非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为
(7)碳的最简单氢化物是CH4,而硼的最简单氢化物不是BH3,其原因为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】共价键参数的应用。
(1)键能的应用。
①表示共价键的强弱:键能越大,断开化学键时需要的能量越多,化学键_________ 。
②判断分子的稳定性:结构相似的分子中,共价键的_________ 越大,分子越稳定。
③判断化学反应的能量变化:在化学反应中,旧化学键的断裂吸收能量,新化学键的形成释放能量,因此反应焓变与键能的关系为ΔH=反应物键能总和一生成物键能总和;ΔH<0时,为放热反应;ΔH>0 时,为吸热反应。
(2)键长的应用。
①一般键长_________ ,键能越大,共价键越稳定,分子越稳定。
②键长的比较方法:
a.根据原子半径比较,同种类型的共价键,成键原子半径_________ ,键长越短。
b.根据共用电子对数比较,相同的两个原子间形成共价键时,_________ 。
(1)键能的应用。
①表示共价键的强弱:键能越大,断开化学键时需要的能量越多,化学键
②判断分子的稳定性:结构相似的分子中,共价键的
③判断化学反应的能量变化:在化学反应中,旧化学键的断裂吸收能量,新化学键的形成释放能量,因此反应焓变与键能的关系为ΔH=反应物键能总和一生成物键能总和;ΔH<0时,为放热反应;ΔH>0 时,为吸热反应。
(2)键长的应用。
①一般键长
②键长的比较方法:
a.根据原子半径比较,同种类型的共价键,成键原子半径
b.根据共用电子对数比较,相同的两个原子间形成共价键时,
您最近半年使用:0次



