有M、N两种溶液,经测定这两种溶液中含有下列12种离子:Al3+、Cl-、Na+、K+、NO3-、OH-、Fe2+、AlO2-、CO32-、NH4+、SO42-、H+。
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:_____________ 、_________________

(2)根据(1)中的实验回答:
NO3-存在于________ 溶液中,理由是___________________________________________ ;
Cl-存在于________ 溶液中,理由是__________________________________________ 。
(3)根据(1)中的实验确定,M溶液中含有的离子为__________________________________
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:

(2)根据(1)中的实验回答:
NO3-存在于
Cl-存在于
(3)根据(1)中的实验确定,M溶液中含有的离子为
更新时间:2018-12-19 08:49:51
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行实验,实验内容如下:
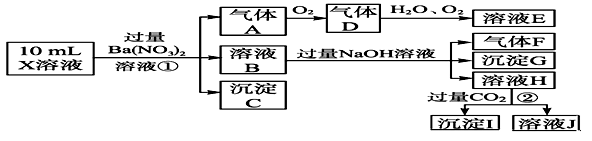
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是______________________________ ;
(2)写出有关离子方程式:
步骤①中生成A__________________ ;步骤②生成沉淀I__________________ 。
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,若沉淀C物质的量大于0.07 mol,溶液X中还一定含有的离子是______ ;若而沉淀C物质的量小于0.07 mol,溶液X中还一定含有的离子是______ 。

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是
(2)写出有关离子方程式:
步骤①中生成A
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,若沉淀C物质的量大于0.07 mol,溶液X中还一定含有的离子是
您最近半年使用:0次
【推荐2】(1)NaHSO4是一种酸式盐。2mol/L的NaHSO4溶液与1mol/L的Ba(OH)2溶液等体积混合,反应的离子方程式为__________________________ 。
(2)写出Na与FeCl3溶液的反应的离子反应方程式:_________________________________
(3)乙同学检测到该溶液中含有大量的Cl﹣、Br﹣、I﹣,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl﹣、Br﹣、I﹣的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
原溶液中Cl﹣、Br﹣、I﹣的物质的量浓度之比为______________ .
(2)写出Na与FeCl3溶液的反应的离子反应方程式:
(3)乙同学检测到该溶液中含有大量的Cl﹣、Br﹣、I﹣,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl﹣、Br﹣、I﹣的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
| Cl2的体积(标准状况) | 11.2L | 22.4L | 28.0L |
| n(Cl﹣) | 2.5mol | 3.5mol | 4.0mol |
| n(Br﹣) | 3.0mol | 2.5mol | 2.0mol |
| n(I﹣) | x mol | 0 | 0 |
原溶液中Cl﹣、Br﹣、I﹣的物质的量浓度之比为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】工厂化验员检验某含有KBrO3、KBr及惰性物的样品。化验员称取了该固体样品1.000 g,加水溶解后配成100 mL溶液X。
Ⅰ. 取25.00 mL溶液X,加入稀硫酸,然后用Na2SO3将BrO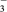 还原为Br-;
还原为Br-;
Ⅱ. 去除过量的SO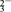 后调至中性;
后调至中性;
Ⅲ. 加入K2CrO4作指示剂,用0.100 0 mol·L-1AgNO3标准溶液滴定Br-至终点,消耗 AgNO3标准溶液11.25 mL;
Ⅳ. 另取25.00 mL溶液X,酸化后加热,再用碱液调至中性,测定过剩Br-,消耗上述AgNO3标准溶液3.75 mL。
已知:①25 ℃时,Ag2CrO4(砖红色)的Ksp=1.12×10-12,AgBr(浅黄色)的Ksp=5.0×
10-15;
②Ⅳ中酸化时发生反应:BrO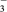 +5Br-+6H+=== 3Br2+3H2O
+5Br-+6H+=== 3Br2+3H2O
请回答:
(1)步骤Ⅰ中,反应的离子方程式为________________________________ 。
(2)步骤Ⅲ中,滴定终点的现象为_____________________________________________ 。
(3)步骤Ⅳ中,加热的目的是________________________ 。
(4)计算试样中KBrO3质量分数。(写出计算过程,结果保留3位有效数字)_______________
Ⅰ. 取25.00 mL溶液X,加入稀硫酸,然后用Na2SO3将BrO
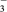 还原为Br-;
还原为Br-;Ⅱ. 去除过量的SO
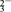 后调至中性;
后调至中性;Ⅲ. 加入K2CrO4作指示剂,用0.100 0 mol·L-1AgNO3标准溶液滴定Br-至终点,消耗 AgNO3标准溶液11.25 mL;
Ⅳ. 另取25.00 mL溶液X,酸化后加热,再用碱液调至中性,测定过剩Br-,消耗上述AgNO3标准溶液3.75 mL。
已知:①25 ℃时,Ag2CrO4(砖红色)的Ksp=1.12×10-12,AgBr(浅黄色)的Ksp=5.0×
10-15;
②Ⅳ中酸化时发生反应:BrO
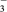 +5Br-+6H+=== 3Br2+3H2O
+5Br-+6H+=== 3Br2+3H2O请回答:
(1)步骤Ⅰ中,反应的离子方程式为
(2)步骤Ⅲ中,滴定终点的现象为
(3)步骤Ⅳ中,加热的目的是
(4)计算试样中KBrO3质量分数。(写出计算过程,结果保留3位有效数字)
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】当温度和压强一定时,向KOH、Ba(OH)2混合溶液中通入足量的CO2气体,随CO2的通入生成的沉淀质量如图所示:
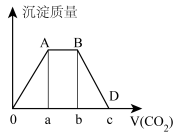
(1)根据图象可知,随着CO2通入KOH、Ba(OH)2混合溶液,反应分多个阶段,0A阶段的离子反应方程式:___________ ;
(2)随着CO2的通入,(不考虑CO2在溶液中的溶解,忽略溶液体积的微小变化)混合溶液的导电性会发生一些变化,导电性:0点___________ D点(填“大于”、“等于”或“小于”);
(3)0A段和BD段消耗CO2用量的关系:___________ (用a、b和c表示);
(4)原溶液中Ba2+和K+的个数之比:___________ (用a、b和c表示)。

(1)根据图象可知,随着CO2通入KOH、Ba(OH)2混合溶液,反应分多个阶段,0A阶段的离子反应方程式:
(2)随着CO2的通入,(不考虑CO2在溶液中的溶解,忽略溶液体积的微小变化)混合溶液的导电性会发生一些变化,导电性:0点
(3)0A段和BD段消耗CO2用量的关系:
(4)原溶液中Ba2+和K+的个数之比:
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】回答下列问题
(1)实验室有瓶标签已损坏的白色固体纯净物,要确定其化学式,有如下操作:
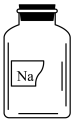
A.取少量固体在试管中加热,一段时间后称量,质量不变
B.待试管冷却后,滴加几滴水,固体结块,试管壁变热
C.再加水使固体完全溶解,将溶液分成两份,一份滴入1~2滴酚酰,溶液变红,说明该溶液显_______ ;一份逐滴加入盐酸,开始无气体,后产生无色无味能使澄清石灰水变浑浊的气体。该固体化学式为_______ 。
(2)硅酸盐种类繁多,结构复杂,通常用二氧化硅和金属氧化物的组合形式表示其组成,例如:硅酸钠: ,已知长石的化学式为:
,已知长石的化学式为: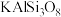 ,其写成氧化物形式为
,其写成氧化物形式为_______ 。
(3)某市售净水剂化学式为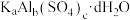 ,要确定其化学组成,可进行如下操作:
,要确定其化学组成,可进行如下操作:
A.取19.2g样品加热至恒重,使结晶水失去,得到13.8g固体
B.将所得固体溶于水,配成100mL溶液
C.取50mL加入足量 溶液,经过滤、洗涤、干燥后,得到
溶液,经过滤、洗涤、干燥后,得到 固体
固体
D.另取50mL溶液,加入足量氨水,过滤、洗涤后,将固体加热至恒重,得到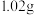 固体
固体
①若要确定该净水剂中的 ,可做
,可做_______ ,现象为_______
②“D”操作中“将固体加热至恒重”所发生的反应为_______
③通过实验数据确定该净水剂化学式为_______
(1)实验室有瓶标签已损坏的白色固体纯净物,要确定其化学式,有如下操作:

A.取少量固体在试管中加热,一段时间后称量,质量不变
B.待试管冷却后,滴加几滴水,固体结块,试管壁变热
C.再加水使固体完全溶解,将溶液分成两份,一份滴入1~2滴酚酰,溶液变红,说明该溶液显
(2)硅酸盐种类繁多,结构复杂,通常用二氧化硅和金属氧化物的组合形式表示其组成,例如:硅酸钠:
 ,已知长石的化学式为:
,已知长石的化学式为: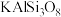 ,其写成氧化物形式为
,其写成氧化物形式为(3)某市售净水剂化学式为
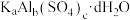 ,要确定其化学组成,可进行如下操作:
,要确定其化学组成,可进行如下操作:A.取19.2g样品加热至恒重,使结晶水失去,得到13.8g固体
B.将所得固体溶于水,配成100mL溶液
C.取50mL加入足量
 溶液,经过滤、洗涤、干燥后,得到
溶液,经过滤、洗涤、干燥后,得到 固体
固体D.另取50mL溶液,加入足量氨水,过滤、洗涤后,将固体加热至恒重,得到
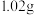 固体
固体①若要确定该净水剂中的
 ,可做
,可做②“D”操作中“将固体加热至恒重”所发生的反应为
③通过实验数据确定该净水剂化学式为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】有甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、CO32-、SO42-中的不同阴、阳离子各一种组成,已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L 乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)它们的化学式分别为甲_________ 、乙_________ 、丁_________ 。
(2)写出甲溶液和丁溶液反应的离子方程式:_________________________________ 。
(1)它们的化学式分别为甲
(2)写出甲溶液和丁溶液反应的离子方程式:
您最近半年使用:0次



