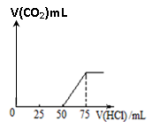
取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1mol/L的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:
(1)A溶液中的溶质为_________ (化学式),其物质的量之比是_______ 。
(2)通入CO2气体体积__________________ (标准状况)。
(3)NaOH溶液的物质的量浓度______________________ 。
(4)假如通入的CO2气体为112mL, 画出得到溶液逐滴缓慢加入0.1mol/L的HCl溶液体积,与产生的CO2气体体积(标准状况)的关系图________________ 。(应体现关键点的数据)
(1)A溶液中的溶质为
(2)通入CO2气体体积
(3)NaOH溶液的物质的量浓度
(4)假如通入的CO2气体为112mL, 画出得到溶液逐滴缓慢加入0.1mol/L的HCl溶液体积,与产生的CO2气体体积(标准状况)的关系图
更新时间:2018-12-30 07:38:55
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打每片含0.50gNaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是 mol
(2)胃舒平每片含0.245gAl(OH)3.中和胃酸时,6片小苏打相当于胃舒平 片
(3)达喜的化学成分是铝和镁的碱式盐:
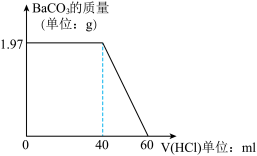
取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时正好完全反应,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比
(1)小苏打每片含0.50gNaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是 mol
(2)胃舒平每片含0.245gAl(OH)3.中和胃酸时,6片小苏打相当于胃舒平 片
(3)达喜的化学成分是铝和镁的碱式盐:
取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时正好完全反应,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取质量为27.4g的Na2CO3和NaHCO3的固体混合物,与200mL 2.00mol·L-1的盐酸恰好完全反应不再放出气体。
(1)原混合物中Na2CO3的质量为_____ g。
(2)若取等质量的原混合物配成溶液,逐滴滴入125mL 2.00mol·L-1的盐酸,并不断搅拌,则生成的气体在标准状况下的体积为____ L 。
(1)原混合物中Na2CO3的质量为
(2)若取等质量的原混合物配成溶液,逐滴滴入125mL 2.00mol·L-1的盐酸,并不断搅拌,则生成的气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】将在空气中暴露一段时间后的氢氧化钠固体样品溶于水得溶液A,将所得溶液中遂滴滴加稀硫酸至过量,生成的二氧化碳体积(标准状况下)与加入稀硫酸体积关系如图所示。

(1)溶液A中滴加硫酸的体积在0-150mL间无CO2气体生成的原因是(用化学方程式表示)_________________________________________________________ ;
(2)硫酸滴加至150mL时溶液中溶质主要成分为(写化学式)_______________ ;
(3)溶液A中碳酸钠的质量为____ g;
(4)硫酸的物质的量浓度为______ mol/L。
(5)该样品中Na2CO3与NaOH物质的量之比为________ 。

(1)溶液A中滴加硫酸的体积在0-150mL间无CO2气体生成的原因是(用化学方程式表示)
(2)硫酸滴加至150mL时溶液中溶质主要成分为(写化学式)
(3)溶液A中碳酸钠的质量为
(4)硫酸的物质的量浓度为
(5)该样品中Na2CO3与NaOH物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】取一定物质的量浓度的NaOH溶液100mL,然后向其中通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1mol/L的HCl溶液,产生CO2的气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:

(1)A溶液中的溶质为(化学式)___ 。
(2)ab段反应的离子方程式为___ 。
(3)通入CO2气体体积为___ mL(标准状况)。
(4)原NaOH溶液的物质的量浓度为___ 。

(1)A溶液中的溶质为(化学式)
(2)ab段反应的离子方程式为
(3)通入CO2气体体积为
(4)原NaOH溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】已知:①碳酸钠高温下不分解;②碳酸氢钠受热发生分解反应:2NaHCO3 Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:
Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:
(1)原混合物中碳酸钠的质量是_______ g。
(2)在剩余固体中,加入过量盐酸,反应后放出二氧化碳的体积(标准状况)是_______ L。
 Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:
Na2CO3+H2O+CO2↑。充分加热碳酸钠和碳酸氢钠的混合物19 g,完全反应后固体质量减轻了3.1 g,求:(1)原混合物中碳酸钠的质量是
(2)在剩余固体中,加入过量盐酸,反应后放出二氧化碳的体积(标准状况)是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3,反应的化学方程式为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl。然后再将NaHCO3制成Na2CO3。

(1)装置乙的作用是__________ 。为防止污染空气,尾气中含有的_____ 需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有__________ 。NaHCO3转化为Na2CO3的化学方程式为___________ 。
(3)若在⑵中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。
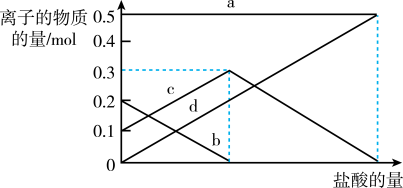
则曲线c对应的溶液中的离子是______ (填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是_____ 。
(4)若取21.0 g NaHCO3固体,加热了t2 min后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol·L-1的盐酸中则充分反应后溶液中H+ 的物质的量浓度为_________ (设溶液体积变化忽略不计)。

(1)装置乙的作用是
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
(3)若在⑵中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。

则曲线c对应的溶液中的离子是
(4)若取21.0 g NaHCO3固体,加热了t2 min后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol·L-1的盐酸中则充分反应后溶液中H+ 的物质的量浓度为
您最近一年使用:0次