热激活电池可用作火箭、导弹的工作电源。一种热激活电池基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列说法正确的是
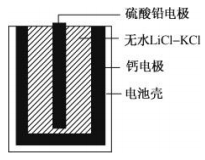

| A.放电过程中,Li+向负极移动 |
| B.正极反应式:Ca+2Cl-—2e-=CaCl2 |
| C.每转移0.1mol电子,理论上生成10.35gPb |
| D.常温时,在正负极间接上电流表或检流计,指针偏转 |
更新时间:2019-01-10 17:16:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】第三周期元素的单质及其化合物具有重要用途。在熔融状态下,可用金属钠制备金属钾;MgCl2可制备多种镁产品;Al-空气电池具有较高的比能量,在碱性电解液中总反应式为4Al+3O2+6H2O=4[Al(OH)4]-;高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷(SiHCl3),再经H2还原得到高纯硅。下列化学反应的表示方法正确的是
| A.钠与水反应的离子方程式:Na+H2O=Na++2OH-+H2↑ |
| B.MgCl2溶液显酸性的原因:Mg2++2H2O=Mg(OH)2↓+2H+ |
| C.该Al-空气电池的负极反应式:Al-3e-+3OH-=Al(OH)3 |
D.SiHCl3转化为高纯硅的化学方程式:SiHCl3+H2 Si+3HCl Si+3HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】如图所示装置,一段时间后右侧电极质量增加,下列叙述错误的是
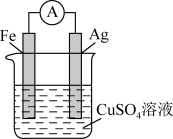

| A.该装置能将化学能转化为电能 | B.铁为负极,发生氧化反应 |
| C.电流从铁电极经导线流向银电极 | D.正极电极反应式为Cu2++2e-=Cu |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】电化学在日常生活中用途广泛,如图是镁次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,下列说法不正确的是( )
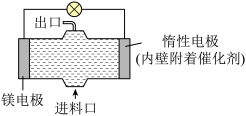

| A.镁电极是该电池的负极 | B.惰性电极上发生氧化反应 |
| C.正极反应式为ClO-+H2O+2e-═Cl-+2OH- | D.进料口加入NaClO溶液,出口为NaCl溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以金属氢化物(MHx)为负极材料的Ni/MHx电池,其充放电原理利用了储氢合金的吸放氢性能,氢通过碱性电解液在金属氢化物电极和Ni(OH)2电极之间运动,充放电过程中的氢像摇椅一样在电池的正负极之间摇动,因此又称为“摇椅”机理,其反应机理如图所示。下列说法错误 的是


| A.过程a表示电池充电过程 |
B.电池总反应:MHx+xNiOOH M+xNi(OH)2 M+xNi(OH)2 |
| C.放电时负极的电极反应:MHx+xOH−−xe−=M+xH2O |
| D.放电时正极的电极反应:NiOOH+H2O+e−=Ni(OH)2+OH− |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】NaBH4燃料电池具有理论电压高、能量密度大等优点。已知,能量密度=电池输出电能/燃料质量(已知电子的电荷量为1.6×10-19C),以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是
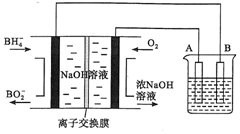

| A.每消耗2.24 L O2(标准状况)时,A电极的质量减轻12.8 g |
| B.离子交换膜应为阳离子交换膜,Na+由左极室向右极室迁移 |
| C.该燃料电池的负极反应式为BH4-+8OH--8e-=BO2- + 6H2O |
| D.若NaBH4 燃料电池的电压为U伏,则此电池的能量密度为2.03×104UkJ·kg-1 |
您最近一年使用:0次

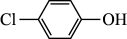 ),其原理如图所示,下列说法错误的是
),其原理如图所示,下列说法错误的是
 、
、 均能与氯化铁溶液发生显色反应
均能与氯化铁溶液发生显色反应 ,电路中通过的电子数为8NA
,电路中通过的电子数为8NA

