化学就在我们身边,它与我们的日常生活密切相关。按要求回答以下问题:
(1)明矾是__________________ ,漂白粉的有效成分是________ (均填化学式)。
(2)用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是________________________________________ (用化学方程式表示)。
(3)绿柱石(绿宝石)矿藏其主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO·Al2O3·6SiO2,其n值为_______ 。
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是___________________ 。
(5)SiO2广泛存在于自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学反应方程式:_________________ 。
(1)明矾是
(2)用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是
(3)绿柱石(绿宝石)矿藏其主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO·Al2O3·6SiO2,其n值为
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是
(5)SiO2广泛存在于自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学反应方程式:
更新时间:2019-02-02 11:04:32
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有物质:①酒精②NaCl固体③SO3④Na2CO3溶液⑤熔融K2SO4⑥CaO⑦CH3COOH⑧银⑨新制氯水⑩CO2⑪)稀硫酸⑫NaOH溶液。
回答下列问题:
(1)上述物质属于盐的是________ (填序号,下同)。
(2)上述物质属于电解质的是________ 。
(3)上述物质属于酸性氧化物的是________ 。
(4)足量的⑩通入少量的⑫中发生反应的离子方程式为________ 。
(5)④和足量⑪发生反应的离子方程式为_________ 。
(6)将⑨滴到pH试纸上的现象是________ ,说明了该溶液具有________ 。
回答下列问题:
(1)上述物质属于盐的是
(2)上述物质属于电解质的是
(3)上述物质属于酸性氧化物的是
(4)足量的⑩通入少量的⑫中发生反应的离子方程式为
(5)④和足量⑪发生反应的离子方程式为
(6)将⑨滴到pH试纸上的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯水中含有多种成分,因而具有多种性质。根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
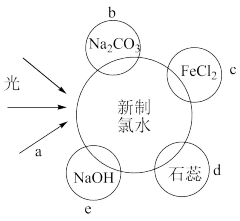
(1)新制氯水的成分有分子:_______ ;离子:_______ ;久置的氯水最终变为_______ ;
(2)b过程中有气泡产生,该气体是_______ ;
(3)c溶液的颜色变化为_______ ;e过程中所发生的主要反应的化学方程式为_______ ;
(4)d的现象为_______ 。

(1)新制氯水的成分有分子:
(2)b过程中有气泡产生,该气体是
(3)c溶液的颜色变化为
(4)d的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Cl2是一种重要的化工原料,如图是一些含氯产品。
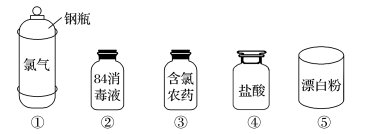
(1)①中钢瓶上应贴的标签为___ (填字母,下同)。
A.腐蚀品 B.爆炸品 C.有毒品 D.易燃品
(2)下列有关漂白粉和84消毒液的说法正确的是___ 。
A.漂白粉是纯净物,84消毒液是混合物
B.84消毒液的有效成分是NaClO
制84消毒液反应方程式为___ 。
(3)工业上利用Cl2制取盐酸,其化学方程式为___ 。Cl2溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是___ 。
A.硝酸银溶液 B.酚酞溶液 C.碳酸钠溶液 D.紫色石蕊溶液

(1)①中钢瓶上应贴的标签为
A.腐蚀品 B.爆炸品 C.有毒品 D.易燃品
(2)下列有关漂白粉和84消毒液的说法正确的是
A.漂白粉是纯净物,84消毒液是混合物
B.84消毒液的有效成分是NaClO
制84消毒液反应方程式为
(3)工业上利用Cl2制取盐酸,其化学方程式为
A.硝酸银溶液 B.酚酞溶液 C.碳酸钠溶液 D.紫色石蕊溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】
(1)某建筑材料,主要成分铝硅酸盐,化学式MgAl2H4Si4O14,化学式改写成氧化物形式为_____________ 。则材料该与足量的氢氧化钠反应后过滤,滤渣主要是______ .写出该过程中发生的离子方程式_______________________________ 、_______________________________________ 。
(2)检验CO2中是否混有SO2可将气体通过盛有______ 的洗气瓶.
(3)鉴别Na2CO3和NaHCO3溶液可选用______ (填序号).
①NaOH ②Ca(OH)2 ③BaCl2 ④K2SO4 ⑤Ca(NO3)2
(4)某溶液中有NH4+,Mg2+,Fe2+,Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是______ .
A.NH B.Mg2+ C.Fe2+ D.Al3+
B.Mg2+ C.Fe2+ D.Al3+
(5)6.4gCu与过量硝酸(60mL 8mol/L)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+为n mol,NO、NO2混合气体的物质的量为________________ 。
(1)某建筑材料,主要成分铝硅酸盐,化学式MgAl2H4Si4O14,化学式改写成氧化物形式为
(2)检验CO2中是否混有SO2可将气体通过盛有
(3)鉴别Na2CO3和NaHCO3溶液可选用
①NaOH ②Ca(OH)2 ③BaCl2 ④K2SO4 ⑤Ca(NO3)2
(4)某溶液中有NH4+,Mg2+,Fe2+,Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
A.NH
 B.Mg2+ C.Fe2+ D.Al3+
B.Mg2+ C.Fe2+ D.Al3+(5)6.4gCu与过量硝酸(60mL 8mol/L)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+为n mol,NO、NO2混合气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学是一门以实验为基础的自然科学。根据题意回答下列问题:
(1)盛装NaOH的溶液的试剂瓶不用玻璃塞,是因为玻璃中的SiO2和NaOH反应,导致难以打开瓶塞。该反应的化学方程式为 SiO2 + 2NaOH == Na2SiO3 +_______________ ;
(2)检验某溶液中是否含有SO42—,先加盐酸,再加_______________ (填“BaCl2”或“NaCl”);
(3)要使AlCl3溶液中的Al3+全部沉淀,应加入过量的____________ (填“氨水”或“氢氧化钠溶液”)
(1)盛装NaOH的溶液的试剂瓶不用玻璃塞,是因为玻璃中的SiO2和NaOH反应,导致难以打开瓶塞。该反应的化学方程式为 SiO2 + 2NaOH == Na2SiO3 +
(2)检验某溶液中是否含有SO42—,先加盐酸,再加
(3)要使AlCl3溶液中的Al3+全部沉淀,应加入过量的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
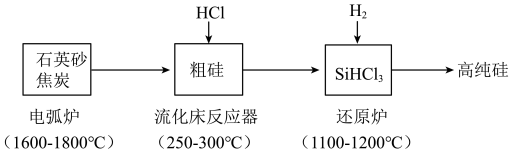
【推荐3】高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:___________ 。当有 C参与反应时,该反应转移的电子数目是
C参与反应时,该反应转移的电子数目是___________ 。
(2)还原炉中发生的化学反应方程式为:___________ 。
(3)上述工艺生产中循环使用的物质除Si、 外,还有
外,还有___________ 。
(4)关于硅及其相关化合物的叙述正确的是___________。
 C参与反应时,该反应转移的电子数目是
C参与反应时,该反应转移的电子数目是(2)还原炉中发生的化学反应方程式为:
(3)上述工艺生产中循环使用的物质除Si、
 外,还有
外,还有(4)关于硅及其相关化合物的叙述正确的是___________。
| A.自然界中存在天然游离的硅单质 |
B.光导纤维的主要成分是 |
C.已知C与Si属于主族元素,由于 ,用类比法得知, ,用类比法得知,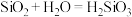 |
| D.硅酸钠的水溶液俗称水玻璃,具有粘性和耐高温,可以作为木材的粘合剂和防火材料 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请按要求书写下列离子方程式:
(1)将NaHSO4溶液滴入Ba(OH)2溶液中,当溶液恰好呈中性时,反应的离子方程式为___ 。
(2)向Ba(HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,写出反应的离子方程式:___ 。
(3)0.2mol·L-1的NH4Al(SO4)2溶液与0.3mol·L-1的Ba(OH)2溶液等体积混合:___ 。
(1)将NaHSO4溶液滴入Ba(OH)2溶液中,当溶液恰好呈中性时,反应的离子方程式为
(2)向Ba(HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,写出反应的离子方程式:
(3)0.2mol·L-1的NH4Al(SO4)2溶液与0.3mol·L-1的Ba(OH)2溶液等体积混合:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空:
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水。
i.其中能导电的是(填编号,下同):________ ;属于电解质的是________ ;属于非电解质的是:________ ;写出与②互为同素异形体的物质________ ;
ii.请写出③和⑨的离子反应方程式________________ 。
(2)实验室制备Fe(OH)3胶体的化学方程式为________________ 。
(3)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为________________ 。
(4)KA1(SO4)2•12H2O的俗名为________ ,因其溶于水生成________ (化学式)可以吸附杂质,从而达到净水作用。
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水。
i.其中能导电的是(填编号,下同):
ii.请写出③和⑨的离子反应方程式
(2)实验室制备Fe(OH)3胶体的化学方程式为
(3)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为
(4)KA1(SO4)2•12H2O的俗名为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学与人类生活密切相关。请按要求,回答下列问题:
(1)漂白粉有效成分的化学式为_____ ,其能消毒杀菌是因有强_____ 性。
(2)KAl(SO4)2•12H2O的俗名为_____ ,因其溶于水生成_____ 而具有净水作用。
(3)酸雨的pH小于_____ ,含亚硫酸的酸雨久置后pH_____ (增大、减小或不变)。
(4)小苏打可用于治疗胃酸过多,其反应的离子方程式为_____ 。
(1)漂白粉有效成分的化学式为
(2)KAl(SO4)2•12H2O的俗名为
(3)酸雨的pH小于
(4)小苏打可用于治疗胃酸过多,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业上以硫铁矿烧渣(主要成分为 、
、 ,含少量难溶杂质)为主要原料制备铁红(
,含少量难溶杂质)为主要原料制备铁红( )步骤如下。
)步骤如下。
(1)酸浸:用硫酸溶液浸取烧渣中的铁元素。若其他条件不变,下列措施中能提高单位时间内铁元素浸出率的有_______ (填序号)。
A.适当升高温度B.适当加快搅拌速率C.适当减小硫酸浓度
(2)沉铁:取 “酸浸”后的滤液并加入
“酸浸”后的滤液并加入 ,改变氨水用量,测得铁的沉淀率随氨水用量的变化如图。
,改变氨水用量,测得铁的沉淀率随氨水用量的变化如图。_______ 。
②氨水用量小于 时,铁的沉淀率变化幅度很小,其原因可能为(不考虑氨水与
时,铁的沉淀率变化幅度很小,其原因可能为(不考虑氨水与 反应)
反应)_______ 。
(3)过滤:“沉铁”后过滤,滤渣中含有 和
和 ,滤液中浓度最大的阳离子是
,滤液中浓度最大的阳离子是_______ (填化学式)。
(4)焙烧: 和
和 高温焙烧后均可得到铁红,反应的化学方程式分别为:
高温焙烧后均可得到铁红,反应的化学方程式分别为:_______ ;_______ 。
 、
、 ,含少量难溶杂质)为主要原料制备铁红(
,含少量难溶杂质)为主要原料制备铁红( )步骤如下。
)步骤如下。(1)酸浸:用硫酸溶液浸取烧渣中的铁元素。若其他条件不变,下列措施中能提高单位时间内铁元素浸出率的有
A.适当升高温度B.适当加快搅拌速率C.适当减小硫酸浓度
(2)沉铁:取
 “酸浸”后的滤液并加入
“酸浸”后的滤液并加入 ,改变氨水用量,测得铁的沉淀率随氨水用量的变化如图。
,改变氨水用量,测得铁的沉淀率随氨水用量的变化如图。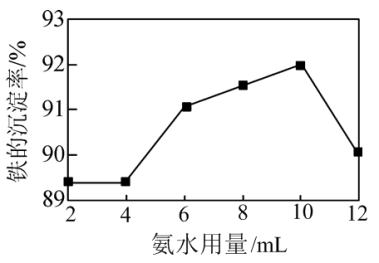
②氨水用量小于
 时,铁的沉淀率变化幅度很小,其原因可能为(不考虑氨水与
时,铁的沉淀率变化幅度很小,其原因可能为(不考虑氨水与 反应)
反应)(3)过滤:“沉铁”后过滤,滤渣中含有
 和
和 ,滤液中浓度最大的阳离子是
,滤液中浓度最大的阳离子是(4)焙烧:
 和
和 高温焙烧后均可得到铁红,反应的化学方程式分别为:
高温焙烧后均可得到铁红,反应的化学方程式分别为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】分别含有下列离子的五种溶液①Ag+ ②Mg2+ ③Fe2+ ④Al3+ ⑤Fe3+
试用标号 回答下列问题:
(1)既能被氧化又能被还原的离子是___________________
(2)向③中加入NaOH溶液,现象是____________________
(3)加入过量NaOH溶液无沉淀的是_____________________________
(4)加铁粉溶液质量增重的是_________ ,溶液质量减轻的___________
(5)遇KSCN溶液呈红色的是_________________________
(6)能用来鉴别Cl–存在的离子是___________
试用
(1)既能被氧化又能被还原的离子是
(2)向③中加入NaOH溶液,现象是
(3)加入过量NaOH溶液无沉淀的是
(4)加铁粉溶液质量增重的是
(5)遇KSCN溶液呈红色的是
(6)能用来鉴别Cl–存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用。某博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
铁器在具有O2、________ 等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
①Fe转化为Fe2+。
②Fe2+在自然环境中形成FeO(OH),该物质中铁元素的化合价为________ 。
③2 mol FeO(OH)和1 mol Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是______ (填字母)。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
④Fe3O4保护层被氧化为FeO(OH),如此往复腐蚀:(将反应补充完全)。
___ Fe3O4+____ O2+____ H2O===____ FeO(OH)
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:将铁器浸没在盛有0.5 mol·L-1 Na2SO3、0.5 mol·L-1 NaOH溶液的容器中,缓慢加热至60~90 ℃。一段时间后,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是_________________________________________________ 。
②脱氯反应:FeOCl+OH-===FeO(OH)+Cl-。根据复分解反应发生的条件,比较FeOCl与FeO(OH)溶解度的大小:S(FeOCl)_____ S[FeO(OH)]。(填>或<或=)
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是(将反应补充完全)。
______ SO32-+______ FeO(OH)===______ SO42-+______ Fe3O4+______ H2O
(1)检测锈蚀产物
主要成分的化学式 | |||
| Fe3O4 | Fe2O3·H2O | FeO(OH) | FeOCl |
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
①Fe转化为Fe2+。
②Fe2+在自然环境中形成FeO(OH),该物质中铁元素的化合价为
③2 mol FeO(OH)和1 mol Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
④Fe3O4保护层被氧化为FeO(OH),如此往复腐蚀:(将反应补充完全)。
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:将铁器浸没在盛有0.5 mol·L-1 Na2SO3、0.5 mol·L-1 NaOH溶液的容器中,缓慢加热至60~90 ℃。一段时间后,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是
②脱氯反应:FeOCl+OH-===FeO(OH)+Cl-。根据复分解反应发生的条件,比较FeOCl与FeO(OH)溶解度的大小:S(FeOCl)
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是(将反应补充完全)。
您最近一年使用:0次



