(1)写出Al2(SO4)3的电离方程式____________________________
(2)除去括号中的杂质,写出所加试剂的化学式与反应的离子方程式
①Cl-(SO42-),所加试剂________________ ,离子方程式_________________________
②Fe2+(Cu2+),所加试剂__________________ ,离子方程式________________________
(3)写出与Cu2++2OH-==Cu(OH)2↓离子方程式相对应的化学方程式__________________
(4)写出下列反应的离子方程式:
①用稀硫酸清洗铁锈(Fe2O3)________________________________________
②向足量澄清石灰水中通入二氧化碳________________________________________
(2)除去括号中的杂质,写出所加试剂的化学式与反应的离子方程式
①Cl-(SO42-),所加试剂
②Fe2+(Cu2+),所加试剂
(3)写出与Cu2++2OH-==Cu(OH)2↓离子方程式相对应的化学方程式
(4)写出下列反应的离子方程式:
①用稀硫酸清洗铁锈(Fe2O3)
②向足量澄清石灰水中通入二氧化碳
11-12高一上·江西赣州·阶段练习 查看更多[1]
(已下线)2011-2012学年江西省赣县中学南北校区高一9月份联考化学试卷
更新时间:2011-10-20 10:53:32
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】回答下列问题:
(1)写出下列物质在水溶液中的电离方程式:
①HNO3:___ 。
②NaOH:___ 。
③Na2CO3:___ 。
(2)按酸、碱、盐分类,其中,属于酸的是___ (填序号,下同),属于盐的是___ ,属于碱的是___ 。
(1)写出下列物质在水溶液中的电离方程式:
①HNO3:
②NaOH:
③Na2CO3:
(2)按酸、碱、盐分类,其中,属于酸的是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】从电离角度认识酸、碱的本质的电离方程式。
(1)

(2)

(3)

(4)

 、
、 的电离方程式。
的电离方程式。①
②
③
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】回答下列问题
(1)取少量 粉末
粉末 红棕色
红棕色 加入适量盐酸,发生反应的离子反应方程
加入适量盐酸,发生反应的离子反应方程___________ ,反应后得到的溶液呈___________ 色。用此溶液分别做如下实验:
(2)在小烧杯中加入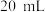 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈___________ 色,停止加热,即制得 胶体。
胶体。
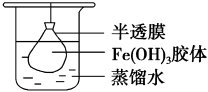
(3)将制得的胶体放入半透膜制成的袋内,如图所示,放置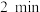 后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察
后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察___________  填“有”或“无”
填“有”或“无” 丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为___________ ;丁达尔效应可以用来区别___________ 。
(1)取少量
 粉末
粉末 红棕色
红棕色 加入适量盐酸,发生反应的离子反应方程
加入适量盐酸,发生反应的离子反应方程(2)在小烧杯中加入
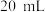 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。
胶体。(3)将制得的胶体放入半透膜制成的袋内,如图所示,放置
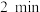 后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察
后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察 填“有”或“无”
填“有”或“无” 丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】写出下列反应的化学方程式和离子方程式
(1)Ca(OH)2溶液和HNO3溶液反应
____________________ ;___________________
(2)用稀硫酸清洗铁锈(Fe2O3)
____________________ ;__________________
(1)Ca(OH)2溶液和HNO3溶液反应
(2)用稀硫酸清洗铁锈(Fe2O3)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】按要求填空:
(1)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式:_______ 。
(2)金属钠在氧气中充分燃烧,将所得产物投入水中,产物和迅速发生反应,写出该反应的化学方程式:_______ 。向所得溶液中加入FeSO4溶液,看到的现象是:_______ ,此过程中发生的氧化还原反应的化学方程式:_______ 。
(3)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式_______ 。
(1)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式:
(2)金属钠在氧气中充分燃烧,将所得产物投入水中,产物和迅速发生反应,写出该反应的化学方程式:
(3)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式
您最近一年使用:0次
【推荐1】为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号 填入对应的空格。
供选择的化学试剂或实验方法有:A.加热B.溶解、过滤、蒸发、结晶C.取样,滴加KSCN溶液,观察现象D.将气体通入盛有饱和食盐水的洗气瓶
供选择的化学试剂或实验方法有:A.加热B.溶解、过滤、蒸发、结晶C.取样,滴加KSCN溶液,观察现象D.将气体通入盛有饱和食盐水的洗气瓶
| 序号 | 实验目的 | 试剂或方法 |
(1) | 除去Cl2中混有少量的HCl | |
(2) | 检验Fe2+溶液中是否含有少量Fe3+ | |
(3) | 除去Na2CO3固体中混有的NaHCO3 | |
(4) | 分离Na2SO4和BaSO4固体混合物 |
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:
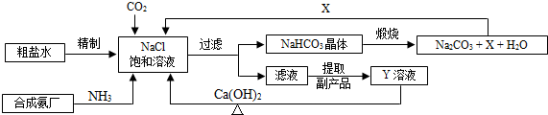
(1)粗盐水中主要含有Ca2+、Mg2+、SO42﹣等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为______ 、盐酸(只写一种)。加盐酸的作用是(用化学方程式表示)____________ 、____________ 。
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由:①CO2+NH3+H2O=NH4HCO3和②NaCl+NH4HCO3=NaHCO3↓+NH4Cl两个反应加合而成,则该反应类型为______________ 。
(3)X的化学式为__________________ 。
(4)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为____________ ,Y的化学式为____________ ,写出Y的一种用途_______________ 。

(1)粗盐水中主要含有Ca2+、Mg2+、SO42﹣等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由:①CO2+NH3+H2O=NH4HCO3和②NaCl+NH4HCO3=NaHCO3↓+NH4Cl两个反应加合而成,则该反应类型为
(3)X的化学式为
(4)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐3】选取下列实验方法分离物质,将分离方法的字母填在横线上:
A.萃取、分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法 F.加热分解法 G.升华法
(1)___________ 分离饱和食盐水与泥沙的混合物。
(2)___________ 分离水和汽油的混合物。
(3)___________ 分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
(4)___________ 除去氧化钙中少量碳酸钙。
(5)___________ 从含硝酸钾和氯化钠的混合液中分离出硝酸钾。
A.萃取、分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法 F.加热分解法 G.升华法
(1)
(2)
(3)
(4)
(5)
您最近一年使用:0次



