下列热化学方程式中,正确的是
| A.甲烷的燃烧热为 890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ/mol |
B.500℃、30MPa 下,将 0.5mol N2和 1.5molH2置于密闭容器中充分反应生成 NH3(g),放热 19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 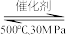 2NH3(g) △H = -38.6 kJ/mol 2NH3(g) △H = -38.6 kJ/mol |
| C.稀盐酸和 稀氢氧化钠溶液混合, 其热化学方程式为:H+(aq)+OH-(aq)=H2O(1) △H = -57.3 kJ/mol |
| D.1molH2完全燃烧放热 142.9kJ,则氢气燃烧的热化学方程式为: 2H2(g)+O2(g)=2H2O(1)△H =+285.8 kJ/mol |
16-17高二上·重庆·期末 查看更多[8]
更新时间:2019-02-19 10:22:13
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列相关方程式不正确的是
A.钢铁制品在潮湿空气中的电化学腐蚀: |
B.加热 溶液除去油污: 溶液除去油污: |
C.用惰性电极电解 溶液: 溶液: |
D.已知: 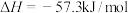 则: 则: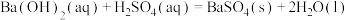 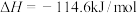 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】有关热化学方程式书写与对应表述均正确的是
| A.稀硫酸与0.1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol1 |
| B.已知2C(s)+O2(g)=2CO(g) △H=—221 kJ·mol-1, 则可知C的燃烧热为110.5 kJ·mol1 |
| C.密闭容器中,0.3mol硫粉与0.2mol铁粉混合加热生成硫化亚铁0.2mol时,放出19.12 kJ热量。则Fe(s)+S(s)=FeS(s) △H= - 95.6 kJ·mol1 |
D.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)  2NH3(g) △H= —38.6kJ·mol1 2NH3(g) △H= —38.6kJ·mol1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列关于反应热和热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
| B.CO(g)的摩尔燃烧焓是-283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+566.0 kJ·mol-1 |
C.氢气的摩尔燃烧焓为-285.5 kJ·mol-1,则电解水的热化学方程式为2H2O(l)  2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1 2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的摩尔燃烧焓 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验方案能够达到实验目的的是
| A.中和热实验中温度的测定:把稀盐酸分多次加入到稀NaOH溶液中,记录混合溶液的最高温度 |
| B.比较Mg和Al的金属活动性:将Mg、Al分别加入浓NaOH溶液中,观察并比较实验现象 |
C.除去 溶液中少量 溶液中少量 :向含有少量 :向含有少量 的 的 溶液中加入适量铁粉,充分反应后过滤 溶液中加入适量铁粉,充分反应后过滤 |
D.探究 溶液是否变质:向少量 溶液是否变质:向少量 溶液中加入足量稀HCl和 溶液中加入足量稀HCl和 溶液,观察现象 溶液,观察现象 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法错误的是
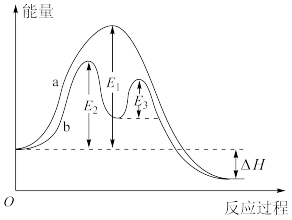

A.在25℃和101kPa时,1moL  (s)完全燃烧生成 (s)完全燃烧生成 (s)和 (s)和 (g)时放出853kJ的热量,则 (g)时放出853kJ的热量,则 燃烧热的热化学方程式为: 燃烧热的热化学方程式为: 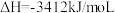 |
B.已知冰的熔化热为6.0 ,冰中氢键键能为20 ,冰中氢键键能为20 ,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 ,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 |
| C.中和反应反应热的测定,需要测量三次温度,第三次测量反应后体系的最高温度 |
| D.某反应过程能量变化如图,b为在有催化剂作用下的反应过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列热化学方程式中△H1~△H4 代表燃烧热的是
| A.CH4(g)+ 3/2 O2(g)= 2H2O(l)+CO(g) △H1 |
| B.H2(g)+ 1/2O2(g)= H2O(g) △H2 |
| C.C2H5OH(l)+3O2(g)= 2CO2(g)+3H2O(l) △H3 |
| D.2CO(g)+O2(g)= 2CO2(g) △H4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知在25℃,101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的燃烧热的热化学方程式正确的是
A.C8H18(l)+ O2(g)=8CO2(g)+9H2O(g) △H=-48.40kJ/mol O2(g)=8CO2(g)+9H2O(g) △H=-48.40kJ/mol |
B.C8H18(l)+ O2(g)=8CO2(g)+9H2O(l) △H=-5518kJ/mol O2(g)=8CO2(g)+9H2O(l) △H=-5518kJ/mol |
C.C8H18(l)+ O2(g)=8CO2(g)+9H2O(l) △H=+5518kJ/mol O2(g)=8CO2(g)+9H2O(l) △H=+5518kJ/mol |
| D.2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l) △H=-11036kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】有关热化学方程式书写与对应表述均正确的是
| A.稀硫酸与0.1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol1 |
| B.已知2C(s)+O2(g)=2CO(g) △H=—221 kJ·mol-1, 则可知C的燃烧热为110.5 kJ·mol1 |
| C.密闭容器中,0.3mol硫粉与0.2mol铁粉混合加热生成硫化亚铁0.2mol时,放出19.12 kJ热量。则Fe(s)+S(s)=FeS(s) △H= - 95.6 kJ·mol1 |
D.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)  2NH3(g) △H= —38.6kJ·mol1 2NH3(g) △H= —38.6kJ·mol1 |
您最近一年使用:0次



