下列说法错误的是
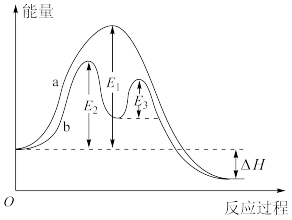

A.在25℃和101kPa时,1moL  (s)完全燃烧生成 (s)完全燃烧生成 (s)和 (s)和 (g)时放出853kJ的热量,则 (g)时放出853kJ的热量,则 燃烧热的热化学方程式为: 燃烧热的热化学方程式为:  |
B.已知冰的熔化热为6.0 ,冰中氢键键能为20 ,冰中氢键键能为20 ,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 ,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 |
| C.中和反应反应热的测定,需要测量三次温度,第三次测量反应后体系的最高温度 |
| D.某反应过程能量变化如图,b为在有催化剂作用下的反应过程 |
更新时间:2022/03/04 16:09:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列实验能达到目的的是
| A.测定中和反应的反应热:用酸碱中和滴定法 |
| B.判断醋酸为弱电解质:测定并比较醋酸和盐酸的pH |
| C.用98%浓硫酸配制10%的稀硫酸:仪器为烧杯、玻璃棒 |
| D.测定镀锌铁皮的镀层厚度:将镀锌铁皮放入稀硫酸中,待产生氢气的速率突然减小,可以判断锌镀层已反应完全 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
解题方法
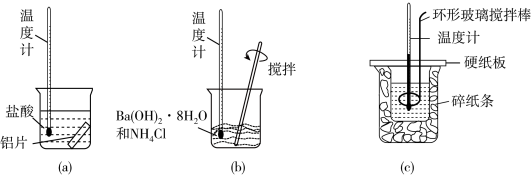
【推荐2】为探究稀盐酸和氢氧化钠溶液反应过程中溶液的 及温度随时间变化关系,小龙同学按图甲连接好实验装置,往盛有一种溶液的烧杯中滴入另一种初温相同的溶液,同时用玻璃棒搅拌。图乙是数据采集器和计算机实时显示数据和曲线,下列说法错误的是
及温度随时间变化关系,小龙同学按图甲连接好实验装置,往盛有一种溶液的烧杯中滴入另一种初温相同的溶液,同时用玻璃棒搅拌。图乙是数据采集器和计算机实时显示数据和曲线,下列说法错误的是
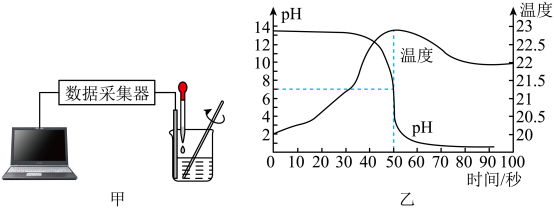
 及温度随时间变化关系,小龙同学按图甲连接好实验装置,往盛有一种溶液的烧杯中滴入另一种初温相同的溶液,同时用玻璃棒搅拌。图乙是数据采集器和计算机实时显示数据和曲线,下列说法错误的是
及温度随时间变化关系,小龙同学按图甲连接好实验装置,往盛有一种溶液的烧杯中滴入另一种初温相同的溶液,同时用玻璃棒搅拌。图乙是数据采集器和计算机实时显示数据和曲线,下列说法错误的是
| A.胶头滴管中的试剂是稀盐酸 | B.60秒时烧杯中的溶质是 和 和 |
| C.盐酸与氢氧化钠反应放出热量 | D.恰好完全反应时,溶液温度升到最高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应:①25℃、101kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol;
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。
下列结论正确的是( )
| A.碳的燃烧热ΔH<-110.5kJ/mol |
| B.反应热有正负之分,标准燃烧热ΔH全部是正值 |
| C.稀硫酸与Ca(OH)2溶液反应的中和热ΔH=-(2×57.3)kJ/mol |
| D.稀醋酸和稀NaOH溶液反应生成1 molH2O,放出57.3kJ的热量 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
【推荐2】下列方程式书写正确的是
| A.已知H2S(g)的燃烧热ΔH=-562kJ/mol,表示其燃烧热的热化学方程式:H2S(g)+2O2(g)= SO3(g)+H2O(l) ΔH=-562kJ/mol |
B.用酸性高锰酸钾和草酸反应研究影响反应速率的因素:2MnO +5C2O +5C2O +16H+= 2Mn2++10CO2↑+8H2O +16H+= 2Mn2++10CO2↑+8H2O |
C.氢氧化铝(一元弱酸)的酸式电离方程式:Al(OH)3+H2O Al(OH) Al(OH) +H+ +H+ |
D.已知常温下Ka1(H2CO3)=4.5×10-7,Ka2(H2CO3)=4.7×10-11,Ka(HClO)=4.0×10-8,向次氯酸钠溶液通入少量CO2:CO2+2ClOˉ+H2O= 2HClO+CO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统。实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量;1 mol CH4 完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写中正确的是( )
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=+890.3 kJ·mol-1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890.3 kJ·mol-1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890.3 kJ |
| D.2H2(g)+O2(g)=2H2O(l)ΔH=-517.6 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法错误的是
| A.当碰撞的分子具有足够的能量和适当的取向时,才能发生化学反应 |
| B.能发生有效碰撞的分子一定是活化分子,活化分子必须具有足够高的能量 |
| C.活化分子间的碰撞一定是有效碰撞,每次碰撞都能发生化学反应 |
| D.活化能指活化分子多出反应物分子平均能量的那部分能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2022年诺贝尔化学奖授予了对点击化学和生物正交化学作出贡献的三位科学家。点击化学的代表反应为“叠氮化物炔烃”反应,其反应原理如图所示(R1和R2代表烷基)。下列说法正确的是
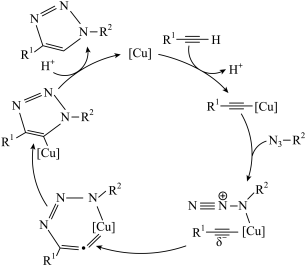
| A.整个反应中碳原子的杂化方式共有2种 |
B. 在[Cu]作用下,C-H键断裂并放出能量 在[Cu]作用下,C-H键断裂并放出能量 |
| C.该反应原理的总反应的原子利用率为100% |
| D.反应中[Cu]可降低反应的活化能,提高反应速率,降低焓变,提高平衡转化率 |
您最近一年使用:0次

 合成
合成 的反应,其中某段反应的相对能量与历程的关系如图所示,图中的
的反应,其中某段反应的相对能量与历程的关系如图所示,图中的 为过渡态,吸附在钯催化剂表面上的物种用*标注。
为过渡态,吸附在钯催化剂表面上的物种用*标注。




