某温度下,在2L容器中3种物质间进行反应,X,Y,Z的物质的量随时间的变化曲线如图,反应在t1 min时到达平衡,如图所示:
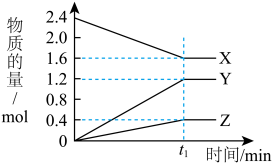
(1)该反应的化学方程式是_________ 。
(2)①若上述反应中X,Y,Z分别为NH3、H2、N2, 且已知1mol 氨气分解成氮气和氢气要吸收46kJ的热量,则至t1 min时,该反应吸收的热量为_______ ;在此t1 min时间内,用H2表示反应的平均速率v(H2)为___________ 。

(1)该反应的化学方程式是
(2)①若上述反应中X,Y,Z分别为NH3、H2、N2, 且已知1mol 氨气分解成氮气和氢气要吸收46kJ的热量,则至t1 min时,该反应吸收的热量为
更新时间:2019-02-26 09:52:56
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】请回答下列问题:
(1)丙烷燃烧可以通过以下两种途径:
途径Ⅰ:
途径Ⅱ:

 (a、b、c、d均为正值)
(a、b、c、d均为正值)
判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量___________ (填“大于”“等于”或“小于”)途径Ⅱ放出的热量。 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量___________ (填“大于”“等于”或“小于”)生成物具有的总能量,b与a、c、d的数学关系式是___________ 。
(2)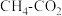 催化重整反应为
催化重整反应为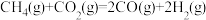 。
。
已知:


该催化重整反应的
___________ kJ/mol。
(3)已知:298K时,相关物质的相对能量如图所示。

请根据相关物质的相对能量计算反应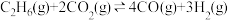 的焓变
的焓变
___________ 。
(4)现有下列3个热化学方程式:



写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:___________ 。
(1)丙烷燃烧可以通过以下两种途径:
途径Ⅰ:

途径Ⅱ:


 (a、b、c、d均为正值)
(a、b、c、d均为正值)判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量
 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量(2)
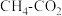 催化重整反应为
催化重整反应为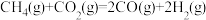 。
。已知:



该催化重整反应的

(3)已知:298K时,相关物质的相对能量如图所示。

请根据相关物质的相对能量计算反应
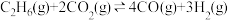 的焓变
的焓变
(4)现有下列3个热化学方程式:



写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)①工业合成氨反应:N2+3H2 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量___ (填“大于”、“小于”或“等于”)920kJ。
②已知断开1molN N键吸收的能量为945.6kJ,形成1molN﹣H键放出的能量为391kJ,根据化学方程式N2+3H2
N键吸收的能量为945.6kJ,形成1molN﹣H键放出的能量为391kJ,根据化学方程式N2+3H2 2NH3,生成标准状况下44.8LNH3时放出的能量为92.4kJ,则断开1molH﹣H键吸收的能量是
2NH3,生成标准状况下44.8LNH3时放出的能量为92.4kJ,则断开1molH﹣H键吸收的能量是___ 。
(2)某实验小组同学进行如图1所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度___ (填“升高”或“降低”)。反应过程___ (填“①”或“②”)的能量变化可用图2表示。

(3)已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图2所示,该反应是___ (填“吸热”或“放热”)反应。
(4)用CH3OH和O2组合形成的质子交换膜燃料电池的结构如图3所示:

①则d电极是___ (填“正极”或“负极”),c电极的电极反应式为___ 。
②若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为___ L。
(1)①工业合成氨反应:N2+3H2
 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量②已知断开1molN
 N键吸收的能量为945.6kJ,形成1molN﹣H键放出的能量为391kJ,根据化学方程式N2+3H2
N键吸收的能量为945.6kJ,形成1molN﹣H键放出的能量为391kJ,根据化学方程式N2+3H2 2NH3,生成标准状况下44.8LNH3时放出的能量为92.4kJ,则断开1molH﹣H键吸收的能量是
2NH3,生成标准状况下44.8LNH3时放出的能量为92.4kJ,则断开1molH﹣H键吸收的能量是(2)某实验小组同学进行如图1所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度

(3)已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图2所示,该反应是
(4)用CH3OH和O2组合形成的质子交换膜燃料电池的结构如图3所示:

①则d电极是
②若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:___ 。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式__ 。
(3)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–1
2NO(g)+O2(g) 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式___ 。
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:___ 。
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式
(3)已知:2SO2(g)+O2(g)
 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–12NO(g)+O2(g)
 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1请写出NO2与SO2反应生成SO3和NO的热化学方程式
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】化学反应速率与生产、生活密切相关。
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①反应速率最大的时间段是______ (填“0~1”“1~2”“2~3”“3~4”“4~5”)min,原因是:_______ 。
②反应速率最小的时间段是___________ ,原因是:___________ 。
③2~3min内该反应的反应速率υ(HCl)=_________ mol∙L−1∙min−1(设溶液体积不变)。
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列___________ (填字母)以减慢反应速率,同时不影响生成氢气的量。
A.蒸馏水 B.NaOH溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl溶液
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况) | 50 | 120 | 232 | 290 | 310 |
①反应速率最大的时间段是
②反应速率最小的时间段是
③2~3min内该反应的反应速率υ(HCl)=
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列
A.蒸馏水 B.NaOH溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】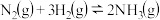 反应过程的能量变化如图所示,请回答下列问题:
反应过程的能量变化如图所示,请回答下列问题:
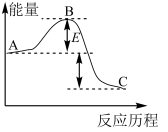
(1)该反应是______________ (填“放热”或“吸热”)反应。
(2)用 作该反应的催化剂,A、C两点的能量差是否变化?
作该反应的催化剂,A、C两点的能量差是否变化?_____________ (填“变化”或“不变”),理由是____________________ 。
(3)在体积为2L的恒容密闭容器中通入2mol 和3mol
和3mol 发生上述反应,10min内
发生上述反应,10min内 的物质的量变化如下表:
的物质的量变化如下表:
①升高温度,反应速率______________ (填“增大”或“减小”)。
②上述反应在7min时_______________ (填“达到”或“未达到”)平衡状态。
③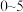 min内,用
min内,用 表示该反应的反应速率为
表示该反应的反应速率为_______________ mol·L-1·min-1。
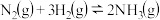 反应过程的能量变化如图所示,请回答下列问题:
反应过程的能量变化如图所示,请回答下列问题:
(1)该反应是
(2)用
 作该反应的催化剂,A、C两点的能量差是否变化?
作该反应的催化剂,A、C两点的能量差是否变化?(3)在体积为2L的恒容密闭容器中通入2mol
 和3mol
和3mol 发生上述反应,10min内
发生上述反应,10min内 的物质的量变化如下表:
的物质的量变化如下表:| 反应时间(min) | 0 | 3 | 5 | 7 | 10 |
 的物质的量(mol) 的物质的量(mol) | 0 | 0.2 | 0.3 | 0.38 | 0.38 |
②上述反应在7min时
③
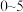 min内,用
min内,用 表示该反应的反应速率为
表示该反应的反应速率为
您最近一年使用:0次

 3C。经2 min后,A的浓度从开始时的1.0mol·L-1 降到0.8 mol·L-1。已知反应开始时B的浓度是1.2mol·L-1。则:2min末B的浓度
3C。经2 min后,A的浓度从开始时的1.0mol·L-1 降到0.8 mol·L-1。已知反应开始时B的浓度是1.2mol·L-1。则:2min末B的浓度

