某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)甲池为__________ (填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为___________________________ 。
(2)丙池中F电极为_________ (填“正极”、“负极”、“阴极”或“阳极”),F电极的电极反应式为_________________________________ 。该池总反应的化学方程式为___________________________ 。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_____ mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是___ (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3

(1)甲池为
(2)丙池中F电极为
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
更新时间:2019-03-12 16:32:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】降低能耗是氯碱工业发展的重要方向。
(1)我国利用氯碱厂生产的 作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。

① 极为
极为_______ (填“正”或“负”)极。
②乙装置中电解饱和 溶液的化学方程式为
溶液的化学方程式为_______ 。
③下列说法正确的是_______ 。
A.甲装置可以实现化学能向电能转化
B.甲装置中 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动
C.乙装置中 极一侧流出的是淡盐水
极一侧流出的是淡盐水
④实际生产中,阳离子交换膜的损伤会造成 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为_______ 。
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为_______ 。
(1)我国利用氯碱厂生产的
 作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
①
 极为
极为②乙装置中电解饱和
 溶液的化学方程式为
溶液的化学方程式为③下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中
 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动C.乙装置中
 极一侧流出的是淡盐水
极一侧流出的是淡盐水④实际生产中,阳离子交换膜的损伤会造成
 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入
 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】甲烷燃料电池采用铂作为电极材料,两个电极上分别通入 和
和 ,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。
,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。

(1)甲烷燃料电池工作时,其电极反应分别为:正极___________ ;负极___________ 。
(2)闭合开关K后,a、b电极上均有气体产生,其中b电极上得到的是___________ ,电解NaCl溶液的总反应式为___________ 。
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为___________ L(标准状况)。
 和
和 ,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。
,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。
(1)甲烷燃料电池工作时,其电极反应分别为:正极
(2)闭合开关K后,a、b电极上均有气体产生,其中b电极上得到的是
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示装置中:b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答

(1)a连接电源的__________ 极。b极的电极反应式为______________________________ 。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:_______________ ,电解进行一段时间后,罩在C极上的试管中也收集到了气体。此时C极上的电极反应式为________________________________
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了__________ mol气体,若在b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为___________ 。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200mL。取该溶液逐滴加入到25.0mL0.1mol/L HCl溶液中,当加入25.00mL这种溶液时刚好沉淀完全。试计算电解前A烧杯中MNO3溶液的物质的量浓度为__________ mol/L。

(1)a连接电源的
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200mL。取该溶液逐滴加入到25.0mL0.1mol/L HCl溶液中,当加入25.00mL这种溶液时刚好沉淀完全。试计算电解前A烧杯中MNO3溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】依据甲、乙、丙三个图回答下列问题:
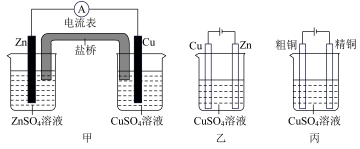
(1)①甲装置中,锌为_____ 极,锌电极上电极反应式为________________
②乙装置中,锌为_____ 极,锌电极上电极反应式为________________
(2)丙装置中,Cu2+浓度________ (填“增大”“减小”或“不变”),原因是_______________________________________________________________________
(3)在25 ℃时,用石墨电极电解2.0 L 0.5 mol·L-1CuSO4溶液。5 min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题:
若电解后溶液的体积不变,则电解后溶液的[H+]为___________ 。
若将溶液恢复到与电解前一样,则需加入_____ mol的______ 。

(1)①甲装置中,锌为
②乙装置中,锌为
(2)丙装置中,Cu2+浓度
(3)在25 ℃时,用石墨电极电解2.0 L 0.5 mol·L-1CuSO4溶液。5 min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题:
若电解后溶液的体积不变,则电解后溶液的[H+]为
若将溶液恢复到与电解前一样,则需加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用电化学装置可消除氮氧化物(如 NO、NO 、NO
、NO 尿素等)污染,变废为宝。
尿素等)污染,变废为宝。
(1)下图为电解 NO制备NH4NO3 的装置。该装置中阴极的电极反应式为___________ ;“反应室”中发生反应的离子方程式为___________ 。

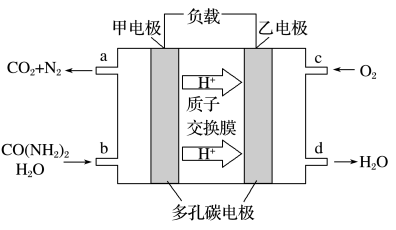
(2)化学家正在研究尿素[CO(NH2)2]动力燃料电池直接去除城市废水中的尿素,既能产生净化的水, 又能发电,尿素燃料电池结构如图所示:
甲电极的电极反应式为___________ ;乙电极的电极反应式为___________ 。理论上每净化 1mol尿素, 消耗O2的体积约为___________ L(标准状况)。
(3)工业上用电解法治理亚硝酸盐 NO
NO 具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:
具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:___________ 。 随后, 铁电极附近有无色气体产生,可能原因是___________ 。

(4)某乙烯熔融碳酸盐燃料电池工作原理如图所示,若要维持电池持续稳定工作,则从理论上讲,进入石墨Ⅱ电极上的CO2与石墨I电极上生成的CO2的物质的量之比是___________ 。

 、NO
、NO 尿素等)污染,变废为宝。
尿素等)污染,变废为宝。(1)下图为电解 NO制备NH4NO3 的装置。该装置中阴极的电极反应式为

(2)化学家正在研究尿素[CO(NH2)2]动力燃料电池直接去除城市废水中的尿素,既能产生净化的水, 又能发电,尿素燃料电池结构如图所示:
甲电极的电极反应式为
(3)工业上用电解法治理亚硝酸盐
 NO
NO 具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:
具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:
(4)某乙烯熔融碳酸盐燃料电池工作原理如图所示,若要维持电池持续稳定工作,则从理论上讲,进入石墨Ⅱ电极上的CO2与石墨I电极上生成的CO2的物质的量之比是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知甲池的总反应式:2CH3OH+3O2+4KOH===2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称。
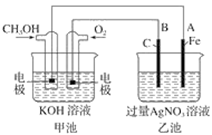
甲池是________ 装置;乙池是________ 装置。
(2)写出电极反应式:通入O2的电极的电极反应式是____________________________________________________ 。
(3)乙池中反应的化学方程式为___________________________ 。
(4)当乙池中A(Fe)极的质量增加5.40 g时,甲池中理论上消耗O2________ mL(标准状况下)。
(1)请回答图中甲、乙两池的名称。

甲池是
(2)写出电极反应式:通入O2的电极的电极反应式是
(3)乙池中反应的化学方程式为
(4)当乙池中A(Fe)极的质量增加5.40 g时,甲池中理论上消耗O2
您最近一年使用:0次



