Ⅰ.A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)B为__________ (填写元素符号),D的最高价氧化物对应的水化物是_________ (填写化学式),离子半径大小B_________ C(填“>”“<”或“=”);
(2)写出A、B的化合物与E反应的化学方程式:______________________ ;A、B两元素形成的化合物属于_________ (填“离子”或“共价”)化合物。
(3)A的单质与D的最高价氧化物对应的水化物反应的化学方程式为_______________ 。
Ⅱ.常温下由三种短周期元素形成的气体单质X、Y、Z,有下列转化关系(反应条件已略去):

已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子。
(4)化合物甲的电子式是_____________ ;化合物丙中存在的化学键为___________ 、_________
(1)B为
(2)写出A、B的化合物与E反应的化学方程式:
(3)A的单质与D的最高价氧化物对应的水化物反应的化学方程式为
Ⅱ.常温下由三种短周期元素形成的气体单质X、Y、Z,有下列转化关系(反应条件已略去):

已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子。
(4)化合物甲的电子式是
更新时间:2019-04-08 09:13:31
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】三氯甲烷为无色油状液体,不溶于水,密度比水大,是良好的有机溶剂。但对光敏感,遇光照会与空气中的氧作用,产生剧毒的光气:2CHCl3+O2 = 2HCl+2COCl2。
(1)氯的原子结构示意图为_______ , 氯所在周期的元素中,最高价氧化物所对应水化物碱性最强的是_______ (填化学式)。O、S等都是氧族元素,该族元素最外层电子的轨道表示式为_______ ;
(2)中子数为8的碳原子的符号可表示为_______ ;三氯甲烷的空间构型是_______ ;
(3)光气的结构式为 ,下列关于光气分子的说法正确的是_______;
,下列关于光气分子的说法正确的是_______;
(4)标准状况下,该反应每消耗11.2L空气(氧气的体积分数为21%),则发生转移的电子有_______ mol。
(5)若保管不当,三氯甲烷会被空气氧化而变质。实验室欲检验某试剂瓶内存放的三氯甲烷是否因氧化而变质,可用_______ (填试剂名称)进行检验。选用该试剂的理由是_______ 。
(1)氯的原子结构示意图为
(2)中子数为8的碳原子的符号可表示为
(3)光气的结构式为
 ,下列关于光气分子的说法正确的是_______;
,下列关于光气分子的说法正确的是_______;A.比例模型为 |
B.电子式是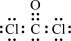 |
| C.具有极性键和非极性键 |
| D.所有原子都达到了最外层8电子稳定结构 |
(5)若保管不当,三氯甲烷会被空气氧化而变质。实验室欲检验某试剂瓶内存放的三氯甲烷是否因氧化而变质,可用
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】原子序数依次增大的五种短周期元素A、B、C、D、E,已知A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y;A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:
(1)B在周期表中的位置是_______ 。
(2)D和E形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式_______ 。
(3)B元素的单质与浓硫酸反应的化学方程式_______ 。
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式_______ 。
(1)B在周期表中的位置是
(2)D和E形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式
(3)B元素的单质与浓硫酸反应的化学方程式
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有部分短周期元素的性质或原子结构如表:
用化学用语回答下列问题:
(1)A元素在周期表中的位置__________________ ;
(2)C单质分子的结构式______________________ ;
(3)元素D与元素A相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是 ______ (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去)。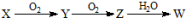
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为_______________ ,试写出Y与H2O2溶液反应的化学方程式: __________________________________________ ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为_________ 。
| 元素编号 | 元素性质或原子结构 |
| A | 有3个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(1)A元素在周期表中的位置
(2)C单质分子的结构式
(3)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去)。
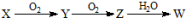
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素A、B、C、D、E的原子序数依次增大。常温下,A、B组成的化合物是常见液体,C的原子半径是短周期主族元素中最大的,D最外层电子数等于电子层数的2倍。回答下列问题:
(1)B在元素周期表中的位置为_______ ;A、B组成的原子个数比为1:1的化合物的电子式为_______ 。
(2)B、C的简单离子中,半径较大的是_______ (填离子符号);A、B、C三种元素组成的化合物中含有的化学键类型是_______ 。
(3)C、E的最高价氧化物对应的水化物间反应的化学方程式为_______ 。
(4)下列叙述能说明E的非金属性强于D的是_______ (填序号)。
a.D的简单氢化物的稳定性弱于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
(1)B在元素周期表中的位置为
(2)B、C的简单离子中,半径较大的是
(3)C、E的最高价氧化物对应的水化物间反应的化学方程式为
(4)下列叙述能说明E的非金属性强于D的是
a.D的简单氢化物的稳定性弱于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期元素的单质X、Y、Z在通常状况下均为气态,并有如图转化关系(反应条件略去):

已知:a.常见双原子单质分子中,X分子含共价键最多。b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是_______ 。
(2)实验室可用如图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。

①在图中方框内绘出用烧瓶收集甲的仪器装置简图_______ 。
②试管中的试剂是_______ (填写化学式)。
③烧杯中溶液由无色变为红色,其原因是_______ (用电离方程式表示)
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是_______ 。
(4)单质Z与过量的共价化合物甲反应有白烟生成,写出反应的化学方程式:_______ 。
(5)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是_______ 。

已知:a.常见双原子单质分子中,X分子含共价键最多。b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是
(2)实验室可用如图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。

①在图中方框内绘出用烧瓶收集甲的仪器装置简图
②试管中的试剂是
③烧杯中溶液由无色变为红色,其原因是
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是
(4)单质Z与过量的共价化合物甲反应有白烟生成,写出反应的化学方程式:
(5)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E、F六种元素,均位于周期表的前四周期,它们的核电荷数依次增加,A原子的L层p轨道中有2个电子,B元素在同周期元素中电负性最大,C与A原子的价电子数相同,D的最高价含氧酸酸性最强,E原子核外不成对电子数最多,F元素能形成的双原子分子,其单质在常温下呈液态。
(1)A的最高价含氧酸酸根离子的价层电子对数为_____ ,其 模型是
模型是_____ 。
(2)B、D、F简单氢化物沸点由高到低的顺序为_____ (填化学式),原因是_____ 。
(3)与E同族的第n周期元素核外电子排布不遵循洪特规则特例,则它的外围电子排布式为_____ 。
(4)与A相比,从电子云重叠方式的角度解释为什么C的原子间难以形成双键和叁键_____ 。
(1)A的最高价含氧酸酸根离子的价层电子对数为
 模型是
模型是(2)B、D、F简单氢化物沸点由高到低的顺序为
(3)与E同族的第n周期元素核外电子排布不遵循洪特规则特例,则它的外围电子排布式为
(4)与A相比,从电子云重叠方式的角度解释为什么C的原子间难以形成双键和叁键
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、C、D、E、G、X、Y、Z是几种常见的短周期主族元素,其原子半径随原子序数变化如下图所示。已知C的最高正价与最低负价的绝对值相等;E的一种核素的质量数为18,中子数为10;G原子和Ne原子的核外电子数相差1;X的简单离子半径在同周期中最小;Y的单质是一种常见的半导体材料;Z的最外层有7个电子。回答下列问题:

(1)C在元素周期表中的位置_____ ,由A、E两种元素组成的18电子微粒的结构式为_________ 。
(2)E、G、Z三种元素的简单离子半径最小的是_____ (填离子符号)。
(3)元素的非金属性:C_____ Y(填“>”或“<”),其实验依据是_____ (用离子方程式表示 )
(4)X的原子结构示意图为_____ 。
(5)Y与Z形成的化合物在一定条件下与足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是_____ 。

(1)C在元素周期表中的位置
(2)E、G、Z三种元素的简单离子半径最小的是
(3)元素的非金属性:C
(4)X的原子结构示意图为
(5)Y与Z形成的化合物在一定条件下与足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素A、B、D、E、F、G均为短周期主族元素,且原子序数依次增大,只有E为金属元素。已知A原子只有一个电子层;E、F的原子序数分别是B、D的2倍,其中D、F同主族,B、E不同主族。回答下列问题:
(1)元素D在周期表中的位置____ 。
(2)F和G形成的化合物,分子中所有原子均为8电子稳定结构,该化合物的电子式为____ 。
(3)由上述元素组成的物质中,按下列要求写出化学方程式
①两种弱酸反应生成两种强酸______ ;
②置换反应,且生成物在常温均为固态____ 。
(4)在D、F、G中选取2种元素组成具有漂白、杀菌作用的化合物___ 。
(1)元素D在周期表中的位置
(2)F和G形成的化合物,分子中所有原子均为8电子稳定结构,该化合物的电子式为
(3)由上述元素组成的物质中,按下列要求写出化学方程式
①两种弱酸反应生成两种强酸
②置换反应,且生成物在常温均为固态
(4)在D、F、G中选取2种元素组成具有漂白、杀菌作用的化合物
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】原子序数由小到大排列的四种短周期元素 X、Y、Z、W,四种元素的原子序数之和为 32,在周期表中 X 是原子半径最小的元素,Y、Z 左右相邻,Z、W 位于同主族。
(1)W 原子的核外电子排布式为__________________ 。
(2)均由 X、Y、Z 三种元素组成的三种常见物质 A.、B、C 分别属于酸、碱、盐,其化学式依次 为________________ 、__________________ 、____________________ ,推测盐中阴离子的空间构型为___________ ,其中心原子杂化方式为_________________________ 。
(3)Z、W 两种元素电负性的大小关系为___________ (填“大于”“等于”或“小于”);Y、Z 两种元素第 一电离能的大小关系为________________ (填“大于”“等于”或“小于”)。
(4)CO 的结构可表示为C≡O,元素Y 的单质Y2 的结构也可表示为Y≡Y。下表是两者的键能数据(单位:kJ⋅mol−1):
①结合数据说明 CO 比 Y2 活泼的原因:_________________________ 。
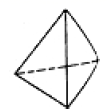
②意大利罗马大学 FulvioCacace 等人获得了极具研究意义的 Y4 分子,其结构如图所示,请结合上表数 据分析,下列说法中,正确的是_____ 。
a. Y4 为一种新型化合物
b. Y4 与 Y2 互为同素异形体
c. Y4 的沸点比 P4(白磷)高
d. 1mol Y4 气体转变为 Y2 将放出 954.6kJ 热量
(1)W 原子的核外电子排布式为
(2)均由 X、Y、Z 三种元素组成的三种常见物质 A.、B、C 分别属于酸、碱、盐,其化学式依次 为
(3)Z、W 两种元素电负性的大小关系为
(4)CO 的结构可表示为C≡O,元素Y 的单质Y2 的结构也可表示为Y≡Y。下表是两者的键能数据(单位:kJ⋅mol−1):
| A−B | A═B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| Y2 | 154.8 | 418.4 | 941.7 |
②意大利罗马大学 FulvioCacace 等人获得了极具研究意义的 Y4 分子,其结构如图所示,请结合上表数 据分析,下列说法中,正确的是

a. Y4 为一种新型化合物
b. Y4 与 Y2 互为同素异形体
c. Y4 的沸点比 P4(白磷)高
d. 1mol Y4 气体转变为 Y2 将放出 954.6kJ 热量
您最近一年使用:0次



