现有部分短周期元素的性质或原子结构如表:
用化学用语回答下列问题:
(1)A元素在周期表中的位置__________________ ;
(2)C单质分子的结构式______________________ ;
(3)元素D与元素A相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是 ______ (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去)。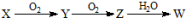
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为_______________ ,试写出Y与H2O2溶液反应的化学方程式: __________________________________________ ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为_________ 。
| 元素编号 | 元素性质或原子结构 |
| A | 有3个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(1)A元素在周期表中的位置
(2)C单质分子的结构式
(3)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去)。
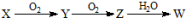
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为
更新时间:2018-06-28 21:18:24
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A为常见的金属单质,根据下图所示的关系:
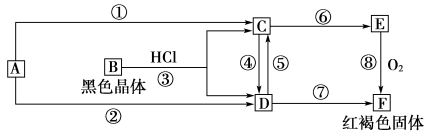
(1)确定A、B、C、D、E、F的化学式,A为________ ,B为________ ,C为________ ,D为________ ,E为________ ,F为________ 。
(2)写出①⑧的化学方程式,④、⑤的离子方程式。
①_________________________________________________ ,
⑧_________________________________________________ ,
④________________________________________________ ,
⑤___________________________________________________ 。

(1)确定A、B、C、D、E、F的化学式,A为
(2)写出①⑧的化学方程式,④、⑤的离子方程式。
①
⑧
④
⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】 、
、 、
、 、
、 、
、 五种物质有如图所示的转化关系(部分反应物产物及反应条件略去),且物质
五种物质有如图所示的转化关系(部分反应物产物及反应条件略去),且物质 是一种淡黄色的固体,
是一种淡黄色的固体, 的相对分子质量为
的相对分子质量为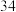 。回答下列问题:
。回答下列问题:

(1)写出下列物质的化学式:
___________ ,
___________ 。
(2)实验室中常用___________ (填试剂名称)来检验 的存在,利用的是
的存在,利用的是 的
的___________ 性。
(3) 的浓溶液在常温下为黏稠的油状液体。
的浓溶液在常温下为黏稠的油状液体。
①将 溶液敞口放置在空气中其质量会增加,溶质的质量分数会
溶液敞口放置在空气中其质量会增加,溶质的质量分数会___________ (填“增大”“减小”或“不变”)。
②E的浓溶液可作干燥剂,下列物质可用 的浓溶液干燥的是
的浓溶液干燥的是___________ (填字母)。
 氨气
氨气  氢气
氢气  二氧化硫
二氧化硫  氧气
氧气  氯化氢
氯化氢
③将C通入B的溶液中,产生的现象为___________ ,写出对应的化学反应方程式___________ 。
 、
、 、
、 、
、 、
、 五种物质有如图所示的转化关系(部分反应物产物及反应条件略去),且物质
五种物质有如图所示的转化关系(部分反应物产物及反应条件略去),且物质 是一种淡黄色的固体,
是一种淡黄色的固体, 的相对分子质量为
的相对分子质量为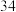 。回答下列问题:
。回答下列问题:
(1)写出下列物质的化学式:


(2)实验室中常用
 的存在,利用的是
的存在,利用的是 的
的(3)
 的浓溶液在常温下为黏稠的油状液体。
的浓溶液在常温下为黏稠的油状液体。①将
 溶液敞口放置在空气中其质量会增加,溶质的质量分数会
溶液敞口放置在空气中其质量会增加,溶质的质量分数会②E的浓溶液可作干燥剂,下列物质可用
 的浓溶液干燥的是
的浓溶液干燥的是 氨气
氨气  氢气
氢气  二氧化硫
二氧化硫  氧气
氧气  氯化氢
氯化氢③将C通入B的溶液中,产生的现象为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E五种短周期元素的原子序数依次增大,A、B同周期,A、C同主族,化合物AB2、DB2均是可使澄清石灰水变浑浊的气体。又已知C、E的单质均可与NaOH溶液反应,且C与NaOH溶液反应可产生氢气。
(1)A元素的名称为_______ ,在元素周期表中的位置是_______ ;
(2)写出C单质的一种用途_______ ;
(3)对B单质或化合物描述正确的是_______ ;
a.常温、常压下单质难溶于水
b.B元素在化合物中的化合价可为﹣1或﹣2价
c.单质分子中含有18个电子
d.氢气与B单质混合在一定条件下可能发生爆炸
(4)写出C、E单质分别与NaOH溶液反应的离子方程式_______ 、_______ 。
(1)A元素的名称为
(2)写出C单质的一种用途
(3)对B单质或化合物描述正确的是
a.常温、常压下单质难溶于水
b.B元素在化合物中的化合价可为﹣1或﹣2价
c.单质分子中含有18个电子
d.氢气与B单质混合在一定条件下可能发生爆炸
(4)写出C、E单质分别与NaOH溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有四种短周期元素,它们的结构、性质等信息如表所述:
(1)X元素在周期表中的位置_____ ;其相对分子质量最小的气态氢化物常用作_____ 。
(2)用电子式表示X最高价氧化物的形成过程_____________________ 。
(3)Y的最高价氧化物对应水化物的电子式________ 。
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式为______________ 。
(5)举出实例说明M的非金属性比X强:_____________ 。
元素 | 结构、性质等信息 |
X | 构成有机物的核心元素,该元素的一种氧化物和气态氢化物都是典型的温室气体 |
Y | 短周期中(除稀有气体外)原子半径最大的元素,该单质与冷水剧烈反应 |
Z | 与Y同周期,其最高价氧化物的水化物呈两性 |
M | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒剂和杀菌剂 |
(2)用电子式表示X最高价氧化物的形成过程
(3)Y的最高价氧化物对应水化物的电子式
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式为
(5)举出实例说明M的非金属性比X强:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E
同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个,C是短周期元素原子半径最大的元素,E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是________________ ;
(2)A单质的结构式____________ ;
(3)乙物质中含有的化学键类型为_____________________ ;
(4)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)________________ 。
(5)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是__________________ 。
同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个,C是短周期元素原子半径最大的元素,E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是
(2)A单质的结构式
(3)乙物质中含有的化学键类型为
(4)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)
(5)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A~H八种短周期主族元素在周期表中的相对位置如下图所示,已知C元素形成的单质有“国防金属”的美誉,E的最高价氧化物对应的水化物能与E的最简单氢化物反应生成离子化合物。

(1)D元素在周期表中的位置为______________ 。
(2)B、E、F的简单离子半径由大到小的顺序为______________ (写离子符号)。
(3)上述元素所形成的气态单质中能用于饮用水消毒的是_________ (写化学式)。
(4)F与G的氢化物中稳定的是________ (写化学式)。
(5)B的单质在F的单质中燃烧所形成化合物的电子式为________ 。
(6)写出实验室制备E的最简单氢化物的化学方程式_____________________________ 。

(1)D元素在周期表中的位置为
(2)B、E、F的简单离子半径由大到小的顺序为
(3)上述元素所形成的气态单质中能用于饮用水消毒的是
(4)F与G的氢化物中稳定的是
(5)B的单质在F的单质中燃烧所形成化合物的电子式为
(6)写出实验室制备E的最简单氢化物的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A~H八种短周期主族元素在周期表中的相对位置如下图所示,已知C元素形成的单质有“国防金属”的美誉,E的最高价氧化物对应的水化物能与E的最简单氢化物反应生成离子化合物。

(1)D元素在周期表中的位置为______________ 。
(2)B、E、F的简单离子半径由大到小的顺序为______________ (写离子符号)。
(3)上述元素所形成的气态单质中能用于饮用水消毒的是_________ (写化学式)。
(4)F与G的氢化物中稳定的是________ (写化学式)。
(5)B的单质在F的单质中燃烧所形成化合物的电子式为________ 。
(6)写出实验室制备E的最简单氢化物的化学方程式_____________________________ 。

(1)D元素在周期表中的位置为
(2)B、E、F的简单离子半径由大到小的顺序为
(3)上述元素所形成的气态单质中能用于饮用水消毒的是
(4)F与G的氢化物中稳定的是
(5)B的单质在F的单质中燃烧所形成化合物的电子式为
(6)写出实验室制备E的最简单氢化物的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大,其相关信息如下表所示,回答下列问题:
(1)R基态原子的价电子排布图为___________________ ,R在周期表中位于________ 区。
(2)X、Y、Z的第一电离能由大到小的顺序为________ (用元素符号表示)。
(3)Q单质形成的晶体的堆积模型为____________ ,配位数是______ 。
(4)光谱证实单质W与强碱溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在________ (填字母)。
a.极性共价键 b.非极性共价键 c.配位键 d.σ键 e.π键
| X的基态原子中电子分布在三个不同的能级中且每个能级中电子总数相同 |
| Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
| Z元素的族序数是周期数的三倍 |
| W原子的第一至第六电离能分别为: I1=578 kJ·mol-1 I2=1 817 kJ·mol-1 I3=2 745 kJ·mol-1 I4=11 575 kJ·mol-1 I5=14 830 kJ·mol-1 I6=18 376 kJ·mol-1 |
| Q为前四周期中电负性最小的元素 |
| R位于周期表中的第11列 |
(1)R基态原子的价电子排布图为
(2)X、Y、Z的第一电离能由大到小的顺序为
(3)Q单质形成的晶体的堆积模型为
(4)光谱证实单质W与强碱溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在
a.极性共价键 b.非极性共价键 c.配位键 d.σ键 e.π键
您最近一年使用:0次
【推荐3】已知元素X、Y、Z、W、Q均为短周期元素,原子序数依次增大。X基态原子的核外电子分布在3个能级,且各能级电子数相等,Z是地壳中含量最多的元素,W是电负性最大的元素,元素Q的核电荷数等于Y、W原子的最外层电子数之和。另有R元素位于元素周期表第4周期第Ⅷ族,基态电子构型中有2个未成对电子。请回答下列问题。
(1)元素Q的元素符号为_______ ,元素R的元素名称为_______ 。
(2)元素X的基态原子中,能量最高的能级中原子轨道形状为_______ 。
(3)基态R3+离子的外围电子排布式为_______ 。
(4)Y、Z、W三种元素第一电离能由大到小顺序为_______ (用元素符号表示)
(5)由H(氢)、X、Y三种元素组成的化合物HXY中,σ键与π键的数目之比为_______ 。
(1)元素Q的元素符号为
(2)元素X的基态原子中,能量最高的能级中原子轨道形状为
(3)基态R3+离子的外围电子排布式为
(4)Y、Z、W三种元素第一电离能由大到小顺序为
(5)由H(氢)、X、Y三种元素组成的化合物HXY中,σ键与π键的数目之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E五种短周期元素,A与D同周期,A的单质既可与盐酸反应,又可与NaOH溶液反应,B的单质在放电条件下能与氧气反应,C元素的离子不含电子,D元素原子的最外层电子数是其次外层电子数的 ,E元素原子的最外层电子数是其次外层电子数的3倍。
,E元素原子的最外层电子数是其次外层电子数的3倍。
(1)A的原子结构示意图为__________________________ 。
(2)0.1 mol/L A的硫酸盐溶液与0.1 mol/L NaOH溶液等体积混合,反应的离子
方程式为__________________________________________________________ 。
(3)以A的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池总反应的化学方程式是______________ 。
(4)化合物甲由元素A、B组成,具有良好电绝缘性。
化合物甲能与水缓慢反应生成含B的化合物乙,乙分子中含有10个电子。写出该
反应的化学方程式:________________________________________ 。
工业用A的单质和化合物乙在高于1700K反应制备甲。已知该反应可以认为是置
换反应,该反应的化学方程式是________________________________________ 。
(5)D和E两种元素相比较,非金属性较强的是(填元素名称)____ ,可以验证该结论的是(填写编号)___________ ;
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
(6)C、D、E间可形成丙、丁两种分子,它们均含有18个电子,则丙与丁反应生成D单质的化学方程式为_______________________ ;
 ,E元素原子的最外层电子数是其次外层电子数的3倍。
,E元素原子的最外层电子数是其次外层电子数的3倍。(1)A的原子结构示意图为
(2)0.1 mol/L A的硫酸盐溶液与0.1 mol/L NaOH溶液等体积混合,反应的离子
方程式为
(3)以A的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池总反应的化学方程式是
(4)化合物甲由元素A、B组成,具有良好电绝缘性。
化合物甲能与水缓慢反应生成含B的化合物乙,乙分子中含有10个电子。写出该
反应的化学方程式:
工业用A的单质和化合物乙在高于1700K反应制备甲。已知该反应可以认为是置
换反应,该反应的化学方程式是
(5)D和E两种元素相比较,非金属性较强的是(填元素名称)
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
(6)C、D、E间可形成丙、丁两种分子,它们均含有18个电子,则丙与丁反应生成D单质的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)C的原子结构示意图为_________ ,D在元素周期表中的位置____________ 。
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为__________ ;A单质在E单质中燃烧生成化合物乙,用电子式表示乙的形成过程___________________ 。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为__________________________ 。
(4)含B元素的化合物常用作净水剂,用文字和化学用语解释净水原因:__________ 。
(5)E元素的非金属性强于D元素,用原子结构解释原因:______________________ ,同周期元素随着原子序数的递增非金属性增强。
(6)工业上将干燥的E单质通入D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为___________________ 。
(1)C的原子结构示意图为
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为
(4)含B元素的化合物常用作净水剂,用文字和化学用语解释净水原因:
(5)E元素的非金属性强于D元素,用原子结构解释原因:
(6)工业上将干燥的E单质通入D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有7种短周期元素的原子序数按A、B、C、D、E、F、G的顺序依次增大;B元素一种原子的含量常用于判定古生物遗体的年代,A和C元素的原子能形成4核10电子的微粒;D和E可形成离子化合物E2D,E2D中所有微粒的电子数相同,且电子总数为30;E、F、G的最高价氧化物对应的水化物之间可以相互反应;G和D同主族。试回答下列问题:
(1)C元素的原子结构示意图___________ 。
(2)A和D形成原子个数比为1:1的物质化学式为___________ 。
(3)B元素在周期表中的位置为___________ ;过量的B元素的最高价氧化物与氢氧化钠溶液反应的离子方程式为___________ 。
(4)D、E、F、G的离子半径由大到小顺序为(用离子符号表示)___________ 。
(5)F的单质与E元素的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(6)写出A、B、D、E四种元素形成的化合物X与少量氢氧化钙溶液反应的离子方程式:___________ 。
(1)C元素的原子结构示意图
(2)A和D形成原子个数比为1:1的物质化学式为
(3)B元素在周期表中的位置为
(4)D、E、F、G的离子半径由大到小顺序为(用离子符号表示)
(5)F的单质与E元素的最高价氧化物对应的水化物反应的离子方程式为
(6)写出A、B、D、E四种元素形成的化合物X与少量氢氧化钙溶液反应的离子方程式:
您最近一年使用:0次



