短周期元素A、B、C、D、E的原子序数依次增大 ,其元素特征信息如下表:
(1)E的简单离子的结构示意图为____________ ;
(2)C元素和A元素能化合形成C3A的化合物,该化合物化学式是__________ ;
(3)C和D简单离子的半径大小为____ >_____ ;(用离子符号表示)
(4)用两根玻璃棒分别蘸取A元素最高价氧化物对应水化物的浓溶液和A元素的氢化物的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式_____________________________ 。
(5)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中可行的是_________ (填序号);
a.比较两种单质的颜色 b. 依据两元素在周期表中的位置
c.比较氢化物的稳定性 d.依据两元素单质在自然界中的存在状态
| 元素编号 | 元素特征信息 |
| A | 最高正价和最低负价的绝对值之差为2 |
| B | 原子核电荷数是内层电子数的4倍 |
| C | 1molC单质能与冷水反应,在标准状况下生成11.2L H2 |
| D | 原子最外层电子数等于其周期序数 |
| E | 负二价阴离子的电子层结构与Ar原子相同 |
(2)C元素和A元素能化合形成C3A的化合物,该化合物化学式是
(3)C和D简单离子的半径大小为
(4)用两根玻璃棒分别蘸取A元素最高价氧化物对应水化物的浓溶液和A元素的氢化物的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式
(5)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中可行的是
a.比较两种单质的颜色 b. 依据两元素在周期表中的位置
c.比较氢化物的稳定性 d.依据两元素单质在自然界中的存在状态
更新时间:2019-04-09 19:40:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表短同期的一部分, A、B、C、D、E五种元素在周期表中的位置如下图所示。C元素的原子最外层电子数为次外层的3倍。
回答下列问题:
(1)B元素在周期表中的位置为__________ 。
(2)D的最高价氧化物对应水化物的化学式为__________ 。
(3)下列事实能说明C元素的非金属性比硫元素的非金属性强的是__________ 。
a.C单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molC单质比1molS得电子多
c.C和S两元素的简单氢化物受热分解,前者的分解温度高
d. C元素的简单氢化物沸点高于S元素的简单氢化物
(4)B与D两元素的单质反应生成化合物M,它的结构类似甲烷,写出M的电子式_____ 。
(5)A与镁形成的1mol化合物N与水反应,生成2molMg(OH)2和1mol气态烃,该烃分子中碳氢质量比为9:1,写出N与水反应的化学方程式______________________________ 。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为__________ 。
| A | E | C | |
| B | D |
(1)B元素在周期表中的位置为
(2)D的最高价氧化物对应水化物的化学式为
(3)下列事实能说明C元素的非金属性比硫元素的非金属性强的是
a.C单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molC单质比1molS得电子多
c.C和S两元素的简单氢化物受热分解,前者的分解温度高
d. C元素的简单氢化物沸点高于S元素的简单氢化物
(4)B与D两元素的单质反应生成化合物M,它的结构类似甲烷,写出M的电子式
(5)A与镁形成的1mol化合物N与水反应,生成2molMg(OH)2和1mol气态烃,该烃分子中碳氢质量比为9:1,写出N与水反应的化学方程式
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试判断:
(1)写出Z离子的结构示意图:_______
(2)由以上元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为_______ ,含有非极性共价键的共价化合物的化学式为_______ 。
(3)由X、Y、Z所形成的的常见离子化合物是_______ (填化学式)
(4)用电子式表示W2Z2的形成过程:_______ 。
(1)写出Z离子的结构示意图:
(2)由以上元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为
(3)由X、Y、Z所形成的的常见离子化合物是
(4)用电子式表示W2Z2的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有A、B、C、D、E、F六种短周期元素,其中A的一种原子不含中子;B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子;C元素的一种气体单质呈蓝色,D与B同周期,该周期中D的简单离子半径最小;E的单质是一种本身有毒可以用来消毒的气体;F元素最高正价与最低负价的代数和为4。
(1)B、C、E三元素组成的化合物之一,是家用消毒剂的主要成分,所含的化学键有__ ,其电子式为__ 。
(2)D、E、F的简单离子半径由大到小的顺序是__ (用离子符号表示)。
(3)B和F两种元素单质可形成化合物M,用电子式表示M的形成过程__ 。
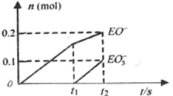
(4)一定量的石灰乳中通入一定量的E单质,两者恰好完全反应,生成物中有三种含E元素的离子。其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。则t2时刻总反应的化学方程为__ 。
(1)B、C、E三元素组成的化合物之一,是家用消毒剂的主要成分,所含的化学键有
(2)D、E、F的简单离子半径由大到小的顺序是
(3)B和F两种元素单质可形成化合物M,用电子式表示M的形成过程
(4)一定量的石灰乳中通入一定量的E单质,两者恰好完全反应,生成物中有三种含E元素的离子。其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。则t2时刻总反应的化学方程为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:

(1)x在元素周期表中的位置位于_______ 。
(2)f单质与e的最高价氧化物对应的水化物反应的化学方程式是_______ 。
(3)g与h的最简单氢化物的稳定性由强到弱的顺序为_______ (用化学式表示)。
(4)z、d、e、f元素中,原子半径由小到大的顺序是_______ (填元素符号);这四种元素分别形成的简单离子中离子半径最小的是_______ (填离子符号)。
(5)e和f两元素相比较,金属性较强是______ (填元素符号),可以证明该结论的实验是______ 。
A.比较这两种元素最高价氧化物对应的水化物的碱性
B.比较这两种元素的气态氢化物的稳定性
C.将相同大小的这两种元素单质分别放入冷水中,观察反应现象
D.比较物质的量相同的这两种元素的单质与酸反应时失电子的数目

(1)x在元素周期表中的位置位于
(2)f单质与e的最高价氧化物对应的水化物反应的化学方程式是
(3)g与h的最简单氢化物的稳定性由强到弱的顺序为
(4)z、d、e、f元素中,原子半径由小到大的顺序是
(5)e和f两元素相比较,金属性较强是
A.比较这两种元素最高价氧化物对应的水化物的碱性
B.比较这两种元素的气态氢化物的稳定性
C.将相同大小的这两种元素单质分别放入冷水中,观察反应现象
D.比较物质的量相同的这两种元素的单质与酸反应时失电子的数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期元素X、Y、Z、W、N 的原子序数依次增大,其中X 的一种同位素原子没有中子,Y 的一种核素可做考古学家测定文物的年代,Z 为地壳中含量最多的非金属元素,W 的焰色反应为黄色,N 原子为所在周期原子半径最小的原子(稀有气体除外)
(1)W 在周期表中的位置_____ ;X、Z 形成的原子个数比 1:1 的分子的结构式 _____ 。
(2)元素 Z 和 W 形成的一种化合物为淡黄色固体,该化合物的电子式为_____ ,该化合物中化学键有 _____ ,该化合物与 Y 的最高价氧化物反应的化学方程式为 __________ 。
(3)Z、W、N 的简单离子半径从大到小的顺序:_____ (用离子符号表示)
(4)甲和乙是由上述元素 X 分别与元素 Y、Z 形成的 10 电子分子,沸点____ >____ (填化学式),原因:_____ 。
(1)W 在周期表中的位置
(2)元素 Z 和 W 形成的一种化合物为淡黄色固体,该化合物的电子式为
(3)Z、W、N 的简单离子半径从大到小的顺序:
(4)甲和乙是由上述元素 X 分别与元素 Y、Z 形成的 10 电子分子,沸点
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、Q、R是原子序数依次增大的短周期主族元素。已知:气体YX3能使润湿的紫色石蕊试纸变蓝,Z和X在同一主族,Q原子的最外层电子数是其周期序数的2倍。回答下列问题:
(1) 原子的结构示意图为
原子的结构示意图为 _____ ,YX3的化学式为 _____ 。
(2) 、Q、R原子的半径从大到小的顺序是
、Q、R原子的半径从大到小的顺序是 ___________ 。 用原子符号表示
用原子符号表示 。
。
(3) 分别与X、Z形成的化合物分别是
分别与X、Z形成的化合物分别是__________ (填化学式),___________ (填电子式)。Q与Z形成的化合物类型是_________ (填离子化合物或共价化合物)。
(4)能证明R的非金属性比Q强的实验事实是______  填字母序号
填字母序号 。
。
A HR的水溶液酸性比H2Q的水溶液酸性强 B R2与H2化合比Q与H2化合容易。
C R的最高价氧化物的水化物的酸性比Q的强 D HR的稳定性比H2Q强
(1)
 原子的结构示意图为
原子的结构示意图为 (2)
 、Q、R原子的半径从大到小的顺序是
、Q、R原子的半径从大到小的顺序是  用原子符号表示
用原子符号表示 。
。(3)
 分别与X、Z形成的化合物分别是
分别与X、Z形成的化合物分别是(4)能证明R的非金属性比Q强的实验事实是
 填字母序号
填字母序号 。
。A HR的水溶液酸性比H2Q的水溶液酸性强 B R2与H2化合比Q与H2化合容易。
C R的最高价氧化物的水化物的酸性比Q的强 D HR的稳定性比H2Q强
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
请回答下列问题:
(1)属于卤族元素的有_______ (填元素符号,下同);属于碱金属元素的有_______ 。
(2)②③原子结构的相同点是_______ 。
(3)画出元素④的原子结构示意图:_______ ;元素④与⑤同属于_______ 族;预测它们单质的化学性质的相似性是_______ 。
(4)元素⑥与⑦的原子最外层电子数都为_______ ;单质的氧化性:⑥_______ (填“>”或“<”)⑦,其依据是_______ 。
(5)写出一种由上述九种元素中的三种不同主族元素组成的离子化合物的化学式:_______ (任写一种)。
| 周期 | IA | 0 | ||||||
| 一 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 二 | ⑥ | |||||||
| 三 | ② | ④ | ⑦ | ⑧ | ||||
| 四 | ③ | ⑤ | ⑨ |
(1)属于卤族元素的有
(2)②③原子结构的相同点是
(3)画出元素④的原子结构示意图:
(4)元素⑥与⑦的原子最外层电子数都为
(5)写出一种由上述九种元素中的三种不同主族元素组成的离子化合物的化学式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,按要求回答下列问题:
I.
(1)⑧的单质的电子式为_______ 。
(2)①~⑧对应元素中,非金属性最强的是_______ (填元素符号)。
(3)⑤⑥两种元素的最高价氧化物对应水化物中,碱性最强的是_______ (填化学式)。
(4)实验室用 和
和 制备②的简单氢化物,其化学方程式为
制备②的简单氢化物,其化学方程式为_______ 。
(5)下列不能用于验证氯元素比硫元素非金属性强的依据是_______(填字母)。
II. 是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。
是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。
工业上用废铁锈(主要成分为 ,含少量的
,含少量的 与Cu)制取绿矾(
与Cu)制取绿矾( )的流程图如下。请回答下列问题。
)的流程图如下。请回答下列问题。

(6)X与Y分别为_______ 、_______ (填化学式)。
(7)废铁锈加入过量 溶液发生的离子方程式为
溶液发生的离子方程式为_______ 。
(8)流程中获得的Cu,可用铁盐溶解,写出反应的离子方程式为_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)⑧的单质的电子式为
(2)①~⑧对应元素中,非金属性最强的是
(3)⑤⑥两种元素的最高价氧化物对应水化物中,碱性最强的是
(4)实验室用
 和
和 制备②的简单氢化物,其化学方程式为
制备②的简单氢化物,其化学方程式为(5)下列不能用于验证氯元素比硫元素非金属性强的依据是_______(填字母)。
A. 比 比 稳定 稳定 |
B.铁与 反应生成 反应生成 ,而铁与硫反应生成 ,而铁与硫反应生成 |
C. 的酸性比 的酸性比 的强 的强 |
D. 的氧化性比 的氧化性比 的强 的强 |
II.
 是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。
是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。工业上用废铁锈(主要成分为
 ,含少量的
,含少量的 与Cu)制取绿矾(
与Cu)制取绿矾( )的流程图如下。请回答下列问题。
)的流程图如下。请回答下列问题。
(6)X与Y分别为
(7)废铁锈加入过量
 溶液发生的离子方程式为
溶液发生的离子方程式为(8)流程中获得的Cu,可用铁盐溶解,写出反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:__ 。F在周期表中的位置__ 。
(2)B、D形成的化合物BD2中存在的化学键为__ 键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为__ 化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为__ 。
(4)A、C、D、E的原子半径由大到小的顺序是__ (用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性___ 于F(填“强”或“弱”),并用化学方程式证明上述结论__ 。
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:
(2)B、D形成的化合物BD2中存在的化学键为
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为
(4)A、C、D、E的原子半径由大到小的顺序是
(5)元素B和F的非金属性强弱,B的非金属性
您最近一年使用:0次



