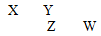根据元素周期表判断下列描述正确的是
| A.元素周期表中,总共有16个纵行,16个族 |
| B.第IA族的元素又称为碱金属元素,第VIIA族的元素又称为卤族元素 |
| C.每个短周期都既包含金属元素也包含非金属元素 |
| D.在金属和非金属元素分界线附近可以寻找制作半导体材料的元素 |
更新时间:2019-04-09 09:28:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】Fe为过渡金属元素,在工业生产中具有重要的用途。已知NO能被FeSO4溶液吸收生成配合物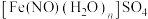 ,该配合物的中心离子的最外层电子数与配体提供的电子总数之和为26.下列有关说法正确的是
,该配合物的中心离子的最外层电子数与配体提供的电子总数之和为26.下列有关说法正确的是
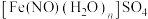 ,该配合物的中心离子的最外层电子数与配体提供的电子总数之和为26.下列有关说法正确的是
,该配合物的中心离子的最外层电子数与配体提供的电子总数之和为26.下列有关说法正确的是A.该配合物的化学式为 |
| B.该配合物中所含非金属元素均位于元素周期表p区 |
C.1mol该配合物与足量 溶液反应可生成1mol沉淀 溶液反应可生成1mol沉淀 |
| D.该配合物中阳离子呈正八面体结构,阴离子呈正四面体结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】X、Y、Z、W是原子序数依次增大的四种短周期元素,X、W同主族,Y、Z、W同周期,其中只有Y为金属元素,W元素最高正价与最低负价的代数和为4.下列说法不正确的是( )
| A.原子半径:Y>Z>W>X |
| B.Y与X形成的化合物不可能含有共价键 |
| C.简单氢化物的稳定性:X>W>Z |
| D.Z与X形成的化合物能与NaOH溶液反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| B.Cs和Ba分别位于第六周期ⅠA和ⅡA族,碱性:CsOH>Ba(OH)2 |
| C.第三周期非金属元素最高价氧化物对应水化物酸性从左到右依次增强 |
| D.若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在1981年才第一次制得卤族元素的第五个成员砹,根据卤素性质的变化规律,我们可以预料砹的下列性质不正确的是( )
| A.砹单质在室温下的状态是固体,颜色比碘深,单质能溶于四氯化碳 |
| B.砹原子得电子能力比碘强 |
| C.AgAt的颜色比AgI深,HAt的稳定性比HI弱 |
| D.单质砹是卤素中弱氧化剂,而砹离子是卤族中的强还原剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于化学用语或元素原子结构的说法正确的是
A. 的电子式为: 的电子式为: |
B. 的价电子排布式为: 的价电子排布式为: |
| C.元素周期表p区元素都是非金属元素 |
D.原子核外电子从 跃迁至 跃迁至 时释放能量 时释放能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法不正确的是
| A.某短周期元素最外层有2个电子,则其一定是第ⅡA族元素 |
| B.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 |
| C.元素周期表有7个周期16个族 |
| D.117号元素Ts位于周期表的第七周期第ⅦA族 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列由事实得出的推断结论不 正确的是
| 选项 | 事实 | 推断结论 |
| A |  为正四面体结构 为正四面体结构 |  也为正四面体结构 也为正四面体结构 |
| B |  是半导体材料 是半导体材料 |  也是半导体材料 也是半导体材料 |
| C |  的原子序数为29 的原子序数为29 | 基态 中电子占据的原子轨道数目为14 中电子占据的原子轨道数目为14 |
| D | 第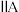 族基态原子最外层电子数都是2 族基态原子最外层电子数都是2 | 基态原子外围电子排布为 的元素位于第5周期 的元素位于第5周期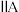 族 族 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法中正确的是( )


| A.W的原子序数不可能是X的原子序数的3倍 |
| B.Z元素可能是金属元素 |
| C.四种元素的原子有可能均能与氢原子形成18电子分子 |
| D.W的气态氢化物的稳定性一定比Y的强 |
您最近一年使用:0次

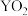 和
和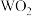 均属于酸性氧化物
均属于酸性氧化物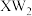 中各原子最外层均达到8电子稳定结构
中各原子最外层均达到8电子稳定结构