短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断正确的是
| A.E位于元素周期表的ⅣA族 | B.E是一种非金属元素 |
| C.在ECln中E与Cl之间形成共价键 | D.E的氧化物的化学式为EO2 |
更新时间:2019-05-07 15:44:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】X元素的阳离子和Y元素的阴离子具有相同的电子层结构,下列叙述正确的是
| A.原子序数:X<Y | B.原子半径:X<Y |
| C.非金属性:X>Y | D.电负性:X<Y |
您最近一年使用:0次
【推荐2】A、M、B、C、D、E、F、G分别是周期表中的短周期主族元素,其原子序数依次增大,A、E同主族,E、F同周期,D、F同主族,且D的质子数是F质子数的一半,M、B、C、D能与A分别形成电子总数相同的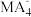 离子、X分子、Y分子、Z分子,下列判断不正确的是
离子、X分子、Y分子、Z分子,下列判断不正确的是
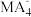 离子、X分子、Y分子、Z分子,下列判断不正确的是
离子、X分子、Y分子、Z分子,下列判断不正确的是| A.气态氢化物的稳定性:G>F |
| B.lmoA2D2分解时转移的电子数为2NA |
| C.熔沸点:Z>X |
| D.已知AGD4与EMA4发生氧化还原反应产生A2,则A2既是氧化产物,也是还原产物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】短周期主族元素X、Y、Z、M的原子序数依次增大,Z的基态原子的2p轨道半充满,M的最高正价与最低负价的绝对值之差为4,由这4种元素组成的一种分子的结构如图所示。下列说法正确的是
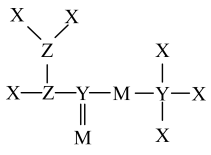

| A.电负性:M<Y |
| B.Y氢化物的沸点可能高于Z氢化物的沸点 |
| C.第一电离能:Y>Z |
| D.X与Z、M形成的化合物中,一定不含离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于晶体说法正确的是( )
| A.金属晶体的熔沸点均高于分子晶体 |
| B.含有阳离子的晶体一定是离子晶体 |
| C.SiO2一定具有多面体外形 |
| D.金属导电和熔融电解质(或电解质溶液)导电的原理不一样 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族, 与
与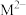 具有相同的电子层结构,离子半径
具有相同的电子层结构,离子半径 ,Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是
,Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是
 与
与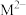 具有相同的电子层结构,离子半径
具有相同的电子层结构,离子半径 ,Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是
,Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是| A.X、M两种元素形成的两种化合物的晶体类型不同 |
| B.W、Z、M元素的氢化物都是分子晶体,其沸点依次降低 |
| C.元素Y、Z、W的单质晶体属于同种类型的晶体 |
| D.元素Y和M形成的化合物具有较大的硬度和较高的熔点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.SO2和SiO2 化学键类型完全相同,晶体类型也相同 |
| B.某物质固态能导电,则它不一定是金属单质 |
| C.冰、Na2SO4分别加热熔化,需要克服相同类型作用力 |
| D.C2H4中所有原子满足8电子结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列物质属于原子晶体的是( )
| A.熔点是1070℃,易溶于水,水溶液能导电 |
| B.熔点是10.31℃,液态不导电,水溶液能导电 |
| C.不溶于水,熔点3550℃,不导电 |
| D.熔点是97.80℃,质软、导电,密度是0.97g•cm-3. |
您最近一年使用:0次