如图是某粒子的结构示意图,试回答:
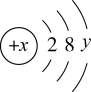
(1)当x-y=10时,该粒子为________ (填“原子”、“阳离子”或“阴离子”)。
(2)当y=8时,该粒子可能是(写微粒符号):______ 、______ 、_____ 、_____ 、_____ ;按离子半径从大到小顺序排列上述离子:____________ 。
(3)写出y=3的元素最高价氧化物对应的水化物与NaOH溶液发生反应的离子方程式______________ 。

(1)当x-y=10时,该粒子为
(2)当y=8时,该粒子可能是(写微粒符号):
(3)写出y=3的元素最高价氧化物对应的水化物与NaOH溶液发生反应的离子方程式
更新时间:2019-05-04 17:34:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)①基态Cu原子有______ 种不同能级的电子。
②N原子中最高能级的电子的电子云轮廓图为______ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(2)元素X位于第四周期,其基态原子有4个未成对电子,基态X2+的价电子排布式是________ ;X3+的价电子排布式为________ 。
(3)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,M元素基态原子的电子排布式为____ ,M+的价电子排布式为____ ,M2+的电子排布式为________ 。
(1)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(2)元素X位于第四周期,其基态原子有4个未成对电子,基态X2+的价电子排布式是
(3)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,M元素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空:
(1)如图是常用于混合物的分离和提纯的装置:

①仪器a的名称是___________ 。
②利用图1装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器是___________ ,仪器a中冷凝水应该从___________ (填“上”或“下”)口进。
③从碘的饱和水溶液中提取碘应选择图___________ (填序号)装置,该实验要用到萃取剂,下列关于所加萃取剂的说法不正确的是___________ (填字母)。
A.该萃取剂不与碘反应 B.碘在该萃取剂中的溶解度比在水中的溶解度大
C.该萃取剂与水不互溶 D.该萃取剂的密度必须比水的密度大
(2)有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的 ,乙元素原子核内无中子,丙元素原子核内有8个质子。
,乙元素原子核内无中子,丙元素原子核内有8个质子。
①写出甲、乙、丙三种元素组成的化合物在水中的电离方程式___________ 。
②画出甲元素的离子结构示意图___________ 。
(3)从V mL 溶液中,取
溶液中,取 mL溶液稀释到4V mL,此时溶液中
mL溶液稀释到4V mL,此时溶液中 物质的量浓度a mol/L,则原溶液中含
物质的量浓度a mol/L,则原溶液中含 的物质的量浓度是
的物质的量浓度是___________ 。
(4)“人造空气”(氧气与氦气的混合气体)可用于减轻某些病痛或供深水潜水员,标准状况下,22.4 L“人造空气”的质量是9.6 g,其中氧气与氦气的体积比为___________ 。
(5)用 作催化剂,在废水中加入
作催化剂,在废水中加入 可以去除废水中的有机物(TOC)。在酸性条件下,
可以去除废水中的有机物(TOC)。在酸性条件下, 的加入量对TOC的去除效果如图所示,则
的加入量对TOC的去除效果如图所示,则 的浓度为
的浓度为___________ mol⋅L 时,废水中TOC去除效果最好。
时,废水中TOC去除效果最好。

(1)如图是常用于混合物的分离和提纯的装置:

①仪器a的名称是
②利用图1装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器是
③从碘的饱和水溶液中提取碘应选择图
A.该萃取剂不与碘反应 B.碘在该萃取剂中的溶解度比在水中的溶解度大
C.该萃取剂与水不互溶 D.该萃取剂的密度必须比水的密度大
(2)有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的
 ,乙元素原子核内无中子,丙元素原子核内有8个质子。
,乙元素原子核内无中子,丙元素原子核内有8个质子。①写出甲、乙、丙三种元素组成的化合物在水中的电离方程式
②画出甲元素的离子结构示意图
(3)从V mL
 溶液中,取
溶液中,取 mL溶液稀释到4V mL,此时溶液中
mL溶液稀释到4V mL,此时溶液中 物质的量浓度a mol/L,则原溶液中含
物质的量浓度a mol/L,则原溶液中含 的物质的量浓度是
的物质的量浓度是(4)“人造空气”(氧气与氦气的混合气体)可用于减轻某些病痛或供深水潜水员,标准状况下,22.4 L“人造空气”的质量是9.6 g,其中氧气与氦气的体积比为
(5)用
 作催化剂,在废水中加入
作催化剂,在废水中加入 可以去除废水中的有机物(TOC)。在酸性条件下,
可以去除废水中的有机物(TOC)。在酸性条件下, 的加入量对TOC的去除效果如图所示,则
的加入量对TOC的去除效果如图所示,则 的浓度为
的浓度为 时,废水中TOC去除效果最好。
时,废水中TOC去除效果最好。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y 原子最外层电子数是次外层电子数的2倍:Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1) 元素X原子结构示意图为_________________ 。
(2) 元素Y的一种同位素可测定文物年代,这种同位素的符号是______________ 。
(3) 元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为_________________________ 。
(4) ZW3可与水反应生成一种酸和一种碱,反应的化学方程式为_________________________________ 。
(1) 元素X原子结构示意图为
(2) 元素Y的一种同位素可测定文物年代,这种同位素的符号是
(3) 元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为
(4) ZW3可与水反应生成一种酸和一种碱,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】A、B、C是三种元素的原子,质子数都小于18。A原子与B原子的最外层电子数都是6,A原子与C原子的核外电子层数都为3, C原子的质子数比A少4。回答下列问题:
(1)A、B、C的元素名称分别为________ 、________ 、________ ;
(2)A的离子结构示意图为________ ;
(3)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为_______ 。
(1)A、B、C的元素名称分别为
(2)A的离子结构示意图为
(3)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
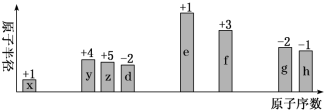
根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
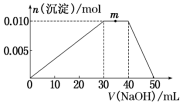
(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________ 。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是
(2)写出m点反应的离子方程式:
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。 请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)________________ 。
(2)X与Y能形成多种化合物,其中相对分子质量最小的分子中只含有_________ 键(填“离子”、“极性”或“非极性”)。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系: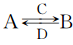 (在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。
(在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。
写出C的结构式:________ ;D的电子式:________ 。
①如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式为________________ 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。由A转化为B的离子方程式为___________________ 。(提示:强酸弱碱盐显酸性,强碱弱酸显碱性)
(1)五种元素原子半径由大到小的顺序是(写元素符号)
(2)X与Y能形成多种化合物,其中相对分子质量最小的分子中只含有
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
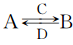 (在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。
(在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:
①如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式为
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。由A转化为B的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】原子中各粒子的作用
(1)___________ 数决定元素种类,同种元素的不同___________ ,其___________ 数相同,___________ 数不同。
(2)___________ 数和___________ 数共同决定了原子(核素)的种类。
(3)元素的化学性质决定于___________ ,特别是___________ 是决定元素化学性质的主要因素。
(1)
(2)
(3)元素的化学性质决定于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是_____
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是_________ ;只由极性共价键构成的物质是_____ ;由极性键和非极性键构成的物质是_______ ;由离子键和极性键构成的物质是_______ 。(填序号)极性共价键与非极性共价键的判断方法_____________________
(3)写出下列物质的电子式:CaF2:_______ CO2:_______ NH4Cl:__________
(4) 用电子式表示下列化合物的形成过程
H2S:__________________________________
MgF2:___________
请归纳物质电子式的书写及用电子式表示化合物的形成过程应注意哪些问题_______________
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是
(3)写出下列物质的电子式:CaF2:
(4) 用电子式表示下列化合物的形成过程
H2S:
MgF2:
请归纳物质电子式的书写及用电子式表示化合物的形成过程应注意哪些问题
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请完成下列问题:
(1)画出氯原子结构示意图___ 。
(2)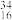 S2-微粒中的质子数是
S2-微粒中的质子数是___ ,中子数是___ 。
(3)49g硫酸的物质的量为___ mol,其完全电离产生H+的个数为___ 。
(4)写出实验室制氯气的离子方程式:___ 。
(1)画出氯原子结构示意图
(2)
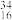 S2-微粒中的质子数是
S2-微粒中的质子数是(3)49g硫酸的物质的量为
(4)写出实验室制氯气的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空。
(1)下列物质中属于同位素的是__________ ;属于同素异形体的是__________ 。
A.O2、O3 B. Cl和
Cl和 Cl
Cl
C.Fe2+、Fe3+ D.H2O、D2O、T2O
(2)据报道,某些花岗岩会产生放射性的稀有气体氡,从而对人体产生伤害,请将以下Rn的原子结构示意图补全。_______

(3)下列四种物质中①Ar,②CO2,③K2S,④NaOH,只有存在共价键的物质是___ ;(填编号)用电子式表示③的形成过程:__________ 。
(4)硅酸盐的组成比较复杂,常用氧化物的形式表示。石棉Mg3Ca(SiO3)4表示为氧化物形式为:__________ 。
(5)若K37ClO3+6H35C1===KCl+3Cl2↑+3H2O,则此反应中生成氯气的相对分子质量约为_________ (计算结果保留三位有效数字)。
(6)将NaHSO4溶于水,破坏了NaHSO4中的______ (填化学键类型),NaHSO4在熔融状态下电离,破坏了______ (填化学键类型),写出其在熔融状态下的电离方程式_____________ 。
(1)下列物质中属于同位素的是
A.O2、O3 B.
 Cl和
Cl和 Cl
Cl C.Fe2+、Fe3+ D.H2O、D2O、T2O
(2)据报道,某些花岗岩会产生放射性的稀有气体氡,从而对人体产生伤害,请将以下Rn的原子结构示意图补全。

(3)下列四种物质中①Ar,②CO2,③K2S,④NaOH,只有存在共价键的物质是
(4)硅酸盐的组成比较复杂,常用氧化物的形式表示。石棉Mg3Ca(SiO3)4表示为氧化物形式为:
(5)若K37ClO3+6H35C1===KCl+3Cl2↑+3H2O,则此反应中生成氯气的相对分子质量约为
(6)将NaHSO4溶于水,破坏了NaHSO4中的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有原子序数依次增大的A、B、C、D、E五种元素,A是短周期中族序数等于周期数的非金属元素;B元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;C元素的价电子构型为nsnnpn+1;D的最外层电子数与电子层数之比为3:1;E是地壳中含量仅次于铝的金属元素,其合金用途最广,用量最大。
(1)E元素在周期表中的位置__________ ;E元素价电子排布式为__________ 。
(2)A分别与B、C、D能形成电子数为10的化合物,它们的沸点由高到低的顺序是______ (写分子式)。
(3)B与D形成的非极性分子的电子式为________ 。
(4)B、C、D三种元素的第一电离能由大到小的顺序是_____ (用元素符号表示)。
(5)C的单质分子中σ键和π键的个数比为________ 。
(6)已知在25℃、101kPa下:ABC(aq)+A2D(l)=BC-(aq)+A3D+(aq) ΔH=+45.6kJ·mol-1
A3D+(aq)+DA-(aq)=2A2D(l)ΔH=-57.3kJ·mol-1
则在25℃、101kPa的稀溶液中,ABC与DA-反应的热化学方程式是(以离子方程式表示):_______ 。
(1)E元素在周期表中的位置
(2)A分别与B、C、D能形成电子数为10的化合物,它们的沸点由高到低的顺序是
(3)B与D形成的非极性分子的电子式为
(4)B、C、D三种元素的第一电离能由大到小的顺序是
(5)C的单质分子中σ键和π键的个数比为
(6)已知在25℃、101kPa下:ABC(aq)+A2D(l)=BC-(aq)+A3D+(aq) ΔH=+45.6kJ·mol-1
A3D+(aq)+DA-(aq)=2A2D(l)ΔH=-57.3kJ·mol-1
则在25℃、101kPa的稀溶液中,ABC与DA-反应的热化学方程式是(以离子方程式表示):
您最近一年使用:0次

 、
、 、
、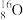 、
、 、
、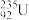 、
、 中
中

