肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1
(1)写出肼(l)和N2O4(l)完全反应生成N2和水蒸气时的热化学方程式:__________ 。
(2)已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,O—H为462,则断裂1 mol N—H键所需的能量是________ kJ。
①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1
(1)写出肼(l)和N2O4(l)完全反应生成N2和水蒸气时的热化学方程式:
(2)已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,O—H为462,则断裂1 mol N—H键所需的能量是
18-19高一下·陕西渭南·期中 查看更多[2]
更新时间:2019-06-05 08:28:46
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】在恒温(500K)、体积为2.0L的密闭容器中通入1.0molN2和1molH2发生合成氨反应,20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的总物质的量为1.6mol。
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率v(NH3)=______ 。
(2)该反应的热化学方程式为______ 。
(3)若拆开1molH—H键和1molN N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是
N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是______ kJ。
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率v(NH3)=
(2)该反应的热化学方程式为
(3)若拆开1molH—H键和1molN
 N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是
N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】200mL 0.200mol/L CuSO4溶液与3.90g锌粉在量热计中充分反应。测得反应前温度为18.1℃,反应后最高温度为28.1℃。已知:反应前后,溶液的比热容均近似为4.18 J⋅g-1⋅C-1、溶液的密度均近似为1.00g/cm3,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=___________ J。
(2)反应Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)的∆H=___________ kJ/mol(列式计算)。
(1)反应放出的热量Q=
(2)反应Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)的∆H=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
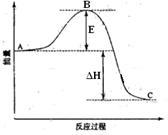
(1)图中A、C分别表示______ 、______ ,E的大小对该反应的反应热有无影响?_______ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________ ,理由是________________________ ;
(2)图中△H=__ KJ·mol-1;
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H__ (要求写计算过程)。

(1)图中A、C分别表示
(2)图中△H=
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】下图是CO和水蒸气发生反应生成CO2和H2的途径和三个状态的能量,该反应为吸热反应,试问:
E1:CO+H2O E2:C+2H+2O
E2:C+2H+2O E3:CO2+H2
E3:CO2+H2
(1)步骤1、2分别是吸热过程还是放热过程?
步骤1:______ ,步骤2:______ 。
(2)比较E1、E3的大小______ 。
(3)已知,25℃时,C(石墨)+1/2O2(g) ═ CO(g) ΔH1=-111 kJ/mol;
H2(g)+1/2O2(g) ═ H2O(g) ΔH2=-242 kJ/mol;
C(石墨)+O2(g) ═ CO2(g) ΔH3=-394 kJ/mol。
则CO和H2O(g)反应的热化学方程式为:______ 。
(4)含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应放出114.6 kJ的热量,写出该反应中和热的热化学方程式:______ 。
(5)在C2H2(g)完全燃烧生成CO2和液态水的反应中,每转移5NA个电子放出a kJ的热量。则表示C2H2的燃烧热的热化学方程式为:______ 。
E1:CO+H2O
 E2:C+2H+2O
E2:C+2H+2O E3:CO2+H2
E3:CO2+H2(1)步骤1、2分别是吸热过程还是放热过程?
步骤1:
(2)比较E1、E3的大小
(3)已知,25℃时,C(石墨)+1/2O2(g) ═ CO(g) ΔH1=-111 kJ/mol;
H2(g)+1/2O2(g) ═ H2O(g) ΔH2=-242 kJ/mol;
C(石墨)+O2(g) ═ CO2(g) ΔH3=-394 kJ/mol。
则CO和H2O(g)反应的热化学方程式为:
(4)含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应放出114.6 kJ的热量,写出该反应中和热的热化学方程式:
(5)在C2H2(g)完全燃烧生成CO2和液态水的反应中,每转移5NA个电子放出a kJ的热量。则表示C2H2的燃烧热的热化学方程式为:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH1=-112.3 kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) ΔH2=-234 kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=179.5 kJ·mol-1
请写出CO和NO2生成N2、CO2的热化学方程式_________________________ 。
(2)亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g) 2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):
2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):
则2NO(g)+C12(g) 2C1NO(g)反应的ΔH和a的关系为ΔH=
2C1NO(g)反应的ΔH和a的关系为ΔH=________ kJ·mol-1。
(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH1=-112.3 kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) ΔH2=-234 kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=179.5 kJ·mol-1
请写出CO和NO2生成N2、CO2的热化学方程式
(2)亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g)
 2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):
2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):| 化学键 | N≡O | Cl- Cl | Cl-N | N=O |
| 键能/kJ·mol-1 | 630 | 243 | a | 607 |
则2NO(g)+C12(g)
 2C1NO(g)反应的ΔH和a的关系为ΔH=
2C1NO(g)反应的ΔH和a的关系为ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】完成下列填空
(1)已知下列两个热化学方程式: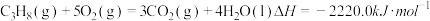 ,
,
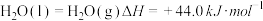 ,则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为
,则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为___________ kJ
(2)已知:8g的CH4与足量的O2反应,生成CO2和液态水,放出445.15kJ的热量写出表示甲烷燃烧热的热化学方程式:___________ 。
(3)足量H2在1molO2中完全燃烧生成 液态水,放出571.6kJ的热量,
液态水,放出571.6kJ的热量, 的燃烧热ΔH=
的燃烧热ΔH=___________ 。
(4)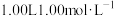 硫酸与2.00L1.00mol/LNaOH溶液完全反应,放出
硫酸与2.00L1.00mol/LNaOH溶液完全反应,放出 的热量,表示其中和热的热化学方程式为
的热量,表示其中和热的热化学方程式为___________ 。
(5)已知: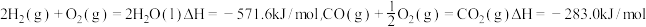 。某H2和CO的混合气体完全燃烧时放出113.84热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为
。某H2和CO的混合气体完全燃烧时放出113.84热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为___________ 。
(1)已知下列两个热化学方程式:
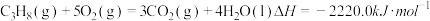 ,
,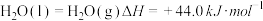 ,则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为
,则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为(2)已知:8g的CH4与足量的O2反应,生成CO2和液态水,放出445.15kJ的热量写出表示甲烷燃烧热的热化学方程式:
(3)足量H2在1molO2中完全燃烧生成
 液态水,放出571.6kJ的热量,
液态水,放出571.6kJ的热量, 的燃烧热ΔH=
的燃烧热ΔH=(4)
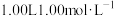 硫酸与2.00L1.00mol/LNaOH溶液完全反应,放出
硫酸与2.00L1.00mol/LNaOH溶液完全反应,放出 的热量,表示其中和热的热化学方程式为
的热量,表示其中和热的热化学方程式为(5)已知:
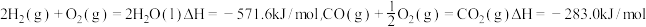 。某H2和CO的混合气体完全燃烧时放出113.84热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为
。某H2和CO的混合气体完全燃烧时放出113.84热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】试从化学键的角度理解化学反应中的能量变化。(以2H2+O2=2H2O为例说明),已知:E反表示反应物(2H2+O2)所具有的总能量,E生表示生成物(2H2O)所具有的总能量。又知:拆开1moL H2中的化学键需要吸收436kJ能量,拆开1moL O2中的化学键需要吸收496kJ能量,形成水分子中的1moLH—O键能够释放463KJ能量。
(1)从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=_______ kJ;形成生成物中的化学键放出的总能量为=________ kJ。所以该反应要_____ (填“吸收”或“放出”)能量,能量变化值的大小△E=_______ kJ(填数值)
(2)由图可知,化学反应的本质是_____ 化学反应中能量变化的主要原因是_____ (从总能量说明)
(1)从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=
(2)由图可知,化学反应的本质是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)对温室气体CO2进行减排和综合治理具有十分重要的意义。CH4•CO2催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。
已知:①CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2kJ•mol﹣1
②CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H2=+165.0kJ•mol﹣1
写出该催化重整反应的热化学方程式:___________ 。
(2)若适量的N2和O2完全反应,每生成92gNO2需要吸收67.8kJ热量,则表示该反应的热化学方程式为___________ 。
(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(1)放出571.6k]的热量,则表示H2燃烧热的热化学方程式为___________ 。
(4)我国是世界上第二大乙烯生产国,乙烯可由乙烷裂解得到;C2H6(g) C2H4(g)+H2(g),相关化学键的键能数据如表所示,则上述反应的△H等于
C2H4(g)+H2(g),相关化学键的键能数据如表所示,则上述反应的△H等于 ___________ 。
(5)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g) △H1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2
再燃料水煤气:2CO(g)+O2(g)=2CO2(g) △H3
2H2(g)+O2(g)=2H2O(g) △H4
则△H1=___________ (用△H2、△H3、△H4表示)。
(1)对温室气体CO2进行减排和综合治理具有十分重要的意义。CH4•CO2催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。
已知:①CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2kJ•mol﹣1
②CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H2=+165.0kJ•mol﹣1
写出该催化重整反应的热化学方程式:
(2)若适量的N2和O2完全反应,每生成92gNO2需要吸收67.8kJ热量,则表示该反应的热化学方程式为
(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(1)放出571.6k]的热量,则表示H2燃烧热的热化学方程式为
(4)我国是世界上第二大乙烯生产国,乙烯可由乙烷裂解得到;C2H6(g)
 C2H4(g)+H2(g),相关化学键的键能数据如表所示,则上述反应的△H等于
C2H4(g)+H2(g),相关化学键的键能数据如表所示,则上述反应的△H等于 | 化学键 | C﹣H | C﹣C | C=C | H﹣H |
| 键能/(kJ•mol﹣1) | 410 | 345 | 610 | 430 |
(5)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g) △H1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2
再燃料水煤气:2CO(g)+O2(g)=2CO2(g) △H3
2H2(g)+O2(g)=2H2O(g) △H4
则△H1=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】依据题意完成下列各小题。
(1)已知下列反应:SO2(g)+2OH-(aq)=SO (aq)+H2O(l) ΔH1,ClO-(aq)+SO
(aq)+H2O(l) ΔH1,ClO-(aq)+SO (aq)=SO
(aq)=SO (aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+SO
(aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+SO (aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
(aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=______________ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1②CH3OH(g)+ O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式:
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式: __________________ 。
(3)下表是部分化学键的键能数据,已知1 mol白磷(P4)完全燃烧放热为d kJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中x=________ kJ·mol-1(用含有a、b、c、d的代数式表示)。
(4)①2O2(g)+N2(g)=N2O4(l) ΔH1②N2(g)+2H2(g)=N2H4(l) ΔH2③O2(g)+
2H2(g)=2H2O(g) ΔH3④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)ΔH4=-1 048.9 kJ·mol-1
上述反应热效应之间的关系式为ΔH4=_____________________________________________ ,
联氨和N2O4可作为火箭推进剂的主要原因为______________________________________ 。
(5)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g) CH3OH(g) ΔH1②CO2(g)+3H2(g)
CH3OH(g) ΔH1②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2③CO2(g)+H2(g)
CH3OH(g)+H2O(g) ΔH2③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3,已知反应①中相关的化学键键能数据如下:
CO(g)+H2O(g) ΔH3,已知反应①中相关的化学键键能数据如下:
由此计算ΔH1=____ kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=_____ kJ·mol-1。
(6)已知反应2HI(g)=H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为____________ kJ。
(1)已知下列反应:SO2(g)+2OH-(aq)=SO
 (aq)+H2O(l) ΔH1,ClO-(aq)+SO
(aq)+H2O(l) ΔH1,ClO-(aq)+SO (aq)=SO
(aq)=SO (aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+SO
(aq)+Cl-(aq) ΔH2,CaSO4(s)=Ca2+(aq)+SO (aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
(aq) ΔH3,则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式:
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式: (3)下表是部分化学键的键能数据,已知1 mol白磷(P4)完全燃烧放热为d kJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中x=
化学键 | P—P | P—O | O=O | P=O |
键能/(kJ·mol-1) | a | b | c | x |
2H2(g)=2H2O(g) ΔH3④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)ΔH4=-1 048.9 kJ·mol-1
上述反应热效应之间的关系式为ΔH4=
联氨和N2O4可作为火箭推进剂的主要原因为
(5)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g)
 CH3OH(g) ΔH1②CO2(g)+3H2(g)
CH3OH(g) ΔH1②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2③CO2(g)+H2(g)
CH3OH(g)+H2O(g) ΔH2③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3,已知反应①中相关的化学键键能数据如下:
CO(g)+H2O(g) ΔH3,已知反应①中相关的化学键键能数据如下:化学键 | H—H | C—O | C≡O | H—O | C—H |
E/(kJ·mol-1) | 436 | 343 | 1 076 | 465 | 413 |
(6)已知反应2HI(g)=H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为
您最近一年使用:0次



