有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;V和Z元素原子的最外层都只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子的L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。
回答下列问题:
(1)V的一种核素中质子数为中子数的 ,则该核素的名称为
,则该核素的名称为________ ,常用于制造________ 。
(2)W元素在周期表中的位置为_______________________________ 。
(3)X元素的离子结构示意图为________ 。
(4)Z的最高价氧化物对应水化物的化学式为:_________________________ 。
回答下列问题:
(1)V的一种核素中质子数为中子数的
 ,则该核素的名称为
,则该核素的名称为(2)W元素在周期表中的位置为
(3)X元素的离子结构示意图为
(4)Z的最高价氧化物对应水化物的化学式为:
18-19高一下·甘肃武威·期中 查看更多[2]
更新时间:2019-06-11 14:58:37
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F为短周期元素,其中C的原子序数最小,它们的最高正价与原子半径关系如图所示。

回答下列问题:
(1)F离子结构示意图为_______ ;化合物EF2的化学式为_______ 。
(2)从原子结构角度解释A金属性强于B的原因:_______ 。
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为_______ ,写出CE2在足量O2中燃烧的化学方程式_______ 。
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有_______ (填“离子键”、“极性键”或“非极性键”)。
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为_______ 。

回答下列问题:
(1)F离子结构示意图为
(2)从原子结构角度解释A金属性强于B的原因:
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有A、B、C、D、E五种短周期元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子:D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8,E与B的质量比为1:1。试回答:
(1)写出D元素基态原子的电子排布式:____ 。
(2)写出AB2的结构式:____ 。
(3)B、C两元素的第一电离能大小关系为____ (填元素符号),原因是____ 。
(4)根据VSEPR模型预测C的氢化物的立体结构为____ ,中心原子C的轨道杂化类型为____ 。
(5)B、D两元素的气态氢化物的稳定性大小关系为____ (填化学式)。
(1)写出D元素基态原子的电子排布式:
(2)写出AB2的结构式:
(3)B、C两元素的第一电离能大小关系为
(4)根据VSEPR模型预测C的氢化物的立体结构为
(5)B、D两元素的气态氢化物的稳定性大小关系为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大。已知:A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2。请回答:
(1)元素C在周期表中的位置是________ 。
(2)元素D的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物与水反应的离子方程式____________________________________ 。
(3)D和E两种元素相比较,其原子得电子能力较强的是________ (写名称)。 以下说法中,可以证明上述结论的是__________ (填写编号)。
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(4)元素A、D、E与钠元素可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中反应的离子方程式是___________________________ 。
(1)元素C在周期表中的位置是
(2)元素D的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物与水反应的离子方程式
(3)D和E两种元素相比较,其原子得电子能力较强的是
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(4)元素A、D、E与钠元素可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)②元素原子的电子式是:_______ 。
(2)硅元素在周期表中的位置是:第_______ 周期_______ 族。
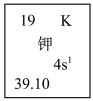
(3)如图所示钾元素的部分信息,“30.97”数值表示_______ 。______ (填元素符号)。③和⑧两种元素形成的气态氢化物稳定性强的是_______ (填化学式)。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方程式_______ 。
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因_______ 。能证明这一事实的化学反应为_______ (写一个化学方程式)。
(6)能证明O元素的非金属性强于S元素的依据是_______ 。
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是_______ 。
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是_______ 。
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是_______ 。
族 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)②元素原子的电子式是:
(2)硅元素在周期表中的位置是:第
(3)如图所示钾元素的部分信息,“30.97”数值表示
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因
(6)能证明O元素的非金属性强于S元素的依据是
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是
| A.质子数相同 | B.质量相同 |
| C.化学性质相同 | D.位置相同(周期表中) |
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
| A.在周期表中金属与非金属的分界处可以找到催化剂材料 |
| B.对氟、氯、硫、磷、砷等元素的研究,有助于制造出新品种的农药 |
| C.在过渡元素中可寻找制造半导体的元素 |
| D.可在第IA、IIA族元素中寻找制造耐高温、耐腐蚀合金的元素 |
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是
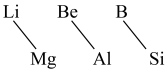
| A.Li在空气中燃烧生成Li2O、Li3N | B.硼酸是弱酸 |
| C.Be不与水反应 | D.Be(OH)2是两性氢氧化物 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】 是汽车尾气中的主要污染物,在汽车尾气系统中装配催化转化器,可有效降低
是汽车尾气中的主要污染物,在汽车尾气系统中装配催化转化器,可有效降低 的排放。
的排放。
Ⅰ.当尾气中空气不足时, (以
(以 为主)在催化转化器中被
为主)在催化转化器中被 还原成
还原成 排出。
排出。
(1)基态碳原子中,电子占据最高能级的电子云轮廓图的形状是___________ 。
(2)氧的基态原子的轨道表示式为___________ 。
(3)C、N、O第一电离能由大到小顺序为___________ ,结合原子结构和价电子排布式解释排序原因___________ 。
Ⅱ.当尾气中空气过量时,催化转化器中的金属氧化物吸收 生成盐。其吸收能力顺序如下:
生成盐。其吸收能力顺序如下: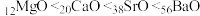 。
。
已知:镁、钙、锶、钡的部分电离能数据如下表所示。
(4)推测Sr的第三电离能a的范围:___________ 。
(5) 、
、 、
、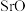 、
、 对
对 的吸收能力增强,从原子结构角度解释原因:
的吸收能力增强,从原子结构角度解释原因:___________ 元素的金属性逐渐增强,金属氧化物对 的吸收能力逐渐增强。
的吸收能力逐渐增强。
Ⅲ.研究 作为
作为 脱硝催化剂的性能时发现:在
脱硝催化剂的性能时发现:在 上适当掺杂不同的金属氧化物如
上适当掺杂不同的金属氧化物如 、
、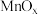 、
、 、
、 、
、 等有利于提高催化脱硝性能。
等有利于提高催化脱硝性能。
(6)基态Ⅴ原子的核外电子排布式为___________ 。
(7)若继续寻找使 催化性能更好的掺杂金属氧化物,可以在元素周期表___________区寻找恰当元素(填序号)。
催化性能更好的掺杂金属氧化物,可以在元素周期表___________区寻找恰当元素(填序号)。
 是汽车尾气中的主要污染物,在汽车尾气系统中装配催化转化器,可有效降低
是汽车尾气中的主要污染物,在汽车尾气系统中装配催化转化器,可有效降低 的排放。
的排放。Ⅰ.当尾气中空气不足时,
 (以
(以 为主)在催化转化器中被
为主)在催化转化器中被 还原成
还原成 排出。
排出。(1)基态碳原子中,电子占据最高能级的电子云轮廓图的形状是
(2)氧的基态原子的轨道表示式为
(3)C、N、O第一电离能由大到小顺序为
Ⅱ.当尾气中空气过量时,催化转化器中的金属氧化物吸收
 生成盐。其吸收能力顺序如下:
生成盐。其吸收能力顺序如下: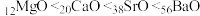 。
。已知:镁、钙、锶、钡的部分电离能数据如下表所示。
| 元素 | Mg | Ca | Sr | Ba | |
电离能( ) ) |  | 738 | 589.7 | 549 | 502.9 |
 | 1451 | 1145 | 1064 | 965.2 | |
 | 7733 | 4910 | a | 3600 |
(4)推测Sr的第三电离能a的范围:
(5)
 、
、 、
、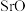 、
、 对
对 的吸收能力增强,从原子结构角度解释原因:
的吸收能力增强,从原子结构角度解释原因: 的吸收能力逐渐增强。
的吸收能力逐渐增强。Ⅲ.研究
 作为
作为 脱硝催化剂的性能时发现:在
脱硝催化剂的性能时发现:在 上适当掺杂不同的金属氧化物如
上适当掺杂不同的金属氧化物如 、
、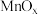 、
、 、
、 、
、 等有利于提高催化脱硝性能。
等有利于提高催化脱硝性能。(6)基态Ⅴ原子的核外电子排布式为
(7)若继续寻找使
 催化性能更好的掺杂金属氧化物,可以在元素周期表___________区寻找恰当元素(填序号)。
催化性能更好的掺杂金属氧化物,可以在元素周期表___________区寻找恰当元素(填序号)。| A.s | B.p | C.d | D.ds |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】六种短周期元素在元素周期表中的相对位置如图所示,其中R元素的最外层电子数是其次外层电子数的一半。

请回答下列问题:
(1)R的元素名称是_______ ,中子数为8的X元素的原子是______ (用原子组成符号表示)。
(2)上述六种元素,非金属性最强的元素为________________ (填元素符号)
(3)Z的最高价氧化物对应水化物的化学式为____________________ 。
(4)W和Y形成一种二元化合物甲的相对分子质量为184,且Y的质量分数约为30%。则化合物甲的化学式为__________________ 。化合物甲在摩擦时会发生猛烈爆炸,分解为一种W的单质和一种Y的单质,其中W的单质与Y的单质的相对分子质量之比为64∶7。写出化合物甲爆炸分解的化学方程式:__________________________________ 。

请回答下列问题:
(1)R的元素名称是
(2)上述六种元素,非金属性最强的元素为
(3)Z的最高价氧化物对应水化物的化学式为
(4)W和Y形成一种二元化合物甲的相对分子质量为184,且Y的质量分数约为30%。则化合物甲的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】如图是元素周期表的一部分,按要求填空。
(1)①~⑧中金属性最强的是_______ (填元素符号),画出⑨的原子结构示意图:_______ 。
(2)②③⑧中,最高价氧化物对应的水化物酸性最强的是_______ (填化学式)。
(3)⑤⑥⑦⑧四种元素中,离子半径最小的是_______ (填离子符号)。
(4)④⑧两种元素氢化物的热稳定性由强到弱的顺序为_______ (用化学式表示)。
(5)⑧的一种含氧弱酸具有强氧化性,常用于杀菌、消毒、漂白,请画出该化合物的电子式:_______ 。
(6)W是第四周期与③同主族的元素。据此推测元素W不可能具有的性质是_______(填字母)。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)①~⑧中金属性最强的是
(2)②③⑧中,最高价氧化物对应的水化物酸性最强的是
(3)⑤⑥⑦⑧四种元素中,离子半径最小的是
(4)④⑧两种元素氢化物的热稳定性由强到弱的顺序为
(5)⑧的一种含氧弱酸具有强氧化性,常用于杀菌、消毒、漂白,请画出该化合物的电子式:
(6)W是第四周期与③同主族的元素。据此推测元素W不可能具有的性质是_______(填字母)。
| A.最高正化合价为+5 |
B.气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硝酸弱 |
| D.单质在常温下可与氢气发生化合反应 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图是元素周期表的一部分,表中所列字母分别代表一种元素

回答下列问题:
(1)h元素的名称是______ ,九种元素中金属性最强的是_______ (填元素符号)。
(2)f的最高价氧化物对应的水化物的化学式____ (填化学式)。
(3)b、c、d、e的原子半径依次________ (填增大或减小)。
(4)e、h元素的氢化物中,热稳定性大的是__ (填氢化物的化学式)。
(5)化合物f2d2与化合物 a2d 反应的离子方程式__________ 。
(6)工业上冶炼g元素的单质的化学方程式__________ 。

回答下列问题:
(1)h元素的名称是
(2)f的最高价氧化物对应的水化物的化学式
(3)b、c、d、e的原子半径依次
(4)e、h元素的氢化物中,热稳定性大的是
(5)化合物f2d2与化合物 a2d 反应的离子方程式
(6)工业上冶炼g元素的单质的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
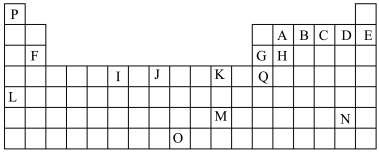
请回答下列问题:
(1)I的最高化合价为___________ , 元素的外围电子排布式为
元素的外围电子排布式为___________ 。
(2)下列对比正确的是___________ 。
a.原子半径
b.第一电离能
c.电负性
d.最高价氧化物的水化物酸性
(3)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是___________ 。
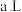 位于元素周期表中第
位于元素周期表中第 周期I
周期I 族,属于
族,属于 区元素
区元素
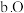 位于元素周期表中第
位于元素周期表中第 周期VIII
周期VIII 族,属于
族,属于 区元素
区元素
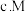 的外围电子排布式为
的外围电子排布式为 ,属于
,属于 区元素
区元素
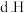 所在族的外围电子排布式为
所在族的外围电子排布式为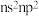 ,属于
,属于 区元素
区元素
(4)元素 和
和 的气态氢化物热稳定性较强的是
的气态氢化物热稳定性较强的是___________ (填化学式)。

请回答下列问题:
(1)I的最高化合价为
 元素的外围电子排布式为
元素的外围电子排布式为(2)下列对比正确的是
a.原子半径

b.第一电离能

c.电负性

d.最高价氧化物的水化物酸性

(3)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是
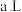 位于元素周期表中第
位于元素周期表中第 周期I
周期I 族,属于
族,属于 区元素
区元素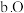 位于元素周期表中第
位于元素周期表中第 周期VIII
周期VIII 族,属于
族,属于 区元素
区元素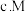 的外围电子排布式为
的外围电子排布式为 ,属于
,属于 区元素
区元素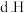 所在族的外围电子排布式为
所在族的外围电子排布式为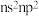 ,属于
,属于 区元素
区元素(4)元素
 和
和 的气态氢化物热稳定性较强的是
的气态氢化物热稳定性较强的是
您最近一年使用:0次
【推荐1】下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,第一电离能最大的是_______ ,电负性最小的金属元素是_____ 。
(2)①、③、⑤三种元素最高价氧化物对应的水化物中,碱性最强的是__________ 。
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是_____________ 。
(4)①和⑨的最高价氧化物对应水化物的化学式分别为_________ 、____________
(5)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为______________________
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的过程:______________________________________
(7)⑨元素的价电子的轨道表示式为________________________________ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 第2周期 | ⑥ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 第4周期 | ② | ④ | ⑨ |
(2)①、③、⑤三种元素最高价氧化物对应的水化物中,碱性最强的是
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是
(4)①和⑨的最高价氧化物对应水化物的化学式分别为
(5)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的过程:
(7)⑨元素的价电子的轨道表示式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:

(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式______ 。
(2)用电子式表示⑥和⑨形成化合物的过程:______ 。
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为______ (用化学式表示)。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式______ 。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为______ (用离子符号表示)。

(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式
(2)用电子式表示⑥和⑨形成化合物的过程:
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式
(5)⑤、⑥、⑩的离子半径由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,且XY2为常见元素形成的离子化合物,则X、Y在元素周期表中的位置分别为______ 、_________ ,用电子式表示该化合物形成过程_____________ 。
(2)现有a~g 7种短周期元素,它们在周期表中的位置如下,请据此回答下列问题:
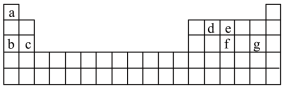
①元素的原子间反应最容易形成离子键的是____ 。
A.c和f B.b和g C.d和g D.b和e
②d与g元素形成的分子中所有原子_____ (填“是”或“不是”)都满足最外层为8电子结构。
(3)X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17。请填空:
①Y、Z和W三种元素是否位于同一周期(填“是”或“否”):________ ,理由是________
②X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1。写出该化合物的化学式_______ 。
(2)现有a~g 7种短周期元素,它们在周期表中的位置如下,请据此回答下列问题:

①元素的原子间反应最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和e
②d与g元素形成的分子中所有原子
(3)X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17。请填空:
①Y、Z和W三种元素是否位于同一周期(填“是”或“否”):
②X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1。写出该化合物的化学式
您最近一年使用:0次



