(1)依据氧化还原反应2Ag+(ag)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
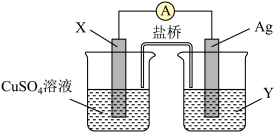
电极X的材料是_______ ;电解质溶液Y是_________________ ;银电极为电池的________ 极,发生的电极反应为______________________ ;X电极上发生的电极反应为______________________ 。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为氢氧燃料电池,
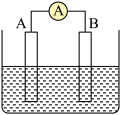
写出A电极反应式:___________________________________ ;写出B电极反应式:_______________________ ;写出该电池反应:__________ 。

电极X的材料是
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为氢氧燃料电池,

写出A电极反应式:
更新时间:2019-06-12 15:52:56
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用导线将锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,此电池的负极是_____ ,正极的电极反应式是___________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现代社会的一切活动都离不开能量,化学反应在发生物质变化的同时伴随能量的变化。
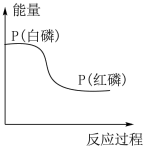
(1)一定条件下,白磷转化为红磷的能量关系如图所示。在该条件下,下列说法正确的是___________。
(2)下列说法中,正确的是___________。
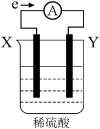
(3)某装置如图所示,下列说法正确的是___________。
(4)NOCl常用于有机合成,合成原理如图所示,反应过程中的能量变化如图所示,写出合成NOCl的热化学方程式___________ 。曲线从a变为b改变的条件是___________ 。

(1)一定条件下,白磷转化为红磷的能量关系如图所示。在该条件下,下列说法正确的是___________。

| A.白磷比红磷稳定 | B.等质量的红磷与白磷完全燃烧释放的热量相同 |
| C.红磷与白磷互为同位素 | D.红磷转化为白磷是吸热反应 |
| A.发生化学反应时,化学能一定转化为热能 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.化学反应能量的变化与反应物的物质的量大小无关 |
| D.当生成物总能量高于反应物总能量时,反应放热 |

| A.外电路的电流方向为:Y→X | B.X极上发生的是还原反应 |
| C.溶液中氢离子向X极移动 | D.若两电极都是金属,则活动性顺序:X>Y |

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
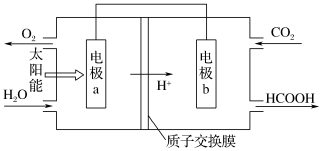
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作___________ 极,发生的电极反应式为___________ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为___________ 极,Y电极反应式为___________ 。
②Y极生成1 mol Cl2时,___________ mol Li+移向X极。
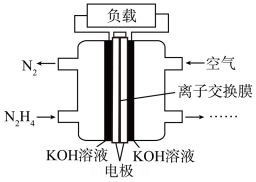
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH溶液作电解质溶液。负极反应式为___________ ,正极反应式为___________ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为
②Y极生成1 mol Cl2时,
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH溶液作电解质溶液。负极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯铝电池是一种新型的燃料电池,电解质溶液是KOH溶液,试回答下列问题:
(1)通入氯气的电极是___________ 极(填“正”或“负”),电极反应式为:___________ 。
(2)加入铝的电极是___________ 极(填“正”或“负”),电极反应式为:___________ 。
(3)电子从___________ 极流向___________ 极(填“Al”或“Cl2”)。
(1)通入氯气的电极是
(2)加入铝的电极是
(3)电子从
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】据报道,最近摩托罗拉(MOTOROLA)公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月充电一次。假定放电过程中,甲醇完全反应产生的CO2被充分吸收生成CO32-
(1)该电池反应的负极反应式为____________________________ ;
(2)甲醇在________ 极发生反应(填“正”或“负”),电池在放电过程中溶液的pH将_______ (填“降低、上升或不变”);
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一电极通入汽油蒸气。其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2(Zr:锆)固体,它在高温下能传导O2-离子(其中氧化反应发生完全),以甲烷(CH4)代表汽油。
①电池的负极反应式为__________________________________________ 。
②放电时固体电解质里的O2-离子的移动方向是向_________ 极移动(填“正”或“负”)。
(1)该电池反应的负极反应式为
(2)甲醇在
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一电极通入汽油蒸气。其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2(Zr:锆)固体,它在高温下能传导O2-离子(其中氧化反应发生完全),以甲烷(CH4)代表汽油。
①电池的负极反应式为
②放电时固体电解质里的O2-离子的移动方向是向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】控制适合的条件,将反应2Fe3++2I-  2Fe2++I2设计成如图所示的原电池。回答下列问题:
2Fe2++I2设计成如图所示的原电池。回答下列问题:
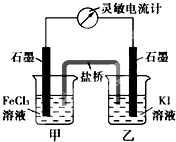
(1)反应开始时,乙中石墨电极上发生________ 反应(填“氧化”或“还原”),盐桥中的阴离子移向________ (填“甲”或“乙”)烧杯。
(2)反应开始时,甲中石墨电极上的电极反应式为________ 。
(3)反应达到化学平衡状态时,电流计指针________ 偏转。(填“是”或“否”)。
(4)反应达到平衡状态后,在甲中溶入FeCl2固体,乙中石墨电极为________ 极。
 2Fe2++I2设计成如图所示的原电池。回答下列问题:
2Fe2++I2设计成如图所示的原电池。回答下列问题:
(1)反应开始时,乙中石墨电极上发生
(2)反应开始时,甲中石墨电极上的电极反应式为
(3)反应达到化学平衡状态时,电流计指针
(4)反应达到平衡状态后,在甲中溶入FeCl2固体,乙中石墨电极为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是________ (填字母)。
A.C(s)+H2O(g)===CO(g)+H2(g) ΔH > 0
B.2H2(g)+O2(g)===2H2O(l) ΔH < 0
C.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH < 0
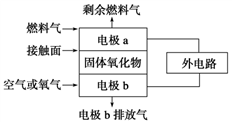
(2)固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动。
①正极:________ (填“电极a”或“电极b”)。 O2-移向________ 极(填“正”或“负”)。
②当燃料气为C2H4时,其正极、负极反应式分别为
正极:______________________ ;负极:____________________ 。
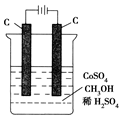
(3)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则除去甲醇的离子方程式为____________________ 。
A.C(s)+H2O(g)===CO(g)+H2(g) ΔH > 0
B.2H2(g)+O2(g)===2H2O(l) ΔH < 0
C.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH < 0
(2)固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动。
①正极:

②当燃料气为C2H4时,其正极、负极反应式分别为
正极:
(3)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则除去甲醇的离子方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图为原电池装置示意图:
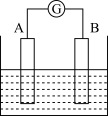
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,做负极的分别是__________ 。
a.铝片 铜片 b.铜片 铝片 c.铝片 铝片 d.铜片 铜片
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:______________________________ ;该电池工作时,A电极的质量将__________ (填“增加”、“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为__________ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池为甲烷燃料电池,写出A电极反应式:______________________________ 。该电池工作一段时间后,溶液的碱性将__________ (填“增强”、“减弱”或“不变”)。

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,做负极的分别是
a.铝片 铜片 b.铜片 铝片 c.铝片 铝片 d.铜片 铜片
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池为甲烷燃料电池,写出A电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。试回答下列问题:
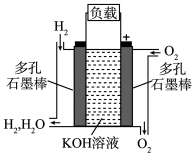
(1)氢气进入的这极为___ 极;
(2)写出氢氧燃料电池工作时的正极反应式:___ ;
(3)该氢氧燃料电池每转移0.1mol电子,消耗标准状态下___ L氧气;
(4)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___ 。

(1)氢气进入的这极为
(2)写出氢氧燃料电池工作时的正极反应式:
(3)该氢氧燃料电池每转移0.1mol电子,消耗标准状态下
(4)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为
您最近一年使用:0次



