某温度时,反应X(g) 4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法
4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法不正确 的是

 4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法
4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法
| A.2 min内,X的平均反应速率为0.25 mol·L-1·min-1 |
| B.第t min时,该反应达到平衡状态 |
| C.第5 min后,X的生成速率与Z的生成速率相等且保持不变 |
| D.5 min内,反应放出的热量为1.6Q kJ |
更新时间:2019-06-29 14:20:24
|
【知识点】 结合反应热图像与化学平衡的综合考查解读
相似题推荐
单选题
|
较难
(0.4)
【推荐1】已知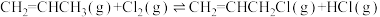 ,该反应的
,该反应的
 ,
, ,
, 、
、 分别为正、逆反应速率常数。在一定压强下,按
分别为正、逆反应速率常数。在一定压强下,按 向密闭容器中投料,平衡时
向密闭容器中投料,平衡时 的体积分数
的体积分数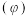 、
、 与温度T、w的关系如图所示。下列说法中正确的是
与温度T、w的关系如图所示。下列说法中正确的是
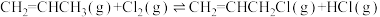 ,该反应的
,该反应的
 ,
, ,
, 、
、 分别为正、逆反应速率常数。在一定压强下,按
分别为正、逆反应速率常数。在一定压强下,按 向密闭容器中投料,平衡时
向密闭容器中投料,平衡时 的体积分数
的体积分数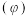 、
、 与温度T、w的关系如图所示。下列说法中正确的是
与温度T、w的关系如图所示。下列说法中正确的是
A. ,曲线n表示 ,曲线n表示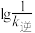 随温度的变化 随温度的变化 |
B.在 、 、 , , 时, 时, |
C.一定温度下,该反应的 随催化剂的不同而发生改变 随催化剂的不同而发生改变 |
D.相同温度下,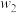 平衡体系中 平衡体系中 大于 大于 的 的 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知工业合成氨的方程式:3H2(g)+N2(g)  2NH3(g),该反应在一定条件下进行时的热效应如图1,所示下列说法正确的是
2NH3(g),该反应在一定条件下进行时的热效应如图1,所示下列说法正确的是


 2NH3(g),该反应在一定条件下进行时的热效应如图1,所示下列说法正确的是
2NH3(g),该反应在一定条件下进行时的热效应如图1,所示下列说法正确的是

| A.由图1可知,该逆反应的活化能为(E+ΔH) kJ/mol |
| B.图2中L、X表示的物理量是温度或压强,依据信息可判断L1>L2 |
| C.图2中a、b、c三点中υ正最大的点是b |
| D.图2中a、b、c点平衡常数的关系为:Ka=Kc<Kb |
您最近一年使用:0次




