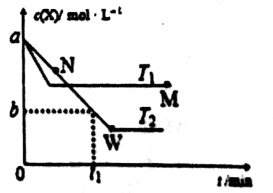
已知图一表示的是可逆反应O2(g)+2SO2(g)⇌2SO3(g) ∆H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)⇌N2O4(g) ∆H<0的浓度(c)随时间t 的变化情况。下列说法中正确的是


| A.若图一t2时改变的条件是增大压强,则反应∆H的增大 |
| B.图一t2时改变的条件可能是升高了温度或增大了压强 |
| C.图二t1时改变的条件可能是增大了压强 |
| D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
2019·安徽·一模 查看更多[1]
(已下线)安徽省江南十校2019届高三二次联考化学试卷
更新时间:2019-02-22 10:59:26
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应: 2A(气)+B(气) 2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0. 6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是
2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0. 6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是
 2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0. 6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是
2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0. 6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是| A.①③ | B.①④ | C.②③ | D.③④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】一定温度下,向2.0L的恒容密闭容器中充入1.6molCO、1.6molNO,发生反应2NO(g)+2CO(g) N2(g)+2CO2(g),经过一段时间后达平衡。反应进行到不同时间测得n(CO)如表所示:
N2(g)+2CO2(g),经过一段时间后达平衡。反应进行到不同时间测得n(CO)如表所示:
下列说法正确的是
 N2(g)+2CO2(g),经过一段时间后达平衡。反应进行到不同时间测得n(CO)如表所示:
N2(g)+2CO2(g),经过一段时间后达平衡。反应进行到不同时间测得n(CO)如表所示:| t/s | 0 | 5 | 10 | 15 | 20 |
| n(CO)/mol | 1.6 | 1.2 | 0.9 | 0.8 | 0.8 |
| A.该温度下,该反应的平衡常数K=1.25 |
| B.反应在前5s的平均速率为v(N2)=0.04mol·L-1·s-1 |
| C.保持其他条件不变,升高温度,达到新平衡时c(CO)=0.45mol·L⁻1,则反应的ΔH>0 |
| D.相同温度下,起始时向容器中充入1.6mol CO、1.6mol NO、0.8mol N2、1.6 molCO2,达到平衡前v正<v逆 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】为了探究反应速率的影响因素,某同学通过碳酸钙与稀盐酸的反应,绘制出收集到的 CO2体积与反应时间的关系图(0-t1、t1-t2、t2-t3的时间间隔相等)。下列说法正确的是

A.0-t1时间段,CO2的化学反应速率 v= mol/(L·min) mol/(L·min) |
| B.t1-t2与 0-t1比较,反应速率加快的原因可能是产生的 CO2气体增多 |
| C.t2-t4时间段,反应速率逐渐减慢的原因可能是盐酸浓度减小 |
| D.在 t4 后,收集到的气体的体积不再增加说明碳酸钙消耗完全 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图I所示;若保持其他条件不变,温度分别为Tl和T2时,B的体积百分含量与时间的关系如图Ⅱ所示。则下列结论正确的是
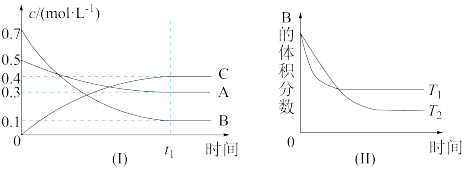

| A.在达平衡后,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B.在达平衡后,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.保持其他条件不变,若反应开始时A、B、C的浓度分别为0.4mol·L-1、0.5 mol·L-1和0.2 mol·L—1,则达到平衡后,C的浓度大于0.4 mol·L-1 |
| D.保持其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】温度为T°C,向体积不等的密闭容器中分别加入足量活性炭和lmolNO2,发生反应:2C(s)+2NO2(g)⇌N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示(V1<V2<V3)。下列说法正确的是
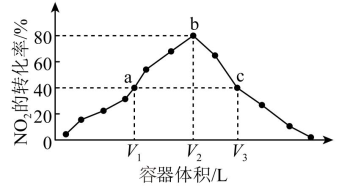

| A.图中a点所示条件下v(正)=v(逆) |
| B.T°C时,a、b两点时反应的平衡常数Ka<Kb |
| C.向b点体系中充入一定量NO2,达到新平衡时,NO2转化率将增大 |
| D.对c点容器加压,缩小容器体积,则此时v(逆)>v(正) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在某容积一定的密闭容器中,有下列可逆反应xA(g)+B(g)⇌2C(g),反应曲线(T表示温度,P表示压强,C% 表示C的体积分数)如图所示,试判断对图的说法中一定正确的是( )
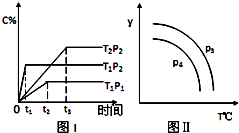

| A.该反应是吸热反应 |
| B.x=2 |
| C.P3<P4,y轴可表示混合气体的相对分子质量 |
| D.P3>P4,y轴可表示C物质在平衡体积中的百分含量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】如图图示与对应的叙述相符的是( )
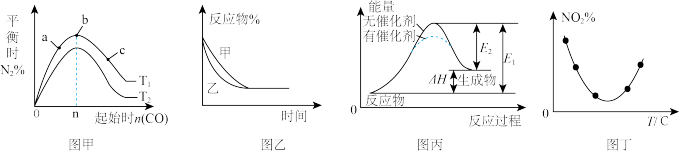

A.图甲表示反应:4CO(g)+2NO2(g) N2(g)+4CO2(g) H 0 ,在其他条件不变的情况下,改变起始物 CO 的物质的量对此反应平衡的影响,则有T1 T2 , K1 K2 N2(g)+4CO2(g) H 0 ,在其他条件不变的情况下,改变起始物 CO 的物质的量对此反应平衡的影响,则有T1 T2 , K1 K2 |
B.图乙表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C.图丙表示的反应是吸热反应,该图表明催化剂能改变化学反应的焓变 |
D.图丁表示等量 NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g)相同时间后测得 NO2含量的曲线,则该反应的H0 N2O4(g)相同时间后测得 NO2含量的曲线,则该反应的H0 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某温度时,反应X(g) 4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法
4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法不正确 的是

 4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法
4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法
| A.2 min内,X的平均反应速率为0.25 mol·L-1·min-1 |
| B.第t min时,该反应达到平衡状态 |
| C.第5 min后,X的生成速率与Z的生成速率相等且保持不变 |
| D.5 min内,反应放出的热量为1.6Q kJ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对于反应 在容积为10L的密闭容器中进行。起始时
在容积为10L的密闭容器中进行。起始时 和
和 均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法
均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法不正确 的是

 在容积为10L的密闭容器中进行。起始时
在容积为10L的密闭容器中进行。起始时 和
和 均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法
均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法
A.实验c条件下,从反应开始至达到平衡时 |
| B.实验a条件下,用浓度表示的平衡常数为100 |
C.该反应的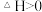 |
| D.比较实验a、c可判断升高温度反应速率加快 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】采用阴离子交换法合成了一系列不同 Zn 和 Pt 含量的PtSn-Mg(Zn)AlO催化剂用于乙烷脱氢反应[CH3CH3(g)⇌CH2 = CH2 (g)+H2(g) △H>0],实验结果表明,在水滑石载体中掺杂少量的 Zn 对乙烷脱氢反应有明显影响,如图所示为不同Zn含量PtSn催化剂的乙烷催化脱氢反应中,乙烷的转化率随时间的变化。下列说法不正确的是( )
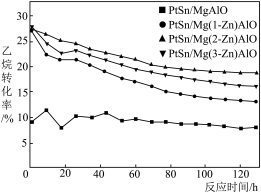

| A.由图可知,PtSn/Mg(2-Zn)AlO催化剂的催化反应活性最优 |
B.一定温度下,将nmol乙烷放入VL密闭容器中进行催化脱氢,维持容器体积不变,测得乙烷平衡转化率为a,则该温度下反应的平衡常数K= |
| C.升高温度,平衡逆向移动 |
| D.随着反应时间的延长,乙烷转化率逐渐稳定,催化活性保持在相对稳定的阶段 |
您最近一年使用:0次

 Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是