(1)典型物质的电子式
NH4Cl:__________ Na2O2:________ CO2:___________ -OH:__________
(2)某短周期元素含氧酸的化学式为HXO3,其气态氢化物的化学式为HX,则X元素在周期表中的位置为_______ 。
(3)石油的综合利用方法有四种,其中____ 的目的是提高轻质油的产量,_____ 主要是得到甲烷、乙烯、丙烯等化工原料,_______ 是从石油中获得苯、甲苯等化工原料。
(4)填写有机除杂试剂
C2H6(C2H4)__________
乙酸乙酯(乙酸或乙醇)_____
乙醇(水)____________
苯(溴)________________
(5)无机方程式书写
①海带提碘的氧化环节,使用稀硫酸酸化的双氧水氧化I-的离子方程式为_______
②海水提溴吸收塔(SO2的水溶液)中的反应离子方程式为__________
③以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
a.高温下,向金红石与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体__________
b.在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛_____
(6)有机方程式书写
①乙醇去氢催化氧化生成乙醛的化学方程式:_______
②对苯二甲酸与乙二醇在一定条件下发生缩聚反应生成涤纶的化学方程式:___
③苯的硝化反应____________
NH4Cl:
(2)某短周期元素含氧酸的化学式为HXO3,其气态氢化物的化学式为HX,则X元素在周期表中的位置为
(3)石油的综合利用方法有四种,其中
(4)填写有机除杂试剂
C2H6(C2H4)
乙酸乙酯(乙酸或乙醇)
乙醇(水)
苯(溴)
(5)无机方程式书写
①海带提碘的氧化环节,使用稀硫酸酸化的双氧水氧化I-的离子方程式为
②海水提溴吸收塔(SO2的水溶液)中的反应离子方程式为
③以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
a.高温下,向金红石与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体
b.在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛
(6)有机方程式书写
①乙醇去氢催化氧化生成乙醛的化学方程式:
②对苯二甲酸与乙二醇在一定条件下发生缩聚反应生成涤纶的化学方程式:
③苯的硝化反应
更新时间:2019-09-02 16:45:13
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
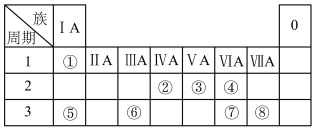
(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素⑦的原子结构示意图为_______ ,元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素④⑤组成原子个数比为1:1的化合物中含_______ (填“离子键”、“共价键”或“离子键和共价键”),将78g该化合物投入98g水中,所得溶液的质量分数为_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式),该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含 和
和 的分子的电子式分别是
的分子的电子式分别是_______ 、_______ 。

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素⑦的原子结构示意图为
(3)由元素④⑤组成原子个数比为1:1的化合物中含
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含
 和
和 的分子的电子式分别是
的分子的电子式分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是_______ ,其原子核外有_______ 个未成对电子,能量最高的电子所在的轨道呈_______ 形。B为周期表中第29号元素,B的电子排布式为_______ 。
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为: ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为_______ ;此反应中涉及物质中互为等电子体的是_______ ; 的结构式为
的结构式为_______ 。
(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:_______ 。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为:
 ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为 的结构式为
的结构式为(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:
您最近一年使用:0次
【推荐3】有机物的表示方法多种多样,下面是常用的有机物的表示方法:
①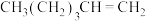 ②
②  ③
③ ④
④  ⑤
⑤  ⑥
⑥ ⑦
⑦  ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)属于结构式的有___________ ;属于键线式的有___________ ;属于空间填充模型的有___________ ;
(2)写出⑨的分子式:___________ 。
(3)写出⑩中官能团的电子式:___________ 、___________ 。
(4)②的分子式为___________ ,最简式为___________ 。
①
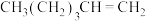 ②
②  ③
③ ④
④  ⑤
⑤  ⑥
⑥ ⑦
⑦  ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)属于结构式的有
(2)写出⑨的分子式:
(3)写出⑩中官能团的电子式:
(4)②的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将6.1g某有机物A(仅含C、H、O元素)样品置于燃烧器中充分燃烧,将燃烧产物依次通过浓硫酸和碱石灰,待燃烧产物被完全吸收后测得前者增重2.7g,后者增重15.4g,请回答:
(1)该有机物的实验式_______ 。
(2)若该有机物A的相对分子量为122,属于芳香族化合物,其核磁共振氢谱上有4组峰,且峰面积之比为1∶2∶2∶1,能与金属钠反应产生氢气,也能和新制 加热后产生砖红色沉淀,该有机物的结构简式是
加热后产生砖红色沉淀,该有机物的结构简式是_______ ,请写出该有机物与足量新制 加热后反应的化学方程式
加热后反应的化学方程式_______ 。
(3)有机物A的某种同分异构体B,可用作食品防腐剂,能和碳酸氢钠溶液反应产生气泡。B是无色结晶,熔点122℃,沸点249℃,在水中溶解度如下图:
B中混有KCl固体和泥沙,若要提纯B,在下列选项中选取合适的操作并正确排序_______ 。
①热水溶解 ②趁热过滤 ③过滤 ④冷却结晶 ⑤蒸发结晶 ⑥蒸馏 ⑦洗涤 ⑧干燥
(1)该有机物的实验式
(2)若该有机物A的相对分子量为122,属于芳香族化合物,其核磁共振氢谱上有4组峰,且峰面积之比为1∶2∶2∶1,能与金属钠反应产生氢气,也能和新制
 加热后产生砖红色沉淀,该有机物的结构简式是
加热后产生砖红色沉淀,该有机物的结构简式是 加热后反应的化学方程式
加热后反应的化学方程式(3)有机物A的某种同分异构体B,可用作食品防腐剂,能和碳酸氢钠溶液反应产生气泡。B是无色结晶,熔点122℃,沸点249℃,在水中溶解度如下图:
| 温度/℃ | 25 | 50 | 75 |
| 溶解度/g | 0.34 | 0.85 | 2.2 |
B中混有KCl固体和泥沙,若要提纯B,在下列选项中选取合适的操作并正确排序
①热水溶解 ②趁热过滤 ③过滤 ④冷却结晶 ⑤蒸发结晶 ⑥蒸馏 ⑦洗涤 ⑧干燥
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化合物C是某合成路线的中间体,可通过下列方法合成:
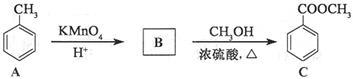
回答下列问题:
(1)在催化剂作用下,A与氢气反应的化学方程式为_____________ ,反应类型为______ 。
(2)B的结构简式为_________ ,所得B的粗产品通常用________ 的方法提纯。
(3)在C的制备中,浓硫酸的作用是_________ 。

回答下列问题:
(1)在催化剂作用下,A与氢气反应的化学方程式为
(2)B的结构简式为
(3)在C的制备中,浓硫酸的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据题意,完成下列有机试题的填空:
(1)提纯固体有机物常采用___________ 法;提纯液体有机物常用的方法是___________ 。
(2)有机物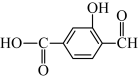 具有三种官能团:
具有三种官能团:___________ 、 ___________ 和___________ (填官能团的名称)。
(3)化合物M分子式是C2H4Br 2, M的核磁共振氢谱图如图所示,则M的结构简式为___________ ,

(4)键线式 表示的有机物的分子式为
表示的有机物的分子式为___________ 。
(5)根据下表中烃的分子式排列规律,判断空格中烃的同分异构体的数目是___________ 。
(6)将甲醛(HCHO)水溶液与氨水混合蒸发可制得乌洛托品(如图所示)。若原料完全反应生成乌洛托品和水,则甲醛与氨的物质的量之比应为___________ 。

(1)提纯固体有机物常采用
(2)有机物
 具有三种官能团:
具有三种官能团:(3)化合物M分子式是C2H4Br 2, M的核磁共振氢谱图如图所示,则M的结构简式为

(4)键线式
 表示的有机物的分子式为
表示的有机物的分子式为(5)根据下表中烃的分子式排列规律,判断空格中烃的同分异构体的数目是
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国石油工业一般采用恒电流库伦分析法测定汽油的溴指数。溴指数是指每100克试样消耗溴的毫克数,它反映了试样中C=C的数目。测定时将V(毫升)试样加入库伦分析池中,利用电解产生的溴与不饱和烃反应。当反应完全后,过量溴在指示电极上还原而指示终点。支持电解质为LiBr,溶剂系统仅含5%水,其余为甲醇、苯与醋酸。设d为汽油试样密度,Q为终点时库伦计指示的溴化反应消耗的电量(库伦)。
(1)导出溴指数与V、d和Q的关系式(注:关系式中只允许有一个具体的数值)_______ 。
(2)若在溶剂体系中增加苯的比例,说明其优缺点_______ 。
(1)导出溴指数与V、d和Q的关系式(注:关系式中只允许有一个具体的数值)
(2)若在溶剂体系中增加苯的比例,说明其优缺点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】用CO和H2在443~473K温度下,并用钴作催化剂时,可以反应生成n=5~8的烷烃,这是人工合成汽油的方法之一。
(1)写出用CnH2n+2表示人工合成汽油的化学方程式___________ 。
(2)如果向密闭的合成塔里通入恰好能完全反应的CO和H2,当完全反应后,合成塔内温度不变,而塔内气体压强降低到原来的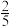 。计算说明这时有无汽油生成
。计算说明这时有无汽油生成_____ 。
(3)要达到上述合成汽油的要求,CO和H2的体积比的取值范围是______________ 。
(1)写出用CnH2n+2表示人工合成汽油的化学方程式
(2)如果向密闭的合成塔里通入恰好能完全反应的CO和H2,当完全反应后,合成塔内温度不变,而塔内气体压强降低到原来的
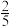 。计算说明这时有无汽油生成
。计算说明这时有无汽油生成(3)要达到上述合成汽油的要求,CO和H2的体积比的取值范围是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】汽车尾气污染已成为一大公害。汽车内燃机中,汽油气化后与空气按一定比例混合进入汽缸,引擎用电火花引燃。汽油燃烧使气缸内温度迅速升高,气体体积急剧膨胀,产生压力推动活塞。燃烧时产生的有害气体通过尾气排出,从而污染大气。为简化讨论,假设汽油的成分全部为辛烷,并假设空气中氧气的体积分数为20%,其余为氮气。请回答下列问题:
(1)设辛烷气体与空气的体积比为a,要使辛烷完全燃烧,则a的最大值为_____________ 。
(2)若辛烷与空气的体积比大于a的最大值时,污染大气的有害气体相对增多的是______________________ 。
(3)若辛烷与空气的体积比小于a的最大值时,则尾气中所含污染大气的有害气体增多的是_____________ ,产生此气体的化学方程式是____________________________ 。
(4)当辛烷与空气的体积比小于a的最大值时,从能量角度来分析,有利也有弊,如其有利的因素是氧气过量,有利于汽油完全燃烧,提高能源利用率。请你举出一个不利的因素:_________________________________________________________________ 。
(1)设辛烷气体与空气的体积比为a,要使辛烷完全燃烧,则a的最大值为
(2)若辛烷与空气的体积比大于a的最大值时,污染大气的有害气体相对增多的是
(3)若辛烷与空气的体积比小于a的最大值时,则尾气中所含污染大气的有害气体增多的是
(4)当辛烷与空气的体积比小于a的最大值时,从能量角度来分析,有利也有弊,如其有利的因素是氧气过量,有利于汽油完全燃烧,提高能源利用率。请你举出一个不利的因素:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知:5 +2
+2 +2H+=I2+5
+2H+=I2+5 +H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、
+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、 中的一种或两种。请补充完整检验含碘废水中是否含有I-、
中的一种或两种。请补充完整检验含碘废水中是否含有I-、 的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
①取适量含碘废水用CCl4多次萃取、分液,直到水层检验不出碘单质存在;
②______________________ ;
③另从水层取少量溶液,加入2~3滴淀粉溶液,滴加____________ (填试剂和现象)。说明废水中含有 ,否则说明废水中不含
,否则说明废水中不含 。
。
 +2
+2 +2H+=I2+5
+2H+=I2+5 +H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、
+H2O。某含碘废水(pH约为8)中一定存在I2,可能存在I-、 中的一种或两种。请补充完整检验含碘废水中是否含有I-、
中的一种或两种。请补充完整检验含碘废水中是否含有I-、 的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)
的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液) ①取适量含碘废水用CCl4多次萃取、分液,直到水层检验不出碘单质存在;
②
③另从水层取少量溶液,加入2~3滴淀粉溶液,滴加
 ,否则说明废水中不含
,否则说明废水中不含 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列说法或操作正确的是_______ 。
①用酒精萃取碘水中的碘,下层液体由分液漏斗下口放出,上层液体由上口倒出
②使用容量瓶之前必须进行检漏操作
③海带中碘元素的分离及检验时,需要向海带灰的浸取液中加入少量稀硫酸和过氧化氢溶液
④将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体
⑤用加热法可以分离高锰酸钾和碘单质的混合物,因为碘单质受热易升华
⑥用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液中的水全部加热蒸干
①用酒精萃取碘水中的碘,下层液体由分液漏斗下口放出,上层液体由上口倒出
②使用容量瓶之前必须进行检漏操作
③海带中碘元素的分离及检验时,需要向海带灰的浸取液中加入少量稀硫酸和过氧化氢溶液
④将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体
⑤用加热法可以分离高锰酸钾和碘单质的混合物,因为碘单质受热易升华
⑥用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液中的水全部加热蒸干
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下流程图回答下列问题:

(1)海水淡化的方法有_______ (填一种)。
(2)过程①为了除去粗盐中的可溶性杂质 、
、 ,可将粗盐溶于水,然后进行下列五项操作:a.过滤,b.加过量NaOH溶液,c.加适量盐酸,d.加过量
,可将粗盐溶于水,然后进行下列五项操作:a.过滤,b.加过量NaOH溶液,c.加适量盐酸,d.加过量 溶液,e.加过量
溶液,e.加过量 溶液,正确的操作顺序是
溶液,正确的操作顺序是_______ (填字母)。
A.adbec B.dabec C.bedac D.ebdac
过程②能否一步实现转化?_______ (填“能”或“否”), 与盐酸反应可以得到
与盐酸反应可以得到 溶液,则该反应的离子方程式为
溶液,则该反应的离子方程式为_______ 。
(3)过程④反应的离子方程式为_______ 。
(4)若用 萃取溴水中的
萃取溴水中的 ,分液时
,分液时 层应从分液漏斗的
层应从分液漏斗的_______ 放出。

(1)海水淡化的方法有
(2)过程①为了除去粗盐中的可溶性杂质
 、
、 ,可将粗盐溶于水,然后进行下列五项操作:a.过滤,b.加过量NaOH溶液,c.加适量盐酸,d.加过量
,可将粗盐溶于水,然后进行下列五项操作:a.过滤,b.加过量NaOH溶液,c.加适量盐酸,d.加过量 溶液,e.加过量
溶液,e.加过量 溶液,正确的操作顺序是
溶液,正确的操作顺序是A.adbec B.dabec C.bedac D.ebdac
过程②能否一步实现转化?
 与盐酸反应可以得到
与盐酸反应可以得到 溶液,则该反应的离子方程式为
溶液,则该反应的离子方程式为(3)过程④反应的离子方程式为
(4)若用
 萃取溴水中的
萃取溴水中的 ,分液时
,分液时 层应从分液漏斗的
层应从分液漏斗的
您最近一年使用:0次



