汽车尾气污染已成为一大公害。汽车内燃机中,汽油气化后与空气按一定比例混合进入汽缸,引擎用电火花引燃。汽油燃烧使气缸内温度迅速升高,气体体积急剧膨胀,产生压力推动活塞。燃烧时产生的有害气体通过尾气排出,从而污染大气。为简化讨论,假设汽油的成分全部为辛烷,并假设空气中氧气的体积分数为20%,其余为氮气。请回答下列问题:
(1)设辛烷气体与空气的体积比为a,要使辛烷完全燃烧,则a的最大值为_____________ 。
(2)若辛烷与空气的体积比大于a的最大值时,污染大气的有害气体相对增多的是______________________ 。
(3)若辛烷与空气的体积比小于a的最大值时,则尾气中所含污染大气的有害气体增多的是_____________ ,产生此气体的化学方程式是____________________________ 。
(4)当辛烷与空气的体积比小于a的最大值时,从能量角度来分析,有利也有弊,如其有利的因素是氧气过量,有利于汽油完全燃烧,提高能源利用率。请你举出一个不利的因素:_________________________________________________________________ 。
(1)设辛烷气体与空气的体积比为a,要使辛烷完全燃烧,则a的最大值为
(2)若辛烷与空气的体积比大于a的最大值时,污染大气的有害气体相对增多的是
(3)若辛烷与空气的体积比小于a的最大值时,则尾气中所含污染大气的有害气体增多的是
(4)当辛烷与空气的体积比小于a的最大值时,从能量角度来分析,有利也有弊,如其有利的因素是氧气过量,有利于汽油完全燃烧,提高能源利用率。请你举出一个不利的因素:
更新时间:2017-07-04 17:47:51
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
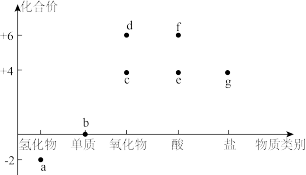
【推荐1】利用元素化合价和物质类别推测物质的性质是化学研究的重要手段。如图是硫元素常见化合价与部分物质类别的对应关系。
(1)按物质性质分类,c、d均属于____ 氧化物。据此类物质的性质列举一种消除c对空气污染的方法____ 。
(2)a中硫元素处于最低化合价,其有____ 性。a溶液久置于空气中会生成b。使溶液变浑浊。写出发生反应的化学方程式____ 。
(3)从化合价的角度看c、e、g既有氧化性又有还原性,写出一个c表现氧化性的化学方程式____ ;用离子方程式表示g与绿色氧化剂的反应____ 。
(4)c→e→f是硫酸型酸雨的形成途径之一。某地收集的雨水样品在不同时间测得pH如表所示,请分析该雨水样品随时间变化酸性逐渐增强的原因____ 。
(1)按物质性质分类,c、d均属于
(2)a中硫元素处于最低化合价,其有
(3)从化合价的角度看c、e、g既有氧化性又有还原性,写出一个c表现氧化性的化学方程式
(4)c→e→f是硫酸型酸雨的形成途径之一。某地收集的雨水样品在不同时间测得pH如表所示,请分析该雨水样品随时间变化酸性逐渐增强的原因
| 时间/h | 0 | 2 | 4 | 6 | 8 | 10 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】十九大报告中指出“持续实施大气污染防治行动,打赢蓝天保卫战”。汽车尾气中的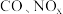 以及燃煤废气中的
以及燃煤废气中的 都是大气污染物,研究它们的性质对环境治理具有重要意义。
都是大气污染物,研究它们的性质对环境治理具有重要意义。
(1)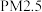 是指大气中直径小于或等于
是指大气中直径小于或等于 的颗粒物。下列说法不正确的是
的颗粒物。下列说法不正确的是_________ (填字母)。
a.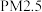 主要来源于火力发电、工业生产、汽车尾气排放等过程
主要来源于火力发电、工业生产、汽车尾气排放等过程
b.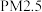 颗粒小,所以对人体无害
颗粒小,所以对人体无害
c.直径介于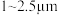 的颗粒物分散到空气中可形成胶体
的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少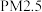 的污染
的污染
(2)直接排放含 的烟气会形成酸雨,危害环境。用化学方程式表示
的烟气会形成酸雨,危害环境。用化学方程式表示 形成硫酸型酸雨的过程
形成硫酸型酸雨的过程_________ (只写第一步)。
(3)洗涤含 的烟气,下列物质不能作为洗涤剂的是
的烟气,下列物质不能作为洗涤剂的是_________ (填字母)。
a. b.
b. c.
c.
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:
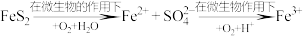
①该技术第一步反应的离子方程式为_________ 。
②处理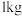 含
含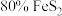 的黄铁矿,第二步消耗
的黄铁矿,第二步消耗 (标准状况下)的体积为
(标准状况下)的体积为_________ L(精确到0.01)。
(5)治理汽车尾气的 (
( 储存还原)技术均可有效降低柴油发动机工作过程中排放的
储存还原)技术均可有效降低柴油发动机工作过程中排放的 。柴油发动机工作时在稀燃(
。柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原,原理如下:
的储存和还原,原理如下:
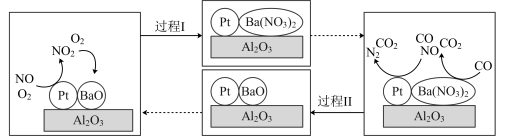
① 吸收
吸收 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为_________ 。
②若柴油中硫含量较高,在稀燃过程中, 吸收氮氧化物的能力会下降至很低水平,结合化学方程式解释其原因
吸收氮氧化物的能力会下降至很低水平,结合化学方程式解释其原因_________ 。
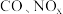 以及燃煤废气中的
以及燃煤废气中的 都是大气污染物,研究它们的性质对环境治理具有重要意义。
都是大气污染物,研究它们的性质对环境治理具有重要意义。(1)
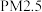 是指大气中直径小于或等于
是指大气中直径小于或等于 的颗粒物。下列说法不正确的是
的颗粒物。下列说法不正确的是a.
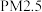 主要来源于火力发电、工业生产、汽车尾气排放等过程
主要来源于火力发电、工业生产、汽车尾气排放等过程b.
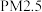 颗粒小,所以对人体无害
颗粒小,所以对人体无害c.直径介于
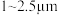 的颗粒物分散到空气中可形成胶体
的颗粒物分散到空气中可形成胶体d.推广使用电动汽车,可以减少
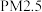 的污染
的污染(2)直接排放含
 的烟气会形成酸雨,危害环境。用化学方程式表示
的烟气会形成酸雨,危害环境。用化学方程式表示 形成硫酸型酸雨的过程
形成硫酸型酸雨的过程(3)洗涤含
 的烟气,下列物质不能作为洗涤剂的是
的烟气,下列物质不能作为洗涤剂的是a.
 b.
b. c.
c.
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:
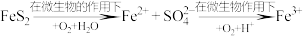
①该技术第一步反应的离子方程式为
②处理
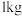 含
含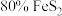 的黄铁矿,第二步消耗
的黄铁矿,第二步消耗 (标准状况下)的体积为
(标准状况下)的体积为(5)治理汽车尾气的
 (
( 储存还原)技术均可有效降低柴油发动机工作过程中排放的
储存还原)技术均可有效降低柴油发动机工作过程中排放的 。柴油发动机工作时在稀燃(
。柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原,原理如下:
的储存和还原,原理如下:
①
 吸收
吸收 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为②若柴油中硫含量较高,在稀燃过程中,
 吸收氮氧化物的能力会下降至很低水平,结合化学方程式解释其原因
吸收氮氧化物的能力会下降至很低水平,结合化学方程式解释其原因
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】硫有多种化合物,如H2S、COS(羰基硫)、SO2等,它们对环境均有一定的影响。
(1)H2S经K2CO3溶液吸收后,生成两种酸式盐 。其中任意一种酸式盐 的化学式是_______ 。
(2)COS(羰基硫)燃烧时有SO2生成,其原理为:2COS+3O2 2CO2+2SO2。若转移3.612×1024个电子,则参加反应COS(羰基硫)的物质的量是
2CO2+2SO2。若转移3.612×1024个电子,则参加反应COS(羰基硫)的物质的量是_______ mol。
(3)电厂排出的烟气中含有CO、SO2等。CO在催化剂存在时可与SO2反应,转化为一种固体和一种无害气体。该反应的化学方程式是_______ 。
(4)石灰石或生石灰作为脱硫剂,可有效吸收废气中的SO2,减少酸雨的产生。
①若在煤炭中加入生石灰可减少燃烧时SO2的排放量,首先生成CaSO3,该反应的化学方程式是_______ 。
②你认为减少酸雨产生的途径可采取的措施是_______ (填序号)。
a.避免直接用高硫煤作燃料 b.把工厂的烟囱造高
c.燃料脱硫 d.开发新能源
(1)H2S经K2CO3溶液吸收后,生成两种
(2)COS(羰基硫)燃烧时有SO2生成,其原理为:2COS+3O2
 2CO2+2SO2。若转移3.612×1024个电子,则参加反应COS(羰基硫)的物质的量是
2CO2+2SO2。若转移3.612×1024个电子,则参加反应COS(羰基硫)的物质的量是(3)电厂排出的烟气中含有CO、SO2等。CO在催化剂存在时可与SO2反应,转化为一种固体和一种无害气体。该反应的化学方程式是
(4)石灰石或生石灰作为脱硫剂,可有效吸收废气中的SO2,减少酸雨的产生。
①若在煤炭中加入生石灰可减少燃烧时SO2的排放量,首先生成CaSO3,该反应的化学方程式是
②你认为减少酸雨产生的途径可采取的措施是
a.避免直接用高硫煤作燃料 b.把工厂的烟囱造高
c.燃料脱硫 d.开发新能源
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2008年5月17日新疆电视台(午间新闻)报道:我国新增阿勒泰大气背景监测点。这标志着气候条件独特、空气质量优良的新疆阿勒泰市已成为我国第8个国家大气背景监测点。监测点安装的监测设备可监测日常二氧化硫、二氧化氮、一氧化氮等污染物。NO分子因污染空气而臭名昭著,近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。请回答下列问题:
(1)NO对环境的危害在于________ (填编号)。
A.破坏臭氧层
B.高温下能使一些金属氧化
C.造成酸雨
D.与人体血红蛋白结合
(2)在含Cu+的酶的活化中心,亚硝酸根离子(NO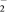 )可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式:
)可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式:_________________________________________ 。
(3)“绿色奥运”是2008年北京奥运会的主题之一,为迎接奥运,减少空气污染,北京为汽车加装了“三效催化净化器”,可将尾气中的一氧化碳和一氧化氮转化为参与大气循环的无毒混合气体,该气体是( )
A.二氧化碳和氮气 B.二氧化碳和二氧化氮
C.二氧化碳和氧气 D.二氧化碳和氢气
(4)氟利昂(如CCl2F2)可在光的作用下分解,产生氯原子,氯原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3)。有关反应如下:
O3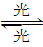 O2+O Cl+O3=ClO+O2 ClO+O=Cl+O2 总反应:2O3===3O2
O2+O Cl+O3=ClO+O2 ClO+O=Cl+O2 总反应:2O3===3O2
在上述臭氧变成氧气的过程中,Cl是__________________ 。
(1)NO对环境的危害在于
A.破坏臭氧层
B.高温下能使一些金属氧化
C.造成酸雨
D.与人体血红蛋白结合
(2)在含Cu+的酶的活化中心,亚硝酸根离子(NO
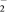 )可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式:
)可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式:(3)“绿色奥运”是2008年北京奥运会的主题之一,为迎接奥运,减少空气污染,北京为汽车加装了“三效催化净化器”,可将尾气中的一氧化碳和一氧化氮转化为参与大气循环的无毒混合气体,该气体是
A.二氧化碳和氮气 B.二氧化碳和二氧化氮
C.二氧化碳和氧气 D.二氧化碳和氢气
(4)氟利昂(如CCl2F2)可在光的作用下分解,产生氯原子,氯原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3)。有关反应如下:
O3
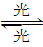 O2+O Cl+O3=ClO+O2 ClO+O=Cl+O2 总反应:2O3===3O2
O2+O Cl+O3=ClO+O2 ClO+O=Cl+O2 总反应:2O3===3O2在上述臭氧变成氧气的过程中,Cl是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)图1记录了1940~2000的60年间 排放总量的变化,以及产生
排放总量的变化,以及产生 的主要因素,燃料燃烧和交通运输是空气中
的主要因素,燃料燃烧和交通运输是空气中 的两大主要来源,请用方程式解释为什么交通运输中会产生
的两大主要来源,请用方程式解释为什么交通运输中会产生 的原因
的原因______ 。 排放量迅速降低,其中原因主要有三:
排放量迅速降低,其中原因主要有三:
①工业生产中的 尾气主要通过集中处理而大幅减少,以碱吸收法和氨还原法为要。
尾气主要通过集中处理而大幅减少,以碱吸收法和氨还原法为要。
碱液吸收法中沙及到的主要反应为: ,
,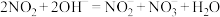 。
。
若碱液回收尾气以后,溶液中 和
和 的物质的量之比为1∶15,则尾气中NO和
的物质的量之比为1∶15,则尾气中NO和 的体积比为
的体积比为______ 。
氨还原法是在催化剂作用下,用 还原NO或
还原NO或 ,相应的化学反应方程式分别为
,相应的化学反应方程式分别为______ 、______ 。
若在相同条件下消耗的 和生成的
和生成的 的体积相等,则氮氧化物中的x为
的体积相等,则氮氧化物中的x为______ 。
②交通运输中汽车在尾气排放之前经过三元催化剂的处理,促使尾气中的CO和NO相互反应,转化为可以参与大气循环的气体,其反应方程式为______ 。
③结合社会生活中交通工具的变化,你认为 的排放总量的下降,还与哪些因素有关?
的排放总量的下降,还与哪些因素有关?______ (请至少例举一条)
(1)图1记录了1940~2000的60年间
 排放总量的变化,以及产生
排放总量的变化,以及产生 的主要因素,燃料燃烧和交通运输是空气中
的主要因素,燃料燃烧和交通运输是空气中 的两大主要来源,请用方程式解释为什么交通运输中会产生
的两大主要来源,请用方程式解释为什么交通运输中会产生 的原因
的原因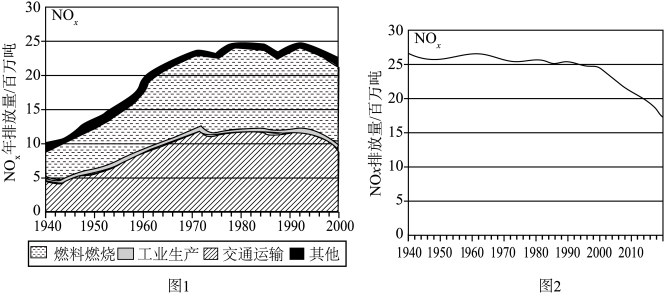
 排放量迅速降低,其中原因主要有三:
排放量迅速降低,其中原因主要有三:①工业生产中的
 尾气主要通过集中处理而大幅减少,以碱吸收法和氨还原法为要。
尾气主要通过集中处理而大幅减少,以碱吸收法和氨还原法为要。碱液吸收法中沙及到的主要反应为:
 ,
,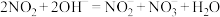 。
。若碱液回收尾气以后,溶液中
 和
和 的物质的量之比为1∶15,则尾气中NO和
的物质的量之比为1∶15,则尾气中NO和 的体积比为
的体积比为氨还原法是在催化剂作用下,用
 还原NO或
还原NO或 ,相应的化学反应方程式分别为
,相应的化学反应方程式分别为若在相同条件下消耗的
 和生成的
和生成的 的体积相等,则氮氧化物中的x为
的体积相等,则氮氧化物中的x为②交通运输中汽车在尾气排放之前经过三元催化剂的处理,促使尾气中的CO和NO相互反应,转化为可以参与大气循环的气体,其反应方程式为
③结合社会生活中交通工具的变化,你认为
 的排放总量的下降,还与哪些因素有关?
的排放总量的下降,还与哪些因素有关?
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】二十大报告中关于生态环境保护的论述全面而深刻,对研究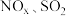 等大气污染物的妥善处理具有重要指导意义。
等大气污染物的妥善处理具有重要指导意义。
主要污染物
(1)上表为孝感市某日空气质量报告,当日的首要空气污染物为___________ 。
(2)煤炭燃烧造成环境污染的主要原因之一是形成硝酸型酸雨。
①氮元素在元素周期表中的位置___________ ,酸雨的pH___________ (填“>”、“<”或“=”)5.6。
②煤燃烧产生的废气中的NO可以转化为硝酸,其过程一般分两步:
第一步为
第二步为___________ 。
(3)CO、 和
和 等城市空气污染物来源之一为汽车尾气。三元催化可将汽车尾气中的CO和
等城市空气污染物来源之一为汽车尾气。三元催化可将汽车尾气中的CO和 进行净化处理,该过程中发生反应的化学方程式为
进行净化处理,该过程中发生反应的化学方程式为___________ 。
(4)硝酸工业废气中有氨氧化物( ),在酸性
),在酸性 溶液中,
溶液中, 氧化NO生成
氧化NO生成 和
和 。已知酸性
。已知酸性 溶液的初始pH越小,硝酸尾气NO转化率越高,其原因是
溶液的初始pH越小,硝酸尾气NO转化率越高,其原因是___________ 。
(5)通过如下流程可实现 和NO综合处理并获得保险粉(
和NO综合处理并获得保险粉( )和硝酸铵。
)和硝酸铵。
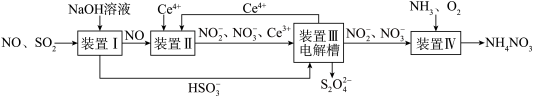
装置Ⅲ中生成 与
与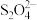 的物质的量之比为
的物质的量之比为___________ 。
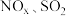 等大气污染物的妥善处理具有重要指导意义。
等大气污染物的妥善处理具有重要指导意义。主要污染物
| PM2.5 | 91 | PM10 | 166 |
| (可入肺颗粒物) | 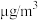 | (可吸入颗粒物) | 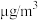 |
 | 23 |  | 78 |
| (二氧化硫) | 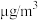 | (二氧化氯) | 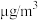 |
| CO | 1 |  | 41 |
| (一氧化碳) | 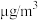 | (臭氧) | 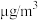 |
(1)上表为孝感市某日空气质量报告,当日的首要空气污染物为
(2)煤炭燃烧造成环境污染的主要原因之一是形成硝酸型酸雨。
①氮元素在元素周期表中的位置
②煤燃烧产生的废气中的NO可以转化为硝酸,其过程一般分两步:
第一步为

第二步为
(3)CO、
 和
和 等城市空气污染物来源之一为汽车尾气。三元催化可将汽车尾气中的CO和
等城市空气污染物来源之一为汽车尾气。三元催化可将汽车尾气中的CO和 进行净化处理,该过程中发生反应的化学方程式为
进行净化处理,该过程中发生反应的化学方程式为(4)硝酸工业废气中有氨氧化物(
 ),在酸性
),在酸性 溶液中,
溶液中, 氧化NO生成
氧化NO生成 和
和 。已知酸性
。已知酸性 溶液的初始pH越小,硝酸尾气NO转化率越高,其原因是
溶液的初始pH越小,硝酸尾气NO转化率越高,其原因是(5)通过如下流程可实现
 和NO综合处理并获得保险粉(
和NO综合处理并获得保险粉( )和硝酸铵。
)和硝酸铵。
装置Ⅲ中生成
 与
与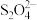 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)典型物质的电子式
NH4Cl:__________ Na2O2:________ CO2:___________ -OH:__________
(2)某短周期元素含氧酸的化学式为HXO3,其气态氢化物的化学式为HX,则X元素在周期表中的位置为_______ 。
(3)石油的综合利用方法有四种,其中____ 的目的是提高轻质油的产量,_____ 主要是得到甲烷、乙烯、丙烯等化工原料,_______ 是从石油中获得苯、甲苯等化工原料。
(4)填写有机除杂试剂
C2H6(C2H4)__________
乙酸乙酯(乙酸或乙醇)_____
乙醇(水)____________
苯(溴)________________
(5)无机方程式书写
①海带提碘的氧化环节,使用稀硫酸酸化的双氧水氧化I-的离子方程式为_______
②海水提溴吸收塔(SO2的水溶液)中的反应离子方程式为__________
③以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
a.高温下,向金红石与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体__________
b.在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛_____
(6)有机方程式书写
①乙醇去氢催化氧化生成乙醛的化学方程式:_______
②对苯二甲酸与乙二醇在一定条件下发生缩聚反应生成涤纶的化学方程式:___
③苯的硝化反应____________
NH4Cl:
(2)某短周期元素含氧酸的化学式为HXO3,其气态氢化物的化学式为HX,则X元素在周期表中的位置为
(3)石油的综合利用方法有四种,其中
(4)填写有机除杂试剂
C2H6(C2H4)
乙酸乙酯(乙酸或乙醇)
乙醇(水)
苯(溴)
(5)无机方程式书写
①海带提碘的氧化环节,使用稀硫酸酸化的双氧水氧化I-的离子方程式为
②海水提溴吸收塔(SO2的水溶液)中的反应离子方程式为
③以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
a.高温下,向金红石与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体
b.在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛
(6)有机方程式书写
①乙醇去氢催化氧化生成乙醛的化学方程式:
②对苯二甲酸与乙二醇在一定条件下发生缩聚反应生成涤纶的化学方程式:
③苯的硝化反应
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】用CO和H2在443~473K温度下,并用钴作催化剂时,可以反应生成n=5~8的烷烃,这是人工合成汽油的方法之一。
(1)写出用CnH2n+2表示人工合成汽油的化学方程式___________ 。
(2)如果向密闭的合成塔里通入恰好能完全反应的CO和H2,当完全反应后,合成塔内温度不变,而塔内气体压强降低到原来的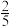 。计算说明这时有无汽油生成
。计算说明这时有无汽油生成_____ 。
(3)要达到上述合成汽油的要求,CO和H2的体积比的取值范围是______________ 。
(1)写出用CnH2n+2表示人工合成汽油的化学方程式
(2)如果向密闭的合成塔里通入恰好能完全反应的CO和H2,当完全反应后,合成塔内温度不变,而塔内气体压强降低到原来的
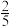 。计算说明这时有无汽油生成
。计算说明这时有无汽油生成(3)要达到上述合成汽油的要求,CO和H2的体积比的取值范围是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】我国石油工业一般采用恒电流库伦分析法测定汽油的溴指数。溴指数是指每100克试样消耗溴的毫克数,它反映了试样中C=C的数目。测定时将V(毫升)试样加入库伦分析池中,利用电解产生的溴与不饱和烃反应。当反应完全后,过量溴在指示电极上还原而指示终点。支持电解质为LiBr,溶剂系统仅含5%水,其余为甲醇、苯与醋酸。设d为汽油试样密度,Q为终点时库伦计指示的溴化反应消耗的电量(库伦)。
(1)导出溴指数与V、d和Q的关系式(注:关系式中只允许有一个具体的数值)_______ 。
(2)若在溶剂体系中增加苯的比例,说明其优缺点_______ 。
(1)导出溴指数与V、d和Q的关系式(注:关系式中只允许有一个具体的数值)
(2)若在溶剂体系中增加苯的比例,说明其优缺点
您最近半年使用:0次



