向27.2g固体Cu(部分被氧化为Cu2O)中加入某浓度的硝酸0.1L,固体物质完全溶解,生成NO2和NO气体,混合气体在标况下体积共8.96L。在所得溶液中加入1.0 mol·L-1的NaOH溶液1.0L,此时溶液呈中性,并得到蓝色沉淀,沉淀质量为39.2g。试计算(写出简要过程)
(1)固体中Cu2O的质量;____
(2)产生的NO在标况下体积;____
(3)固体物质与硝酸反应后,剩余的硝酸的物质的量浓度(忽略溶液体积变化)。___
(1)固体中Cu2O的质量;
(2)产生的NO在标况下体积;
(3)固体物质与硝酸反应后,剩余的硝酸的物质的量浓度(忽略溶液体积变化)。
更新时间:2019-10-22 13:39:25
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】硝酸跟金属反应时,随着硝酸浓度的下降和金属活动性的增大,产物中氮元素的化合价会逐渐下降,它们可能是NO2、NO、N2O、N2或NH4NO3中的一种或几种。现有一定量的铁粉和铝粉组成的混合物跟100 mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00 mol·L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解):
请回答下列问题:
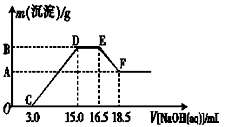
(1)由图可知,往反应后的澄清溶液中加入NaOH溶液没有立即出现沉淀,其原因是______________________________ 。
(2)混合物跟稀硝酸充分反应后的产物中铁元素的化合价是___ 。
(3)写出图中D―→E阶段所发生的反应的离子方程式:____________________ 。
(4)纵坐标中A点的数值是_________ ,原硝酸的浓度是_____________ 。
请回答下列问题:

(1)由图可知,往反应后的澄清溶液中加入NaOH溶液没有立即出现沉淀,其原因是
(2)混合物跟稀硝酸充分反应后的产物中铁元素的化合价是
(3)写出图中D―→E阶段所发生的反应的离子方程式:
(4)纵坐标中A点的数值是
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如图所示,则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为____ ,按反应的先后顺序写出该过程的离子反应方程式:___________ 。

您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】3.84克铜与足量的浓硫酸在加热条件下充分反应。
(1)求生成的气体在标准状况下的体积是多少___ ?
(2)求被还原的硫酸的物质的量是多少___ ?
(1)求生成的气体在标准状况下的体积是多少
(2)求被还原的硫酸的物质的量是多少
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】向铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500mL,再加入足量锌粉,使之充分反应,收集到2.24L(标准状况)气体.过滤得残留固体,干燥后,质量减轻了7.5g.求原硫酸的物质的量浓度。_____________
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL4.40mol/L盐酸中,充分反应后产生896mLH2(标准状况),残留固体1.28g。过滤,滤液中无Cu2+。将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L。求原混合物中单质铁的质量。
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将Cu2O与Fe2O3的混合物共ag加入20.0mL4.00mol·L-1的过量稀硫酸中,充分反应后剩余固体的质量为bg。请计算:
(1)若向反应后的溶液中加入40.0mLNaOH溶液能刚好使溶液中的所有金属离子完全沉淀,则该氢氧化钠溶液的物质的量浓度为__________________ mol·L-1。
(2)若a=7b,则混合物中Cu2O与Fe2O3的物质的量之比为__________________ 。
(1)若向反应后的溶液中加入40.0mLNaOH溶液能刚好使溶液中的所有金属离子完全沉淀,则该氢氧化钠溶液的物质的量浓度为
(2)若a=7b,则混合物中Cu2O与Fe2O3的物质的量之比为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】电解饱和食盐水是一项重要的化学工业,请完成下列计算:
(1)当电解产生0.2molNaOH时,能收集到标准状况下的H2____ L。
(2)已知室温时饱和食盐水的溶质质量分数为0.265,取200g饱和食盐水进行电解,当NaCl反应了一半时停止电解,
①求出所得混合溶液中NaCl的质量。_____
②求出所得混合溶液中NaOH的质量分数。____ (写出计算过程,保留3位小数)
(1)当电解产生0.2molNaOH时,能收集到标准状况下的H2
(2)已知室温时饱和食盐水的溶质质量分数为0.265,取200g饱和食盐水进行电解,当NaCl反应了一半时停止电解,
①求出所得混合溶液中NaCl的质量。
②求出所得混合溶液中NaOH的质量分数。
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】计算
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为_______ 。
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为_______ 。
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为_______ 。
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为_______ 。
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】生态农业涉及农家肥料的综合利用。某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体16.8L(标准状况)。该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为: 。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L 0.1mol/L的澄清
。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L 0.1mol/L的澄清 溶液,充分吸收,生成沉淀10g。
溶液,充分吸收,生成沉淀10g。
(1)原混合气体的物质的量是___________ mol。
(2)设反应后溶液体积不变,则反应后澄清 溶液的物质的量的浓度
溶液的物质的量的浓度_________ mol/L。
(3)原混合气体中氮气的体积是_________ L。
 。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L 0.1mol/L的澄清
。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L 0.1mol/L的澄清 溶液,充分吸收,生成沉淀10g。
溶液,充分吸收,生成沉淀10g。(1)原混合气体的物质的量是
(2)设反应后溶液体积不变,则反应后澄清
 溶液的物质的量的浓度
溶液的物质的量的浓度(3)原混合气体中氮气的体积是
您最近半年使用:0次



