金属的冶炼方法有很多,有加热法,热还原法、 电解法、湿法治金等:我国古代利用铁和硫酸铜溶液反应炼铜,属于___ (填冶炼的方法);铝热反应是铝与一些金属氧化物在高温下反应,属于___ (填冶炼的方法);写出铝与四氧化三铁的反应方程式:____ 。
更新时间:2019-10-24 12:25:18
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】铜、铁、铝是应用最广泛的三种金属。它们在人类的金属使用历史中,由早到晚的顺序为_________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】阅读下面一段材料,根据所学知识,回答下列问题:
将用砂纸打磨过的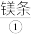 在空气中燃烧,生成
在空气中燃烧,生成 和
和 ,氮化镁溶于水得到
,氮化镁溶于水得到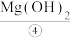 固体和
固体和 ,将Mg(OH)2固体溶于
,将Mg(OH)2固体溶于 ,得到无色溶液,将无色溶液经过一系列操作得到
,得到无色溶液,将无色溶液经过一系列操作得到 ,将
,将 在
在 气流中加热得到
气流中加热得到 。
。
(1)镁在元素周期表中的位置是___________ ,MgCl2中含有的化学键类型为___________ 。
(2)常温下,上述有标号的物质中,能导电的是___________ (填标号,下同),属于电解质的有___________ 。
(3)写出氮化镁固体溶于水发生反应的化学方程式:___________ 。
(4)实验1:将一块金属钠投入MgCl2溶液中,写出发生反应的离子方程式:___________ 。
实验2:将已经打磨过的、大小相同的镁条与铝片分别同时投入足量 的稀硫酸中,相同时间内,观察到的现象为
的稀硫酸中,相同时间内,观察到的现象为___________ ,可得出的结论是___________ 。
将用砂纸打磨过的
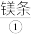 在空气中燃烧,生成
在空气中燃烧,生成 和
和 ,氮化镁溶于水得到
,氮化镁溶于水得到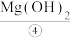 固体和
固体和 ,将Mg(OH)2固体溶于
,将Mg(OH)2固体溶于 ,得到无色溶液,将无色溶液经过一系列操作得到
,得到无色溶液,将无色溶液经过一系列操作得到 ,将
,将 在
在 气流中加热得到
气流中加热得到 。
。(1)镁在元素周期表中的位置是
(2)常温下,上述有标号的物质中,能导电的是
(3)写出氮化镁固体溶于水发生反应的化学方程式:
(4)实验1:将一块金属钠投入MgCl2溶液中,写出发生反应的离子方程式:
实验2:将已经打磨过的、大小相同的镁条与铝片分别同时投入足量
 的稀硫酸中,相同时间内,观察到的现象为
的稀硫酸中,相同时间内,观察到的现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】金属和非金属在人类生产生活中得到了广泛应用,请你回答下列问题。
(1)面包发酵粉的主要成分之一是一种钠盐,其俗称为________ ;漂白粉的有效成分为__________ (写化学式);FeCl3常用作净水剂,其原理为_________ (用离子方程式表示)。
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是_________ 。
(3)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生素C可以解毒.对上述的分析正确的是( )
A.亚硝酸盐是还原剂 B.维生素C是氧化剂
C.维生素C被氧化 D.亚硝酸盐发生氧化反应
(4)某CuSO4、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),且SO42-的物质的量浓度为6mol/L,则此溶液中阳离子的浓度为___________ mol/L,若向此溶液中加入金属Zn,则最多溶解Zn的质量为____________ g。
(1)面包发酵粉的主要成分之一是一种钠盐,其俗称为
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(3)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生素C可以解毒.对上述的分析正确的是
A.亚硝酸盐是还原剂 B.维生素C是氧化剂
C.维生素C被氧化 D.亚硝酸盐发生氧化反应
(4)某CuSO4、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),且SO42-的物质的量浓度为6mol/L,则此溶液中阳离子的浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请按要求回答下列问题:
(1)盛放烧碱液的试剂瓶不能用玻璃塞,是为了防止发生_______________________________ 反应(用化学方程式表示),而使瓶塞与瓶口粘在一起;
(2)铝热反应在工业生产中的重要用途之一是_____________________ ;
(3)“ 硅材料”又被称为信息材料。其中广泛用于光导纤维的材料是______________ (填化学式,下同);广泛用于制造集成电路的材料是________________ ;
(1)盛放烧碱液的试剂瓶不能用玻璃塞,是为了防止发生
(2)铝热反应在工业生产中的重要用途之一是
(3)“ 硅材料”又被称为信息材料。其中广泛用于光导纤维的材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】影响冶炼方法的主要因素是____________ ,不活泼金属,如:Hg、Ag等采用_________ 法冶炼,Fe、Cu、Zn等金属等采用_________ 法冶炼,K、Ca、Na等强还原性金属采用_________ 法冶炼,写出冶炼金属铝的化学反应方程式________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金,理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成了铁铝合金。你认为他的解释是否合理?答:___________ (填“合理”或“不合理”)
请设计一个简单实验方案,证明上述所得的块状熔融物中含有金属铝;该实验所用试剂是___________ ,反应的化学方程式为___________ 。
(2)现有A:KI溶液;B:淀粉溶液;C:NaOH溶液;D:新制氯水等四种溶液。现将它们按某种顺序依次加入一支试管中,发现溶液颜色依下列次序变化:①无色→②棕黄色→③蓝色→④无色。请回答
写出加入药品的顺序(用字母表示):___________ ;
写出①→②的离子反应方程式:___________ ;
写出③→④蓝色变无色的化学方程式:___________ 。
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | --- |
(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金,理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成了铁铝合金。你认为他的解释是否合理?答:
请设计一个简单实验方案,证明上述所得的块状熔融物中含有金属铝;该实验所用试剂是
(2)现有A:KI溶液;B:淀粉溶液;C:NaOH溶液;D:新制氯水等四种溶液。现将它们按某种顺序依次加入一支试管中,发现溶液颜色依下列次序变化:①无色→②棕黄色→③蓝色→④无色。请回答
写出加入药品的顺序(用字母表示):
写出①→②的离子反应方程式:
写出③→④蓝色变无色的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】判断正误
1.铝在自然界中有游离态和化合态两种形式。(_______)
2.MgO与Al粉的混合物也可称为铝热剂。(_______)
3.铝与Fe2O3发生铝热反应,反应后固体物质增重。(_______)
4.冶炼铝时常用焦炭做还原剂。(_______)
5.由于铝在空气中不会锈蚀,所以铝制品的使用寿命都很长。(_______)
6.由于铝具有强还原性,所以常用铝来冶炼某些高熔点金属。(_______)
7.常温下,铝被浓硫酸钝化,所以可用浓硫酸除去铝表面的铜镀层。(_______)
8.由于铝的导电性能比铜强,所以常用铝制造电线、电缆。(_______)
9.铝与少量NaOH溶液反应得到铝盐,与足量NaOH溶液反应生成偏铝酸盐。(_______)
10.铝能在空气中稳定存在是因为其表面覆盖着一层氧化铝薄膜。(_______)
1.铝在自然界中有游离态和化合态两种形式。(_______)
2.MgO与Al粉的混合物也可称为铝热剂。(_______)
3.铝与Fe2O3发生铝热反应,反应后固体物质增重。(_______)
4.冶炼铝时常用焦炭做还原剂。(_______)
5.由于铝在空气中不会锈蚀,所以铝制品的使用寿命都很长。(_______)
6.由于铝具有强还原性,所以常用铝来冶炼某些高熔点金属。(_______)
7.常温下,铝被浓硫酸钝化,所以可用浓硫酸除去铝表面的铜镀层。(_______)
8.由于铝的导电性能比铜强,所以常用铝制造电线、电缆。(_______)
9.铝与少量NaOH溶液反应得到铝盐,与足量NaOH溶液反应生成偏铝酸盐。(_______)
10.铝能在空气中稳定存在是因为其表面覆盖着一层氧化铝薄膜。(_______)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】自然资源的综合利用和环境污染的研究及治理是化学重要研究课题。
(1)请写出工业上通过电解法冶炼活泼金属镁的化学方程式:_______ 。对于不活泼的金属通过加热其化合物使其分解,写出冶炼金属银的化学方程式:_______ 。
(2)①海水淡化的方法常见的有_______ 、电渗析法和离子交换法。
②煤可以通过干馏、气化和液化获得清洁燃料和多种化工原料。煤的干馏是_______ 变化(填“物理”或“化学”)。煤的气化是将煤转化为可燃性气体的过程,主要反应是碳与水蒸气反应生成水煤气,该反应的化学方程式为_______ 。
(3)汽车的发明与使用是人类智慧的杰出体现,它为人们的生活和生产带来了极大的方便,同时由此引发的环境污染问题也越来越引起人们的关注。汽车排放的尾气中因含有氮的氧化物而污染大气,产生氮的氧化物的主要原因是在高温条件下_______ ,治理汽车尾气中 和
和 的方法之一是在汽车的排气管上装一个催化转化装置,使
的方法之一是在汽车的排气管上装一个催化转化装置,使 和
和 在催化剂的作用下转化为无毒物质,写出该反应的化学方程式:
在催化剂的作用下转化为无毒物质,写出该反应的化学方程式:_______ 。
(1)请写出工业上通过电解法冶炼活泼金属镁的化学方程式:
(2)①海水淡化的方法常见的有
②煤可以通过干馏、气化和液化获得清洁燃料和多种化工原料。煤的干馏是
(3)汽车的发明与使用是人类智慧的杰出体现,它为人们的生活和生产带来了极大的方便,同时由此引发的环境污染问题也越来越引起人们的关注。汽车排放的尾气中因含有氮的氧化物而污染大气,产生氮的氧化物的主要原因是在高温条件下
 和
和 的方法之一是在汽车的排气管上装一个催化转化装置,使
的方法之一是在汽车的排气管上装一个催化转化装置,使 和
和 在催化剂的作用下转化为无毒物质,写出该反应的化学方程式:
在催化剂的作用下转化为无毒物质,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)地壳中含量最高的金属元素是________ 。
(2)根据金属的下列应用:①制电线,②制金属细丝,③制炊具,推断金属具有的物理性质是__________ 。
(3)人们每年要从金属矿物资源中提取大量的金属,根据所学化学知识,按要求写出两个生成金属的化学方程式:
①___________________________________________________ (置换反应);
②___________________________________________________ (分解反应)。
(1)地壳中含量最高的金属元素是
(2)根据金属的下列应用:①制电线,②制金属细丝,③制炊具,推断金属具有的物理性质是
(3)人们每年要从金属矿物资源中提取大量的金属,根据所学化学知识,按要求写出两个生成金属的化学方程式:
①
②
您最近一年使用:0次



