某化学实验小组用酸性KMnO4溶液和草酸(H2C2O4)溶液反应,研究外界条件反应速率的影响,实验操作及现象如下:
(1)高锰酸钾与草酸反应的离子方程式:______________________________________
(2)由实验I、II可得出的结论是____________________________ 。
(3)关于实验II中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的Mn2+对反应有催化作用。利用提供的试剂设计实验III,验证猜想。
提供的试剂:0.01mol/L酸性 KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
① 补全实验III的操作:向试管中先加入1mL 0.01mol/L酸性 KMnO4溶液,______ ,最后加入1mL 0.1mol/L草酸溶液。
② 若猜想成立,应观察到的实验现象是______ 。
(4)该小组拟采用如图所示的实验方案继续探究外界条件对反应速率的影响。
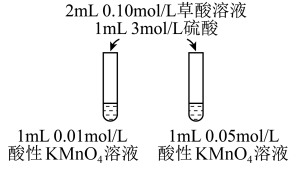
① 他们拟研究的影响因素是______ 。
② 你认为他们的实验方案______ (填“合理”或“不合理”),理由是______ 。
| 编号 | 实验操作 | 实验现象 |
| I | 向一支试管中先加入1mL 0.01 mol/L酸性 KMnO4溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入1mL 0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅, 30 in后几乎变为无色 |
| II | 向另一支试管中先加入1mL 0.01mol/L酸性 KMnO4溶液,再加入10滴3mol/L硫酸,最后加入1mL 0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
(1)高锰酸钾与草酸反应的离子方程式:
(2)由实验I、II可得出的结论是
(3)关于实验II中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的Mn2+对反应有催化作用。利用提供的试剂设计实验III,验证猜想。
提供的试剂:0.01mol/L酸性 KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
① 补全实验III的操作:向试管中先加入1mL 0.01mol/L酸性 KMnO4溶液,
② 若猜想成立,应观察到的实验现象是
(4)该小组拟采用如图所示的实验方案继续探究外界条件对反应速率的影响。

① 他们拟研究的影响因素是
② 你认为他们的实验方案
19-20高二上·黑龙江大庆·阶段练习 查看更多[3]
黑龙江省大庆铁人中学2019-2020学年高二10月月考化学试题人教版高中化学(2019)必修第二册第六章《化学反应与能量》检测题(已下线)专题06 化学反应的速率和限度(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)
更新时间:2019-10-18 12:26:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ、实验室可在简易量热计中进行中和反应,通过测定反应过程中所放出的热量可计算中和热ΔH。回答下列问题:
(1)该实验中往往用0.50 mol·L-1HCl和0.55 mol·L-1的NaOH溶液各50 mL。NaOH的浓度大于HCl的浓度的作用是_______ 。当室温低于10 ℃时进行,对实验结果会造成较大的误差,原因是_______ 。
(2)实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热_______ (填“相等”或“不相等”),理由是_______ 。
(3)下列关于中和热实验的说法,正确的是_______ (填字母)
Ⅱ、某学生设计如下图Ⅰ装置,测定2 mol/L的硫酸与锌粒和锌粉反应的速率。请回答:

(4)装置图Ⅰ进行实验时,还需要使用到的仪器(或用品)是_______ 。
(5)按照图Ⅰ装置实验时,他限定了实验时间为10 min,他还需要测定的另一个数据是_______ 。
(6)对比实验结束后,得到的结论是_______ 。
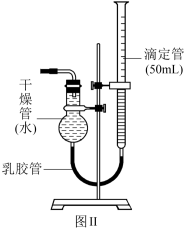
(7)该生又将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所在处的刻度数,发现滴定管中液面高于干燥管中液面,应首先采取的操作是_______ 。
(1)该实验中往往用0.50 mol·L-1HCl和0.55 mol·L-1的NaOH溶液各50 mL。NaOH的浓度大于HCl的浓度的作用是
(2)实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热
(3)下列关于中和热实验的说法,正确的是
| A.在测定中和热的过程中,每一组实验需要测定并记录温度2次 |
| B.大烧杯上若不盖硬纸板,测得的中和热数值会偏小 |
| C.用相同浓度和体积的氨水代替NaOH溶液进行实验,测得的中和热数值会偏大 |
| D.为防止液体溅出,酸碱混合时应将量筒中的溶液缓缓倒入烧杯中再慢慢搅拌 |
Ⅱ、某学生设计如下图Ⅰ装置,测定2 mol/L的硫酸与锌粒和锌粉反应的速率。请回答:

(4)装置图Ⅰ进行实验时,还需要使用到的仪器(或用品)是
(5)按照图Ⅰ装置实验时,他限定了实验时间为10 min,他还需要测定的另一个数据是
(6)对比实验结束后,得到的结论是
(7)该生又将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所在处的刻度数,发现滴定管中液面高于干燥管中液面,应首先采取的操作是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组进行以下实验探究。
Ⅰ.设计实验探究反应速率的测定和比较实验步骤:
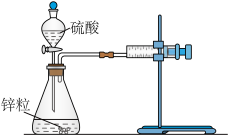
(1)用如图所示装置,加入 的稀硫酸溶液,测量收集
的稀硫酸溶液,测量收集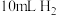 所需的时间。
所需的时间。
(2)另取一套相同的装置,加入40 mL 4 mol·L-1的稀硫酸溶液,测量收集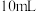 (相同条件下)
(相同条件下) 所需的时间。
所需的时间。
实验现象:锌跟稀硫酸反应产生气泡,收集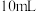 气体,(2)所用时间比(1)所用时间
气体,(2)所用时间比(1)所用时间__________ (填“长”或“短”)
实验结论: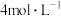 的稀硫酸与锌反应比
的稀硫酸与锌反应比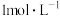 的稀硫酸与锌反应速率
的稀硫酸与锌反应速率___________ (填“大”或“小”):
注意事项:①锌粒的质量、颗粒(即表面积)大小___________ ;
②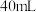 的硫酸要迅速加入;
的硫酸要迅速加入;
③装置____________ ,且计时要迅速准确;
④气体收集可以用排水量气装置代替。
实验讨论:除本实验测定反应速率的方法外,可行的方案还有_________________________ (任写一种)。
Ⅱ.利用 与大理石反应来研究影响反应速率的因素,所用
与大理石反应来研究影响反应速率的因素,所用 浓度为
浓度为 、
、 ,大理石有细颗粒与粗颗粒两种规格,实验温度为
,大理石有细颗粒与粗颗粒两种规格,实验温度为 、
、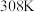 。
。
请完成以下实验设计表。
Ⅰ.设计实验探究反应速率的测定和比较实验步骤:

(1)用如图所示装置,加入
 的稀硫酸溶液,测量收集
的稀硫酸溶液,测量收集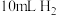 所需的时间。
所需的时间。(2)另取一套相同的装置,加入40 mL 4 mol·L-1的稀硫酸溶液,测量收集
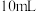 (相同条件下)
(相同条件下) 所需的时间。
所需的时间。实验现象:锌跟稀硫酸反应产生气泡,收集
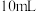 气体,(2)所用时间比(1)所用时间
气体,(2)所用时间比(1)所用时间实验结论:
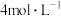 的稀硫酸与锌反应比
的稀硫酸与锌反应比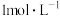 的稀硫酸与锌反应速率
的稀硫酸与锌反应速率注意事项:①锌粒的质量、颗粒(即表面积)大小
②
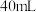 的硫酸要迅速加入;
的硫酸要迅速加入;③装置
④气体收集可以用排水量气装置代替。
实验讨论:除本实验测定反应速率的方法外,可行的方案还有
Ⅱ.利用
 与大理石反应来研究影响反应速率的因素,所用
与大理石反应来研究影响反应速率的因素,所用 浓度为
浓度为 、
、 ,大理石有细颗粒与粗颗粒两种规格,实验温度为
,大理石有细颗粒与粗颗粒两种规格,实验温度为 、
、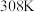 。
。请完成以下实验设计表。
| 实验编号 | T/K | 大理石规格 | 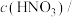  | 实验目的 |
| ① | 298 | 粗颗粒 |  | (1)实验①和②探究 浓度对该反应速率的影响; 浓度对该反应速率的影响;(2)实验①和 (3)实验①和 |
| ② | ||||
| ③ | 粗颗粒 | |||
| ④ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】为了进一步探究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积气体所需的时间。
请完成此实验设计,其中:V1=_____ ,V6=______ ,V9=________ 。
实验 混合溶液 | A | B | C | D | E | F |
4mol·L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
请完成此实验设计,其中:V1=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W 是原子序数依次增大的短周期主族元素,X、Z位于同一主族且二者均可与Y元素形成两种常见的化合物,W 原子的最外层电子比次外层上电子少5 个。
(1)几种元素的原子半径由大到小的顺序是_________ (用元素符号表示),X 与Z 可形成一种稳定的化合物,该化合物的化学式为_________ 。
(2)欲用实验方法证明金属性:Z >W,所用试剂为______ ,相应的实验现象为____________ 。
(3)X2Y2 在Fe3+ 催化下可发生分解反应,为探究一定温度下X2Y2 溶液的浓度、Fe3+的浓度对X2Y2 分解速率的影响情况,其同学设计了如下实验,内容如下表所示:
①V1=________ 。
②实验I、II的探究目的是_____________________ 。
③实验I、III探究催化剂浓度对X2Y2 分解速率的影响情况,则V2=______ ,若实验III中产生气泡的速率较快,由此可得出的结论是_________________ 。
(1)几种元素的原子半径由大到小的顺序是
(2)欲用实验方法证明金属性:Z >W,所用试剂为
(3)X2Y2 在Fe3+ 催化下可发生分解反应,为探究一定温度下X2Y2 溶液的浓度、Fe3+的浓度对X2Y2 分解速率的影响情况,其同学设计了如下实验,内容如下表所示:
| 实验序号 | 实验所用试剂 | ||||
| 酸性Fe2(SO4)3溶液 | X2Y2溶液 | H2O | |||
| V/mL | c(mol/L) | V/mL | c(mol/L) | V/mL | |
| I | 4 | 0.1 | 3 | 2 | 3 |
| II | 4 | 0.1 | 2 | 2 | V1 |
| III | 5 | 0.1 | V2 | 2 | 2 |
②实验I、II的探究目的是
③实验I、III探究催化剂浓度对X2Y2 分解速率的影响情况,则V2=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】结合所学内容回答下列问题:
Ⅰ.某实验小组以H2O2的分解为例,研究浓度、催化剂、温度对化学反应速率的影响,按照如下方案设计实验。
(1)实验①和②的目的是研究_______________ 对反应速率的影响。
(2)实验③和④测得生成氧气的体积随时间变化的关系如下图所示。

分析上图能够得出的实验结论是________________________________________________ 。
(3)实验⑤和⑥是研究温度相差10℃对反应速率的影响,请在上面表格空白处补齐对应的内容_________ 。
Ⅱ.某温度时,在2L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:

(4)反应开始至2 min,Z的平均反应速率____________ 。
(5)保持容器容积不变,在第2min时改变下列条件时,化学反应速率的变化是:
①向其中充入1 molX气体,化学反应速率_______ (填 “加快”“减慢”或“不变”,下同);
②向其中充入1 mol N2(g) (N2不参加反应),化学反应速率_______________ ;
③同时加入0.9molX、0.7molY 和0.2molZ,化学反应速率________________ 。
Ⅰ.某实验小组以H2O2的分解为例,研究浓度、催化剂、温度对化学反应速率的影响,按照如下方案设计实验。
| 实验编号 | 反应物 | 催化剂 | 温度 |
| ① | 10 mL 2% H2O2溶液 | 无 | 20℃ |
| ② | 10 mL 5% H2O2溶液 | 无 | 20℃ |
| ③ | 10 mL 5% H2O2溶液 | 1-2滴1 mol/LFeCl3溶液 | 20℃ |
| ④ | 10 mL 5% H2O2溶液 | 无 | 20℃ |
| ⑤ | 10 mL 5% H2O2溶液 | ||
| ⑥ | 无 | 20℃ |
(2)实验③和④测得生成氧气的体积随时间变化的关系如下图所示。

分析上图能够得出的实验结论是
(3)实验⑤和⑥是研究温度相差10℃对反应速率的影响,请在上面表格空白处补齐对应的内容
Ⅱ.某温度时,在2L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:

(4)反应开始至2 min,Z的平均反应速率
(5)保持容器容积不变,在第2min时改变下列条件时,化学反应速率的变化是:
①向其中充入1 molX气体,化学反应速率
②向其中充入1 mol N2(g) (N2不参加反应),化学反应速率
③同时加入0.9molX、0.7molY 和0.2molZ,化学反应速率
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)通过实验A、B,可探究出____ ( 填外部因素)的改变对化学反应速率的影响,其中 V1=____ 、T1=____ ;通过实验____ (填实验序号)可探究出温度变化对化学反应速率的影响,其中 V2=____ 。
(2)若 t1<8,则由此实验可以得出的结论是______________________ 。
| 实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)若 t1<8,则由此实验可以得出的结论是
您最近一年使用:0次



