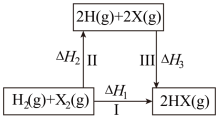
关于如图所示转化关系(X代表卤素),下列说法正确的是

A.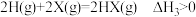 |
B.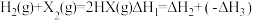 |
C.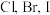 的非金属性依次减弱,所以途径II吸收的热量依次增多 的非金属性依次减弱,所以途径II吸收的热量依次增多 |
D.生成相同物质的量 放出的热量比生成 放出的热量比生成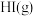 的多,说明 的多,说明 比 比 稳定 稳定 |
18-19高二·浙江·期中 查看更多[2]
更新时间:2019-11-09 15:49:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
A.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,则其热化学方程式为N2(g)+3H2(g) 2NH3(g)ΔH=-38.6kJ/mol 2NH3(g)ΔH=-38.6kJ/mol |
| B.测定盐酸和氢氧化钠反应的中和热时,每次实验均应测量三个温度,即盐酸起始温度、NaOH起始温度和反应后的终止温度 |
| C.已知:CH4的燃烧热为890.3kJ/mol,则101kPa时,CH4(g)+2O2(g)=CO2(g)+2H2O(g)的∆H<-890.3kJ/mol |
| D.已知2H2(g)+2S(g)=2H2S(g) ∆H1<0,2H2(g)+2S(s)=2H2S(g) ∆H2<0,则∆H1<∆H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】M经光照可转化成N,转化过程如下:
 ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.N的能量低,N相比M更稳定 |
| B.M生成N的过程中会形成过渡态,过渡态和N的能量差就是该反应的活化能 |
C.碳碳单键的键能为a kJ/mol,碳碳双键的键能为b kJ/mol, |
| D.M和N的标准燃烧热相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
①需要加热方能发生的反应一定是吸热反应
②化学反应的发生一定会伴随能量变化
③反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
④旧化学键的断裂说明- 一定发生了化学反应
①需要加热方能发生的反应一定是吸热反应
②化学反应的发生一定会伴随能量变化
③反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
④旧化学键的断裂说明- 一定发生了化学反应
| A.③④ | B.①② | C.②③ | D.②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】含硫物质在医药、农业、能源等领域都有广泛的应用,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图所示:

下列说法正确的是

下列说法正确的是
| A.反应Ⅰ、Ⅱ、Ⅲ均为放热反应 | B.储能过程中 被消耗 被消耗 |
| C.存储的能量不可能完全转化为电能 | D.循环过程中 为储能物质 为储能物质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法或表示方法正确的是( )
| A.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)ΔH=+285.8kJ/mol |
| B.若将等量的硫蒸气和硫固体分别完全燃烧,后者反应的△H小 |
| C.由“C(石墨)→C(金刚石) ΔH=+1.9kJ/mol”可知,金刚石比石墨稳定 |
| D.反应是放热的还是吸热的必须看反应物和生成物所具有的总能量的相对大小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法不正确的是
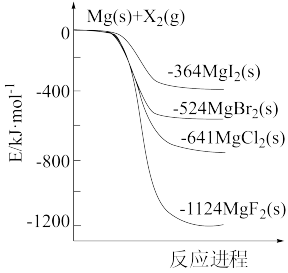

| A.由MgCl2制取Mg是吸热过程 |
| B.热稳定性:MgI2<MBr2<MgCl2<MgF2 |
| C.常温下还原性:F->Cl->Br->I- |
| D.由图知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2 (s)+Cl2(g)=MgCl2(s)+Br2 (g) △H=-117kJ/ mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】异丁烯与氯化氢可能发生两种加成反应及相应的能量变化与反应进程的关系如图所示,下列说法正确的是


| A.反应 ②的活化能大于反应① |
| B.反应①的△H 小于反应② |
| C.中间体 2 更加稳定 |
| D.改变催化剂,反应①、②的活化能和反应热发生改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各项表述与示意图一致的是
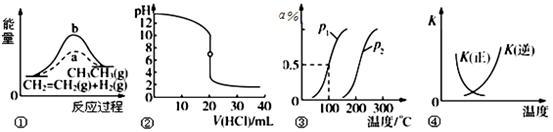

| A.图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g) →CH3CH3(g) ∆H<0;使用和未使用催化剂时,反应过程中的能量变化 |
| B.图②表示25 ℃时,用0.01 mol·L-1盐酸滴定一定体积的0.01 mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化 |
C.图③表示CH4(g)+H2O(g) CO(g)+3H2(g) ∆H,反应CH4的转化率与温度、压强的关系,且p1>p2、0>ΔH CO(g)+3H2(g) ∆H,反应CH4的转化率与温度、压强的关系,且p1>p2、0>ΔH |
D.图④中曲线表示反应2SO2(g)+O2(g) 2SO3(g) ∆H<0;正、逆反应的平衡常数K随温度的变化 2SO3(g) ∆H<0;正、逆反应的平衡常数K随温度的变化 |
您最近一年使用:0次

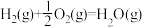
 ,
, 和
和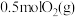 反应过程中的能量变化如图所示。a、b、c、d都表示正数,下列说法正确的是
反应过程中的能量变化如图所示。a、b、c、d都表示正数,下列说法正确的是






