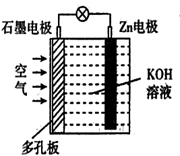
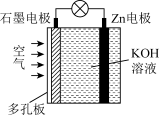
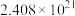锌-空气电框(原理如图)适宜用作城市电动车的动力电源。该电池放电时 转化为
转化为 。该电池工作时,下列说法正确的是
。该电池工作时,下列说法正确的是
 转化为
转化为 。该电池工作时,下列说法正确的是
。该电池工作时,下列说法正确的是
A. 电极是该电池的正极 电极是该电池的正极 |
B. 电极上的电极反应式: 电极上的电极反应式: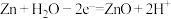 |
C. 向石墨电极移动 向石墨电极移动 |
| D.氧气在石墨电极上发生还原反应 |
更新时间:2019-11-12 09:25:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有机物液流电池因其电化学性能可调控等优点而备受关注。南京大学研究团队设计了一种水系分散的聚合物微粒“泥浆”电池(图1)。该电池在充电过程中,聚对苯二酚被氧化,下列说法错误的是
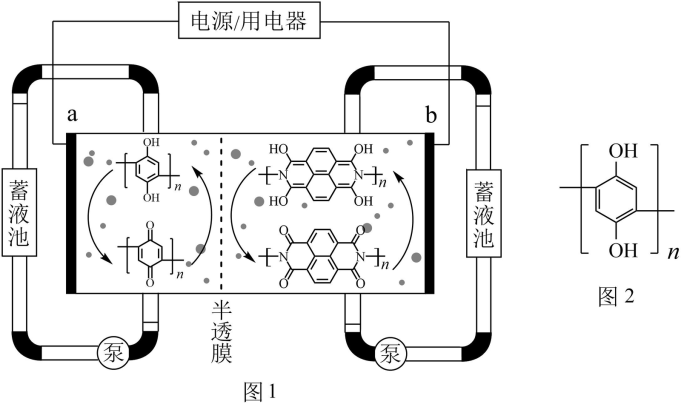
| A.放电时,电子由b电极流向a电极 |
| B.充电时,a电极附近的pH增大 |
| C.电池中间的隔膜为特殊尺寸半透膜,目的是阻止正负极物质的交叉污染 |
D.放电时,b电极的电极反应方程式为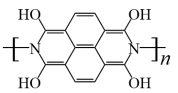 -4ne-= -4ne-=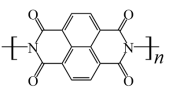 +4nH+ +4nH+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
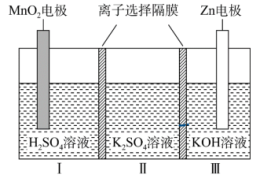
【推荐2】一种水性电解液 离子选择双隔膜电池如下图所示,已知在KOH溶液中,
离子选择双隔膜电池如下图所示,已知在KOH溶液中, 以
以 存在。电池放电时,下列说法
存在。电池放电时,下列说法不正确 的是
 离子选择双隔膜电池如下图所示,已知在KOH溶液中,
离子选择双隔膜电池如下图所示,已知在KOH溶液中, 以
以 存在。电池放电时,下列说法
存在。电池放电时,下列说法
A. 电极反应: 电极反应: |
B.Ⅰ区的 通过隔膜向Ⅱ区迁移 通过隔膜向Ⅱ区迁移 |
C.若有1molZn参与反应,则有1mol 发生迁移 发生迁移 |
D.电池总反应: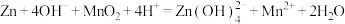 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。对该电池的描述合理的是:
①溶液中硫酸的物质的量浓度保持不变;②Cu极上有气泡产生,发生还原反应;③Cu为负极,Zn为正极;④原电池在工作时电子由负极通过溶液流向正极;⑤该装置将化学能转变为电能( )
①溶液中硫酸的物质的量浓度保持不变;②Cu极上有气泡产生,发生还原反应;③Cu为负极,Zn为正极;④原电池在工作时电子由负极通过溶液流向正极;⑤该装置将化学能转变为电能( )
| A.②⑤ | B.①③⑤ | C.②④⑤ | D.④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】表明金属甲比金属乙活动性强的叙述正确的是( )
| A.在氧化还原反应中,甲失电子数比乙多 |
| B.甲、乙氢氧化物溶液碱性:甲<乙 |
| C.甲能与盐酸反应放出H2,而乙不反应 |
| D.将甲、乙组成原电池时,甲为正极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
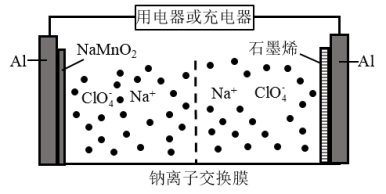
【推荐1】我国科研团队成功研究出高比能量、低成本的钠离子二次电池,其工作原理如图所示。已知电池反应:Na1-xMnO2 + NaxCn NaMnO2 + nC.下列说法错误的是
NaMnO2 + nC.下列说法错误的是
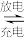 NaMnO2 + nC.下列说法错误的是
NaMnO2 + nC.下列说法错误的是
| A.电池放电过程中,NaMnO2/Al 为正极 |
| B.电池放电时,正极发生反应 Na1-xMnO2 +xNa+ +xe- =NaMnO2 |
| C.电池充电时,外接电源的负极连接 NaMnO2/Al 电极 |
| D.电池充电时,Na+由 NaMnO2/Al 电极移向石墨烯/Al 电极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某种碱性氢氧燃料电池的的正极反应式为:O2+4e-+2H2O=4OH-。下列有关该电池的叙述正确的是( )
| A.工作时,电解质溶液中的OH-向正极移动 |
| B.工作一段时间后,电解液中KOH的物质的量浓度减小 |
| C.负极上发生的反应为H2-2e-=2H+ |
| D.若电池在工作过程中有0.4mol电子转移,则正极消耗2.24L O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
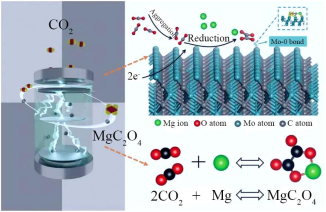
【推荐1】北京科技大学教授与浙江大学教授合作,首次探究了在完全无水环境下 电池体系的充、放电机理。其采用
电池体系的充、放电机理。其采用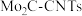 作为正极催化剂,调控
作为正极催化剂,调控 电化学氧化还原路径,将放电产物调节为
电化学氧化还原路径,将放电产物调节为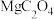 ,工作原理如图所示。下列说法错误的是
,工作原理如图所示。下列说法错误的是
 电池体系的充、放电机理。其采用
电池体系的充、放电机理。其采用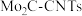 作为正极催化剂,调控
作为正极催化剂,调控 电化学氧化还原路径,将放电产物调节为
电化学氧化还原路径,将放电产物调节为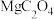 ,工作原理如图所示。下列说法错误的是
,工作原理如图所示。下列说法错误的是
A.放电时,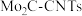 能降低正极反应的活化能 能降低正极反应的活化能 |
B.充电时,每转移4mol电子理论上生成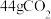 |
C.放电时,副产物可能有 |
D.充电时,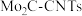 极与直流电源正极连接 极与直流电源正极连接 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
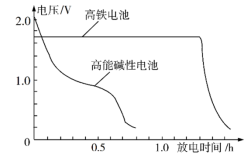
【推荐2】高铁电池是以高铁酸盐(K2FeO4、BaFeO4等)为材料的新型可充电电池,这种电池能量密度大、体积小、重量轻、污染低。这种电池的总反应为:3Zn+2 +8H2O
+8H2O 3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
 +8H2O
+8H2O 3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
| A.放电过程中正极区域电解液pH升高 |
| B.放电时负极反应式为:Zn+2H2O−2e−=Zn(OH)2+2H+ |
| C.充电时,每转移3 mol电子,则有1 mol Fe(OH)3被氧化 |
| D.高铁电池比高能碱性电池电压稳定,放电时间长 |
您最近一年使用:0次

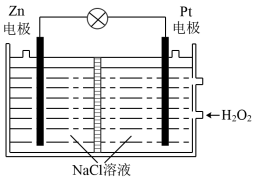
 向
向 电极移动
电极移动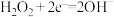
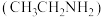 转化成无毒无害物质。下列分析错误的是
转化成无毒无害物质。下列分析错误的是 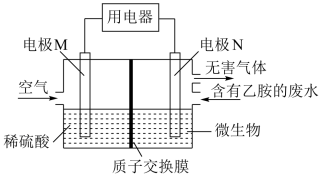
 保持不变
保持不变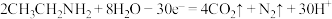
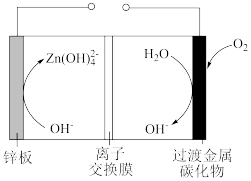
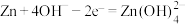
 ,外电路转移电子数约为
,外电路转移电子数约为